
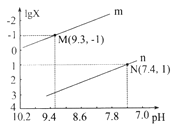
【题目】25℃时,向Na2CO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。
己知:lgX=lg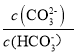 或lg
或lg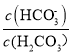 ,下列叙述正确的是
,下列叙述正确的是
A. 曲线m表示pH与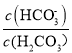 的变化关系
的变化关系
B. 当溶液呈中性时,c(Na+)= ![]() +2
+2![]()
C. Ka1(H2CO3)=1.0×10-6.4
D. 25℃时,CO32-+H2O![]()
![]() +OH-的平衡常数为1.0×10-7.6
+OH-的平衡常数为1.0×10-7.6
【答案】C
【解析】A、碳酸钠溶液中滴加盐酸,发生CO32-+H+=HCO3-,HCO3-+H+=H2O+CO2↑,根据图像,推出曲线m表示的是 ,故A错误;B、根据电中性,c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)+c(Cl-),因为溶液显中性,因此c(H+)=c(OH-),即得出c(Na+) =c(HCO3-)+2c(CO32-)+c(Cl-),故B错误;C、n曲线代表的是
,故A错误;B、根据电中性,c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)+c(Cl-),因为溶液显中性,因此c(H+)=c(OH-),即得出c(Na+) =c(HCO3-)+2c(CO32-)+c(Cl-),故B错误;C、n曲线代表的是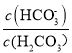 ,根据N点,c(HCO3-)/c(H2CO3)=10,此时c(H+)=10-7.4mol·L-1,根据电离平衡常数的定义,H2CO3的一级电离平衡常数为
,根据N点,c(HCO3-)/c(H2CO3)=10,此时c(H+)=10-7.4mol·L-1,根据电离平衡常数的定义,H2CO3的一级电离平衡常数为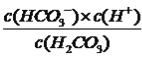 =10×10-7.4=10-6.4,故C正确;D、该反应的平衡常数为
=10×10-7.4=10-6.4,故C正确;D、该反应的平衡常数为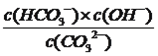 ,根据M点,c(HCO3-)/c(CO32-)=10,c(H+)=10-9.3mol·L-1,c(OH-)=10-4.7mol·L-1,代入数值,得出此反应的化学平衡常数为10-3.7,故D错误。
,根据M点,c(HCO3-)/c(CO32-)=10,c(H+)=10-9.3mol·L-1,c(OH-)=10-4.7mol·L-1,代入数值,得出此反应的化学平衡常数为10-3.7,故D错误。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】下列关于“物质的量”“摩尔”和“摩尔质量”的叙述正确的是( )
A.“物质的量”是国际单位制中的个基本单位
B.1mol任何物质均约含有6.02×1023个分子
C.物质的摩尔质量等于其相对分子质量或相对原子质量
D.0.012kg12C中所含的碱原子数为NA(NA代表阿伏加德罗常数的数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小王要制备纯净的二氧化碳气体,可供选用的仪器如图所示。可供选用的药品如下:①石灰石②澄清石灰水③稀硫酸④浓硫酸⑤盐酸溶液⑥烧碱溶液⑦蒸馏水。下列装置连接顺序及组合最恰当的是( )
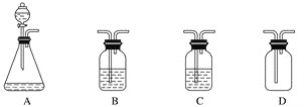
A. A(①⑤)、B(④)、C(⑦)、D B. A(①③)、B(④)、C(⑦)、D
C. A(①⑤)、B(⑦)、C(④)、D D. A(①⑤)、B(⑥)、C(④)、D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z,原子半径依次增大。W、X在同一主族,Y元素在第三周期中离子半径最小,Y和Z的原子序数之和是W的3倍。下列说法正确的是
A. X的简单氢化物的热稳定性比W的强 B. X的氧化物对应的水化物是强酸
C. Z和W形成的化合物可能含有非极性键 D. Z、Y的氧化物是常用的耐火材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色、透明的强酸性溶液中,能大量共存的离子组是( )
A.NH4+、NO3-、Al3+、Cl-B.Na+、SO42-、Ba2+、NO3-
C.MnO4-、K+、SO42-、Na+D.H+、SO42-、HCO3-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出C1O2,C1O2有类似Cl2的性质。某兴趣小组探究亚氯酸钠的制备与性质。

Ⅰ.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量C1O2,充分反应。
(1)仪器a的名称为_______,仪器b的作用是_____。
(2)装置A中生成NaC1O2的离子方程式为_______。
(3)若从装置A反应后的溶液中获得NaClO2晶体,则主要操作有减压蒸发浓缩、降温结晶______、_____干燥等。
Ⅱ.探究亚氯酸钠的性质
停止通ClO2气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
(4)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因_________。
(5)B中现象为_________ 。
(6)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示:
含氧酸酸性强弱与非羟基氧原子数的关系
次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
含氧酸 | Cl—OH |
|
|
|
非羟基氧原子数 | 0 | 1 | 2 | 3 |
酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性强弱相差很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可知它们的结构式分别为①__________,②__________。
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是①__________,②__________。
(3)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况__________,写出反应的化学方程式________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com