
����Ŀ���ݱ�����������M�Է��ѻ�ù���нϺõ��־����ԣ���ϳ�·������ͼ��ʾ��

��֪��
�ش��������⣺
��1��������C�еĺ�������������Ϊ_________��A��B�ķ�Ӧ����Ϊ__________��
��2��A������Ϊ____________
��3��д��D�Ľṹ��ʽ��_____________________________��
��4��д����Ӧ�ڵĻ�ѧ����ʽ��____________________________________________��
��5��������C��������������ͬ���칹����_______�֣�д������һ����5�ֲ�ͬ������ԭ�ӵ�ͬ���칹��Ľṹ��ʽ��_______________��
�ٺ������ṹ�����ڼ��������·���ˮ�⣻
������FeCl3������ɫ��Ӧ��
���ܷ���������Ӧ��
��6����֪CH3CH2CN![]() CH3CH2COOH������
CH3CH2COOH������ ��CH2=CHCN���Ҵ�Ϊԭ�Ϻϳɻ�����
��CH2=CHCN���Ҵ�Ϊԭ�Ϻϳɻ�����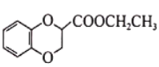 ��д���Ʊ��ĺϳ�·������ͼ�����Լ����ã�____________________
��д���Ʊ��ĺϳ�·������ͼ�����Լ����ã�____________________
���𰸡��Ѽ� ȡ����Ӧ 1,2,4�������� ![]()
![]() 13
13 

��������
����A��B��C������C�� ���Ľṹ��ʽ�в�����λ�á������֪��A�ķ���ʽ��֪AΪ
���Ľṹ��ʽ�в�����λ�á������֪��A�ķ���ʽ��֪AΪ![]() ��BΪ
��BΪ ��Ȼ�����úϳ�ͼ���йصķ�Ӧ��������Ϣ��֪��Ӧ��ΪD��-NO2��ԭΪ-NH2��������ԭ��Ӧ����Ӧ��ΪE��-NH2����һ��Ӧ���-COOH����ȡ����Ӧ���γ��ļ��������÷�Ӧ�ܺ�M�Ľṹ��ʽ������֪E�Ľṹ��ʽΪ
��Ȼ�����úϳ�ͼ���йصķ�Ӧ��������Ϣ��֪��Ӧ��ΪD��-NO2��ԭΪ-NH2��������ԭ��Ӧ����Ӧ��ΪE��-NH2����һ��Ӧ���-COOH����ȡ����Ӧ���γ��ļ��������÷�Ӧ�ܺ�M�Ľṹ��ʽ������֪E�Ľṹ��ʽΪ ��DΪ
��DΪ ���ݴ˷�������
���ݴ˷�������
��������������֪��
��1���ɿ�ͼ ֪AΪ
֪AΪ ��
��
��C�Ľṹ��ʽ ֪C�к���������Ϊ�Ѽ���
֪C�к���������Ϊ�Ѽ��� ��CH2Cl2��һ��������ת��Ϊ
��CH2Cl2��һ��������ת��Ϊ ����������ȡ����Ӧ��
����������ȡ����Ӧ��
�ʴ�Ϊ���Ѽ���ȡ����Ӧ��
��2��AΪ![]() �����ݺ������������ϵͳ��������֪��A������Ϊ1,2,4�������ӣ�
�����ݺ������������ϵͳ��������֪��A������Ϊ1,2,4�������ӣ�
�ʴ�Ϊ��1,2,4�������ӣ�
��3��������������֪��D�Ľṹ��ʽΪ�� ��
��
�ʴ�Ϊ��![]() ��
��
��4����Ӧ����������Ӧ������ʽΪ![]() ��
��
�ʴ�Ϊ�� ![]() ��
��
��5��������CΪ ������ʽΪC8H8O3�������Ͷ�=
������ʽΪC8H8O3�������Ͷ�=![]() ���������ṹ������FeCl3������ɫ��Ӧ�����ǻ������ڼ��������·���ˮ�⣬���ܷ���������Ӧ������������HCOO-�������ݱ����ϵ�ȡ���������ɷ������ۣ���ͬ���칹�����Ϊ����ȡ����Ϊ-OH�����ǻ�����-CH2OOCH������ͬ���칹���ڱ����Ϸֱ�Ϊ�ڼ��λ����3�֣���ȡ����Ϊ-OH�����ǻ�����-CH3��-OOCH����ȡ����ʱ������������һ��������жϳ�����10�֣����Ի�����C������������������ͬ���칹����3+10=13�֣�����һ����5�ֲ�ͬ������ԭ�ӵ�ͬ���칹��Ľṹ��ʽ��
���������ṹ������FeCl3������ɫ��Ӧ�����ǻ������ڼ��������·���ˮ�⣬���ܷ���������Ӧ������������HCOO-�������ݱ����ϵ�ȡ���������ɷ������ۣ���ͬ���칹�����Ϊ����ȡ����Ϊ-OH�����ǻ�����-CH2OOCH������ͬ���칹���ڱ����Ϸֱ�Ϊ�ڼ��λ����3�֣���ȡ����Ϊ-OH�����ǻ�����-CH3��-OOCH����ȡ����ʱ������������һ��������жϳ�����10�֣����Ի�����C������������������ͬ���칹����3+10=13�֣�����һ����5�ֲ�ͬ������ԭ�ӵ�ͬ���칹��Ľṹ��ʽ�� ��
��
�ʴ�Ϊ��13�� ��
��
(6)�ɺϳɲ������������������![]() ���Ҵ������õ����Ȼ���������-CN��ˮ���ã�
���Ҵ������õ����Ȼ���������-CN��ˮ���ã� ��CH2=CHCN�����������Ƚ�CH2=CHCN��Br2�����ӳɷ�Ӧ����±����ٷ���������������A��B�ķ�Ӧ�������ϳ�·��Ϊ��
��CH2=CHCN�����������Ƚ�CH2=CHCN��Br2�����ӳɷ�Ӧ����±����ٷ���������������A��B�ķ�Ӧ�������ϳ�·��Ϊ�� ��
��
�ʴ�Ϊ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X�Ľṹ��ʽ��ͼ������˵������ȷ����

A. X����ʽΪC10H20O�����ǻ�������ͬϵ��
B. X��һ��ȡ������6��
C. X��ʹ���Ը��������Һ��ɫ
D. ��һ�������£�X�ܷ�����ȥ��Ӧ����2��ϩ���������������칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������辧�����������״�ṹ���侧��ģ������ͼ��ʾ��������۲�þ���ģ�ͺ�ش��������⣺

��������ľ����ṹ
(1)�������辧������С��Ϊ________Ԫ����
(2)ÿ����ԭ��Ϊ________����С�����С�
(3)ÿ����С��ƽ��ӵ��________����ԭ�ӡ�________����ԭ�ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1915��ŵ��������ѧ������Henry Bragg��Lawrence Bragg���Ա���������X���߶Ծ���ṹ�ķ��������Ĺ��ף�
(1)��ѧ��ͨ��X����̽����NaCl��KCl��MgO��CaO����ṹ���ƣ��������־���ľ������������±���

4�־���NaCl��KCl��MgO��CaO�۵��ɸߵ��͵�˳����__��
(2)��ѧ��ͨ��X�����Ʋ���мȺ�����λ�����ֺ����������ṹʾ��ͼ�ɼ�ʾ���£�������λ����������������߱�ʾ��

��д����̬Cuԭ�ӵĺ�������Ų�ʽ__������ͭ��������__������ĸ���ţ��ѻ���ʽ��

��д������������ˮ��ͭ���ӵĽṹ��ʽ�����뽫��λ����ʾ������__��
��ˮ���Ӽ��������������о�������ʵ˵�������ˮ�����ʵ�Ӱ��__��
��SO42���Ŀռ乹����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƣ�Na2S2O3�������������Լ������Լ�����ԭ�������ȼ��ȡ�
��ʵ�����Ʊ����������װ��ͼ���¡�

��1������B��������________��
��2��д��װ��B�Ʊ�Na2S2O3�Ļ�ѧ��Ӧ����ʽ____________________________��
��3��NaOH��Һ��������____________________________________��
�������������Ʒ���Ȳ�������
�ٳ�ȡ�����Ƶ������������Ʒ8.0g���250mL��Һ
�ڴӢ�����ȡ20.00mL��Һ����ƿ��
����0.lmol��L-1����Һ�ζ���ʵ������������
�ζ�ǰ������mL�� | �ζ��������mL�� | ����Һ�����mL�� | |
ʵ��һ | 1.20 | 21.00 | 20.00 |
ʵ��� | 0.40 | 19.20 | 20.00 |
ʵ���� | 0.50 | x | 20.00 |
��4���õζ�ʱ������ƿ�м���1��2�ε���Һ��ָʾ������ﵽ�ζ��յ���жϱ���______________��
��5��x������ͼ��ʾ����x=________��������������ݼ���������������Ʒ����Ϊ_______________������֪I2+2Na2S2O3=2NaI+Na2S4O6��

��6�������������ȡ20.00mL�����������Һʱ��δ�������������Һ��ϴ�ζ��ܣ�������Ʒ�Ĵ��Ƚ�______________���ƫ��ƫС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������㶨���ܱ������з�����ӦN2O4(g)![]() 2NO2(g)����H>0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯��������ͼ��ʾ������˵����ȷ����
2NO2(g)����H>0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯��������ͼ��ʾ������˵����ȷ����

A. A��C����ķ�Ӧ���ʣ�A>C
B. A��C�����������ɫ��A�Cdz
C. ��״̬B��״̬A�������ü��ȵķ���
D. A��C���������ƽ����Է���������A>C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ϊ36.5%��Ũ����(�ܶ�Ϊ1.16 g��cm��3)���Ƴ�1 mol��L��1��ϡ���ᡣ��ʵ���ҽ���Ҫ��������220 mL���Իش��������⣺
(1)����ϡ����ʱ��Ӧѡ������Ϊ________mL������ƿ��
(2)��������Ҫ________mLŨ���ᣬ����ȡʱ��ѡ��������Ͳ�е�_____��
A��5 mL B��10 mL C��25 mL D��50 mL
(3)����ȡŨ������������в�����
�ٵ�ϡ�͵�������¶�������һ�º��ز�����ע��250 mL����ƿ�С�
��������ƿ��С�ļ�����ˮ��Һ��������ƿ�̶���1��2 cmʱ�����á�����
����ʢ������ձ���ע������ˮ�����ò�����������ʹ���Ͼ��ȡ�
��������ˮϴ���ձ��Ͳ�����2��3�Σ�����ϴ��Һȫ��ע������ƿ��
���������У���ȷ��˳����(�����)_____�����Т��еIJ����С������������________����
(4)ʹ������ƿ������Һʱ�����ڲ��������������������������Ӱ��������Һ��Ũ��(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)
������ƽ����ʹ�����룩����ʱ�����������������λ�÷ŵߵ���____
������Ͳ��ȡҺ�����ʣ�����ʱ������Ͳ��������Һ��Ũ��____
���ý�ͷ�ιܶ���ʱ�����ӿ̶��ߣ�������Һ��Ũ��____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���ij�ܱ������з�����Ӧ��2A(g)![]() B(g)��C(s)����H>0����0��15 s��c(A)��0.1 mol��L��1����0.07 mol��L��1��������˵����ȷ����(����)
B(g)��C(s)����H>0����0��15 s��c(A)��0.1 mol��L��1����0.07 mol��L��1��������˵����ȷ����(����)
A. 0��15 s����C��ʾ��ƽ����Ӧ����Ϊv(C)��0.001 mol��L��1��s��1
B. 0��15 s��v(B)��0.002 mol��L��1��s��1
C. �����¶�����Ӧ���ʼӿ죬�淴Ӧ���ʼ���
D. ��С��Ӧ��ϵ���������ѧ��Ӧ���ʼӿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������֤�����������̼������Ӧ����ȷ��������װ����ͼ��ʾ(��֪��PdC12��Һ��CO�ܲ�����ɫ��Pd)������˵���������

A. װ�âٵ�������������ȡH2��NH3������
B. װ�â���ʯ��ˮ����Ǻ��ٵ�ȼ�ƾ���
C. װ�âڢ��зֱ�ʢװ����Na2CO3��Һ��ŨH2SO4
D. װ�â����к�ɫ�����������ķ�Ӧ��PdC12+CO+H2O=Pd��+CO2+2HC1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com