
有M、N两种溶液,经测定这两种溶液中含有下列12种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、Fe2+、AlO2-、CO32-、NH4+、SO42-、H+。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
| 实验内容以及现象 | 结论 |
| ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | N中不含 离子 |
| ② | 确定M溶液中含有Na+,不含K+ |
 ③用pH试纸检测M溶液,pH试纸呈蓝色 ③用pH试纸检测M溶液,pH试纸呈蓝色 | |
(1) ①CO32-、SO42- ②取少量M溶液进行焰色反应,焰色为黄色,再透过蓝色钴玻璃观察火焰颜色,不呈紫色。
(2)M 由于N溶液显酸性,又含有Fe2+,与NO3-不能大量共存N溶液呈电中性原则
(3)CO32-、SO42-、Na+、OH-、AlO2-、NO3-
解析试题分析:(1) ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生,说明N溶液中不含CO32-、SO42-,因为CO32-、SO42-能和Ba2+发生复分解反应生成BaCO3和Ba SO4沉淀;②由结论M溶液中含有Na+,不含K+可知本题考查Na+、K+的检验实验操作:取少量M溶液进行焰色反应,焰色为黄色,再透过蓝色钴玻璃观察火焰颜色,不呈紫色。(2)由(1)①知N溶液中不含CO32-、SO42-,则CO32-、SO42-在M溶液中,与CO32-不能大量共存的Fe2+、Al3+在N溶液中;由②知Na+在M溶液中,K+在N溶液中;由③用pH试纸检测M溶液,pH试纸呈蓝色,说明M溶液存在大量OH-,则与OH-不能大量共存的NH4+、H+存在于N溶液中,与H+不能大量共存的AlO2-在M溶液中;由于N溶液中含有H+、Fe2+,不能含有NO3-,因硝酸能把Fe2+氧化为Fe3+,NO3-在M溶液中;根据电中性原则Cl-在N溶液中。综上所述,N溶液中含有H+、Fe2+、、Al3+、K+、NH4+、Cl-,M溶液中含有CO32-、SO42-、Na+、OH-、AlO2-、NO3-。
考点:考查离子检验和离子推断


 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:填空题
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在________ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)现有铜、氯化铁溶液、盐酸、硝酸银溶液、氧化铝、二氧化碳、氧气七种物质,两两能发生反应的反应中,属于离子反应的有 种,属于置换反应的有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图所示是中学化学里常见纯净物A—L间的反应关系,其中A、H、E、F为单质且E、F为气体,B在常温下是无色液体,C是淡黄色固体,L是红褐色固体。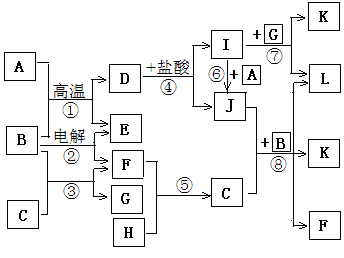
请根据图示判断并回答下列问题:
(1)单质A中所含元素在周期表中的位置是 ;
(2)反应③的化学方程式为 ;
(3)反应④的离子方程式为 ;
(4)反应⑧的离子方程式为 ;
(5)反应②发生过程中,当有3.01×1024个电子发生转移时,电解消耗物质B的质量为 g,同时阴极生成的气体的体积为 L(换算为标准状况下的体积)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有以下物质:①KCI晶体②食盐水③液态的醋酸④I2⑤BaSO4固体⑥蔗糖(C12H22O11 )⑦酒精(C2H5OH)⑧熔融的NaOH⑨K2O⑩SO2。请回答下列问题:
(1)以上物质中能导电的是_________________(用序号)。
(2)以上物质属于电解质的是_________________(用序号)。
(3)以上物质中属于非电解质的是_________________(用序号)。
(4)从②溶液中得到氯化钠固体,应选择下列装置中的______________(填代表装置图的字母,下同);分离④与⑦的混合液,应选择下列装置中的________________。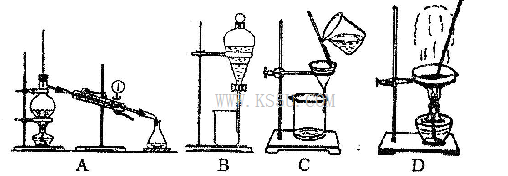
(5)请写出③和⑧中两种物质的溶液混合后发生反应的离子方程式:________________________________________________________________________.
(6)在标准状况下,__________L⑩与34. 2g⑥中含有相同的氧原子数。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)现有以下物质:①NaCl晶体 ②SO2 ③稀硫酸 ④石墨 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精 ⑧熔融的KNO3 ⑨CaO ⑩纯净的醋酸
请回答下列问题(用序号):
以上物质中能导电的是 ;以上物质中属于电解质的是 。
(2)按要求写出下列对应的方程式:
(①电离方程式、②化学方程式、③离子方程式)
①Al2(SO4)3:
②CO2+2OH-=CO32-+H2O:
③NaHCO3与NaHSO4溶液反应:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示: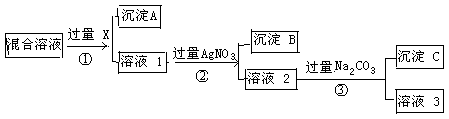
请回答下列问题:⑴写出实验流程中下列物质的化学式
试剂X : 沉淀A:
⑵上述实验流程中加入过量的Na2CO3的目的是 。
⑶按此实验方案得到的溶液3中肯定含有 (填化学式)杂质。
(4)请写出①②中反应的离子方程式①
②
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列物质①NaCl晶体②冰醋酸(纯醋酸晶体) ③干冰 ④铜⑤蔗糖 ⑥熔融的KNO3 ⑦稀硫酸溶液 ⑧酒精 ⑨液氯⑩BaSO4固体
(1)以上物质能导电的是 ;(2)以上物质属于电解质的是 ;(3)以上物质属于非电解质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)(1)环境专家认为可以用金属铝将水体中的NO3-转化为N2,从而消除污染。该反应中涉及的微粒有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将这些微粒中除NO3-以外的微粒填入以下空格内(不用配平)。 
该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应是4Al +3O2+6H2O ="4" Al(OH)3。电池正极的电极反应式是 ;消耗13.5 g Al时转移_________mole-。
(3)铝与某些金属氧化物在高温下的反应称为铝热反应,可用于冶炼高熔点的金属。
已知:4Al(s) +3O2(g) = 2Al2O3(s)△H = -2830 kJ/mol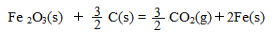 △H = +230 kJ/mol
△H = +230 kJ/mol
C(s)+O2(g) = CO2(g) △H = -390 kJ/mol
铝与氧化铁发生铝热反应的热化学方程式是 ,铝热反应属于______(填字母)反应。
a.氧化还原 b.复分解 c.置换
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(14分)已知:A为含金属离子的淡黄色固体化台物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。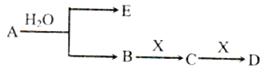
请回答下列问题
(1)这种金属离子的离子结构示意图为_____________;
(2)X的电子式_______________;
(3)B中所含化学键的类型是_____________;
常温常压下,7.8gA与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式
_________________________________________________________________.
(4)①C也可转化为B,写出该转化的化学方程式_______________________________;
②B与D反应的离子方程式为_______________________________________.
(5)将一定量的气体X通入2LB的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量, 产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。
请回答:a点溶液中所含溶质的化学式为__________ ,b点溶液中各离子浓度由大到小的关系是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com