
【题目】研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用子炼铁等。
①已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=akJ·mol-1
C(石墨)+CO2(g)=2CO(g) ΔH2=bkJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为______________。
(2)将CO2转化为甲醇的热化学方程式为: CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H
取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。
①下列情况能说明反应已达平衡状态的是________(填字母)。
A.容器内气体密度不变 B.容器内气体总压强保持不变
C.绝热恒容时,平衡常数不变 D.v正(CH3OH)=3v逆(H2)
②反应过程中测得甲醇的体积分数α(CH3OH)与反应温度T的关系如图所示,则该反应的ΔH______0(填“>”、“<”或“=”)。
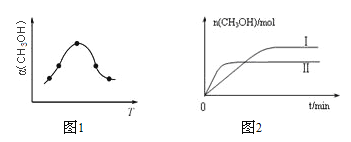
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ_____KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
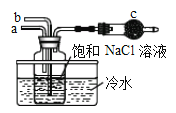
①如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。操作中先在_____处通入NH3气体,然后再在_______处通入CO2气体。
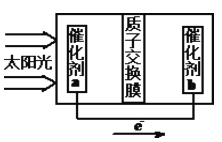
②人工光合作用能够借助太阳能用CO2和水制备化学原料,右图是通过人工光合作用制备HCOOH的原理示意图,请写出催化剂b处的电极反应式:________________。
【答案】 Fe2O3(s)+3CO( g)=2Fe(s) +3CO2(g) △H=(a-3b)kJ/mol BC < > a b CO2+2e-+2H+=HCOOH
【解析】(1)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=akJmol-1,②C(石墨)+CO2(g)=2CO(g)△H2=bkJmol-1,依据盖斯定律①-②×3得到Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=(a-3b)kJmol-1;
(2)①A.体积和质量始终不变,则密度始终不变,无法判断是平衡状态,故A错误;B.反应前后气体的物质的量不等,容器内气体总压强保持不变,说明气体总的物质的量一定,可判断是平衡状态,故B正确;C.平衡常数不变,说明温度不变,在绝热恒容时温度不变,是平衡状态,故C正确;D.当v正(CH3OH)=v逆(H2)时表明平衡状态,故D错误;答案为BC;②由图可知最高点反应到达平衡,达平衡后,温度越高,α(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H<0;
③由图2可知,温度TⅠ<TⅡ,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应移动,升高温度平衡向吸热反应移动,故该反应正反应为放热反应,则△H<0,升高温度,平衡向逆反应移动,所以KⅠ>KⅡ;
(3)①“侯氏制碱法”制取NaHCO3的原理是在饱和食盐水中通入氨气和二氧化碳,而得到NaHCO3的,在这一实验过程中,由于C02在水中的溶解度较小,而NH3的溶解度较大,为防止倒吸,b管通C02,a管通NH3,所以要在食盐水先a管通NH3然后再b管通C02;
②由图可知,左室投入是水,生成氧气与氢离子,催化剂a表面发生氧化反应,为负极,右室催化剂b表面通入二氧化碳,酸性条件下生成HCOOH,电极反应式为CO2+2H++2e-=HCOOH。


科目:高中化学 来源: 题型:
【题目】某组同学为探究草酸浓度对该反应速率的影响,设计下列对照实验:
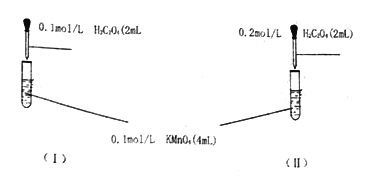
(1)写出上述反应的离子方程式____________。
(2)根据所学知识,你预期的实验现象是:_______(填“l”或“Ⅱ”)中紫色先褪去
(3)实验时,他们发现反应速率的变化从开始后的一段时间内,变化趋势如图,已知反应过程中温度基本不变,分析:
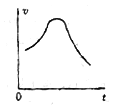
① 反应开始时,速度加块的原因为________;
② 后期反应速度下降的原因为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性无色透明的溶液中,可以大量共存的离子组是
A. K+、NO3ˉ、OHˉ、Clˉ B. SO42-、Al3+、NH4+、Na+
C. Iˉ、Ba2+、Mg2+、NO3ˉ D. Clˉ、SCNˉ、K+、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Cr2(SO4)3的水溶液中加入Na0H溶液,当pH=4.6时,开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多,但当pH≥13时,沉淀消失,出现亮绿色的亚铬酸根离子(CrO2-),其平衡关系为:![]()
向50mL0.05mol/L的Cr2(SO4)3溶液中,加入l.0mol/L的NaOH溶液50mL,充分反应后,溶液中可观察到的现象为
A. 溶液为紫色 B. 溶液中有灰绿色沉淀 C. 溶液为亮绿色 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俗语“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌。“一滴香”的分子结构如图所示,下列说法正确的是
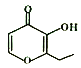
A. 该机物能与Na、NaOH发生反应
B. 1mol该有机物最多能与2molH2发生加成反应
C. 该机物能发生取代、加成、氧化和还原反应
D. 该机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于葡萄糖的叙述中正确的是 ( )
A. 它是果糖的同系物 B. 葡萄糖水解为乙醇和二氧化碳
C. 葡萄糖只有还原性没有氧化性 D. 葡萄糖在人体内发生氧化反应,释放能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.lmol·L-1的三种酸HA、HB和HD溶液,pH随NaOH溶液体积变化如图。下列说法不正确的是( )
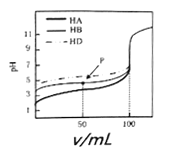
A. HA、HB和HD均为弱酸
B. P点时,c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 三种酸溶液分别被NaOH溶液恰好完全中和后互混:c(HA)+c(HB)+c(HD)=c(OH-) - c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语
回答下列问题:
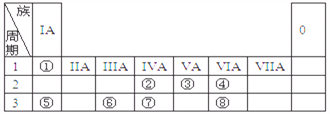
(1)画出⑦的原子结构示意图_______;
(2)②⑤⑥的原子半径由大到小的顺序为_______(填元素符号);②⑦⑧的最高价含氧酸的酸性由强到弱的顺序是_______(填化学式);
(3)②与④的一种化合物是温室气体的主要成分,该物质的结构式为_____________;
(4)①③④⑧四种元素形成的一种化合物既含离子键又含共价键,还可以用作化肥,
该物质的化学式为___________。
(5)⑤⑥⑧的最高价氧化物的水化物之间可以相互反应,请写出⑤⑥两元素最高价氧化物的水化物之间发生反应的离子方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂贮存方法不正确的是
A. 金属钠保存在煤油中 B. 漂白粉密封保存
C. 氢氟酸保存在塑料瓶中 D. 氢氧化钠溶液保存在带磨口玻璃塞的玻璃瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com