
【题目】亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。已知:室温下,2NO+Na2O2====2NaNO2,以木炭、浓硝酸、Na2O2为主要原料制备亚硝酸钠的装置如图所示。(加热装置及部分夹持装置已略去)

回答下列问题:
(1)A装置中反应的化学方程式为__________________________________________。
(2)B装置的作用是_________________________________________________。
(3)充分反应后,C中生成的固体除NaNO2外,还可能生成_________(填化学式),为避免杂质的生成,应在B、C之间加一个为_________装置,该装置和所盛放试剂的名称分别是____________。
(4)检查装置气密性并装入药品后,以下实验操作步骤正确的顺序为_________( (填标号)。
a.打开弹簧夹,向装置中通入N2 b.点燃酒精灯
c.向三颈烧瓶中滴加浓硝酸 d.熄灭酒精灯
e.关闭分液漏斗旋塞 f.停止通入N2
(5)D装置用于尾气处理,写出D中反应的离子方程式:________________________。
【答案】C+4HNO3(浓)![]() CO2+4NO2+2H2O 将NO2转化为NO Na2CO3、NaOH 干燥管 碱石灰 acebdf
CO2+4NO2+2H2O 将NO2转化为NO Na2CO3、NaOH 干燥管 碱石灰 acebdf ![]()
【解析】
试题(1)A中浓硝酸与木炭在加热条件下发生氧化还原反应生成二氧化碳、二氧化氮、水;(2)本实验的目的是2NO+Na2O2====2NaNO2,所以B装置中把NO2转化为NO;(3)从B装置出来的气体含有CO2、H2O,C中Na2O2与CO2、H2O反应生成Na2CO3、NaOH;为避免杂质的生成,用碱石灰吸收 CO2、H2O;(4)NO能与氧气反应生成NO2,先用氮气排出装置中的空气,加入硝酸后加热,反应结束后停止加热,用氮气把装置中的NO全部排入D装置吸收。(5)D中NO被高锰酸钾氧化为硝酸根离子;
解析:(1)浓硝酸与木炭在加热条件下发生氧化还原反应的化学方程式C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O。
CO2↑+4NO2↑+2H2O。
(2)A中生成的二氧化氮进入B中并与水反应,生成了硝酸和 NO,硝酸和铜反应生成NO, D装置的作用是将NO2转化为NO。
(3)从B装置出来的气体含有CO2、H2O,C中Na2O2与CO2、H2O反应生成Na2CO3、NaOH,为避免产生这些副产物应在B、C装置间增加干燥管,药品名称是碱石灰。
(4)NO与氧气反应生成NO2,先用氮气排出装置中的空气,加入硝酸后加热,反应结束后停止加热,用氮气把装置中的NO全部排入D装置吸收。所以实验操作步骤正确的顺序为acebdf;
(5)D中反应的离子方程式![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】CO和H2在一定条件下可以合成乙醇(CH3CH2OH):2CO(g)+4H2(g) ![]() CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
A. CO全部转化为乙醇
B. 正反应和逆反应的化学反应速率均为零
C. 反应体系中乙醇的物质的量浓度不再变化
D. CO和H2以1:2的物质的量之比反应生成乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 质量均为32g的氧气和臭氧含有分子数均为NA
B. 1 L1mol·L-1NaOH水溶液中含有氧原子数为NA
C. 标准状况下,0.224L辛烷完全燃烧生成的CO2分子数为0.08NA
D. 含0.4molHNO3的浓硝酸与足量铜反应,转移的电子数大于0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
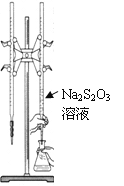
【题目】H2S2O3是一种弱酸,实验室欲用0.01 mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是
A. 该滴定可用甲基橙做指示剂
B. Na2S2O3是该反应的还原剂
C. 该滴定可选用右图所示装置
D. 该反应中每消耗2mol Na2S2O3,电子转移数为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学利用下图装置对电化学原理进行了一系列探究活动。

(1)甲池为装置_______(填“原电池”或“电解池”)。
(2)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,导线中通过_________mol电子。
(3)实验过程中,甲池左侧烧杯中NO3-的浓度_______(填“变大”、“变小”或“不变”)。
(4)其他条件不变,若用U形铜棒代替“盐桥”,工作一段时间后取出铜棒称量,质量___________(填“变大”、“变小”或“不变”)。若乙池中的某盐溶液是足量AgNO3溶液,则乙池中左侧Pt电极反应式为___________________________________,工作一段时间后,若要使乙池溶液恢复原来浓度,可向溶液中加入_____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某液态肼(N2H4)燃料电池被广泛应用于发射通讯卫星、战略导弹等运载火箭中。其中以固体氧化物为电解质,生成物为无毒无害的物质。下列有关该电池的说法正确的是( )

A.a电极上的电极反应式为N2H4+2O2-+4e-=N2↑+2H2O
B.电池内电路中,电流方向:电极a→电极b
C.当电极a上消耗1molN2H4时,电极b上被氧化的O2在标准状况下体积为22.4L
D.b极附近的pH值变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①蔗糖 ②熔融NaCl ③石墨 ④铜丝 ⑤NaOH固体 ⑥SO2 ⑦NaHSO4固体 ⑧K2O固体 ⑨液态H2SO4 ⑩饱和FeCl3溶液
(1)上述物质中可导电的是_________(填序号,下同);上述物质中不能导电,但属于电解质的是_______。
(2)NaHSO4是一种酸式盐,当NaHSO4与Ba(OH)2溶液混合时溶液呈中性,该反应的离子方程式为____________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有______(填序号)和蒸馏水,反应的离子方程式为__________。
(4)某强酸性反应体系中,反应物和生成物共六种为:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 硅晶体和二氧化硅晶体中都含共价键
B. 冰和干冰熔化时克服的作用力均为分子间作用力
C. 硫晶体和硫酸钠晶体均属于离子晶体
D. 氯气和四氯化碳分子中每个原子的最外电子层都形成了具有8个电子的稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的物质转化关系中,A、H为常见的金属单质,其中A为紫红色金属;D、F为气体,其中F为黄绿色气体;B、G为两种常见的酸;由J生成I的反应是电子工业常用的反应。(部分生成物和反应条件未列出)
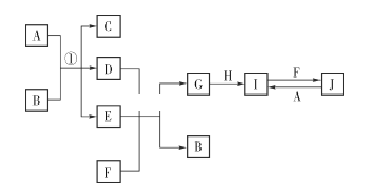
请回答下列问题:
(1)F的电子式为 ____________ 。
(2)G的化学式为 ____________。
(3)写出反应①的化学方程式:______________________________________________
(4)写出由J生成I的离子方程式:______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com