
����Ŀ���ߴ���ˮ�Ȼ��Ⱦ���(SrCl2��6H2O)�����л��ϳɵĴ�������̼���ȿ�ʯ(������BaCO3��FeO��SiO2������)�Ʊ��ߴ���ˮ�Ȼ��Ⱦ���Ĺ�����ͼ��ʾ��
��֪��

I��25�棬Ksp[Fe(OH)3]=1��0��10-38 ��Ksp[Fe(OH)2]=1��0��10-16
��SrCl2��6H2O������61��ʱ��ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ��
��ش�
(1)������н���ʯ�Ƴɽ�Һ�ܼӿ췴Ӧ���ʵ�ԭ����_____________________________��
(2)�ڡ���Һ���м��빤ҵ���ᣬ����ȵĽ��������¶ȡ�ʱ��Ĺ�ϵ��ͼ��ʾ��

�ݴ˺��ʵĹ�ҵ��������Ϊ_________________________��
(3)����ڡ���Һ���м���30����H2O2����������_____________________________(�����ӷ���ʽ��ʾ)��
(4)�����������������Ҫ�ɷֳ�Fe(OH)3�⣬����_______________________(�ѧʽ)��25�棬ΪʹFe3+������ȫ�������ҺpHֵ��СΪ_____________(������Ũ�ȼ�С��1��0��10-5mol��L-1ʱ������Ϊ������ȫ)��
(5)�������������и������˵������ȷ����___________(����)��
A���������60�����ˮԡ�����������о�Ĥ����
B���������ȴ�ᾧ������Ӧͨ��HC1����
C������ݸ���SrCl2��6H2O������Բ��ü�ѹ����
(6)Ϊ�ⶨ����SrCl2��6H2O(Mr=267)������Ʒ�Ĵ��ȣ���������·�������ȡ1��10g��Ʒ�ܽ�������ˮ�У������м��뺬AgNO31��70g��AgNO3��Һ(��Һ�г�Cl-�⣬����������Ag+��Ӧ���ɳ���������)��C1-����ȫ��������Ȼ���ú�Fe3+����Һ��ָʾ������0��100 mol��L-1��NH4SCN����Һ�ζ�ʣ���AgNO3��Һ��ʹʣ���Ag+��AgSCN��ɫ��������ʽ��������___________ʱ�ﵽ�ζ��յ㣬��ȥNH4SCN��Һ20��00 mL����ԭSrCl2��6H2O����Ĵ���Ϊ________________��(����������1λС��)��
���𰸡�����Ӧ��Ӵ���� 40![]() 2Fe2++H2O2+2H+=2Fe3++2H2O SiO2 ��BaSO4 3 AC ���һ��NH4SCN��Һ���룬��ƿ����Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ 97.1
2Fe2++H2O2+2H+=2Fe3++2H2O SiO2 ��BaSO4 3 AC ���һ��NH4SCN��Һ���룬��ƿ����Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ 97.1
��������
��1������Ӱ�컯ѧ��Ӧ���ʵ����أ�����Ӵ�������������¶ȡ�����������Ũ�ȡ����ֽ���ȶ��ܼӿ췴Ӧ���ʽ����жϣ���2������ͼ1��ͼ2�����жϣ���3����̼���ȿ�ʯ(������BaCO3��FeO��SiO2������)�������ˮ�ټӹ�ҵ�����FeO��������ʱ�����������ӣ�˫��ˮ����ǿ�����ԣ����Խ�������������Ϊ�����ӣ����Լ�30����H2O2��ϡ�������������ԭ��Ӧ����Fe2+����ΪFe3+��Ba2+��SO42-����BaSO4������ͨ������pH��ʹ��Һ�е�Fe3+���Fe(OH)3��������ȥ����4�������ܶȻ�������⣻��5�����������Ϣ�������𣻣�6������ʵ����̺�ϵʽ���н��
(1)����Ӱ�컯ѧ��Ӧ���ʵ����أ�����Ӵ�������������¶ȡ�����������Ũ�ȡ����ֽ���ȶ��ܼӿ췴Ӧ���ʡ�������н���ʯ�Ƴɽ�Һ������Ӧ��Ӵ�������ܼӿ췴Ӧ���ʣ��𰸣�����Ӧ��Ӵ������
(2)������Һ���м��빤ҵ���ᣬ�����ȵĽ��������¶ȡ�ʱ��Ĺ�ϵͼ��ͼ1��֪��40��ʱ�ȵĽ�������ߣ���ͼ2��֪60min�ȵĽ�������ߣ����Թ�ҵ�������ʵ�����Ϊ40�棻60min���𰸣�40�棻60min��
(3)���������������������Һ���к���Fe2+������30����H2O2��ϡ���ᣬ�ᷢ��2Fe2++H2O2+2H+=2Fe3++2H2O��H2O2���������������ã��𰸣�2Fe2++H2O2+2H+=2Fe3++2H2O��
(4)�����������������Ҫ�ɷֳ�Fe(OH)3�⣬���в�����ˮ�����SiO2���壬�����й��������ɵ�BaSO4������25�棬Ksp[Fe(OH)3]=1.0��10-38 ��ҪʹFe3+��ȫ������c3(OH-)= Ksp[Fe(OH)3]/ 1.0��10-5=1.0��10-38/1.0��10-5=1.0��10-33�� ����c(OH-)=1.0��10-11mol/L��c(H+)=1.0��10-3����pH=3��ҪʹFe3+������ȫ�������ҺpHֵ��СΪ3���𰸣�SiO2 ��BaSO4��3��
(5) SrCl2��6H2O������61��ʱ��ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ��A���������60�����ˮԡ�����������о�Ĥ���֣��������SrCl2��6H2Oʧȥ�ᾧˮ�����ܼӿ����ʣ���A��ȷ��B����ΪSr�Ľ����Ժ�ǿ��Sr2+����Һ�в��ᷢ��ˮ�⣬���Բ������ȴ�ᾧ�����в���ͨ��HC1���壬��B����C������ݸ���SrCl2��6H2O������ü�ѹ������Լ���SrCl2��6H2O����ʧˮ����C��ȷ���𰸣�AC��
(6) Fe3+Ϊ��ɫ����SCN-����Һ��죻��Fe3+����Һ��ָʾ�������������һ��NH4 SCN��Һʱ����ƿ����Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ��˵���ﵽ�ζ��յ㡣����AgSCN~NH4SCN��֪����AgSCN�����ʵ���n=0.02L��0.100mol/L-1=0.002mol����Cl-��Ӧ��Ag+Ϊ1.70g��170g/mol- 0.002mol=0.008mol������SrCl2��6H2O~2Ag+��֪n(SrCl2��6H2O)=0.004mol��SrCl2��6H2O����Ĵ���=(0.004mol![]() 267g/mol)�� 1.10g��100��=97.1�����𰸣����һ��NH4SCN��Һ���룬��ƿ����Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ��97.1��
267g/mol)�� 1.10g��100��=97.1�����𰸣����һ��NH4SCN��Һ���룬��ƿ����Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ��97.1��


 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǻ�����ij����μӵĻ�ѧ��Ӧ�ķ�Ӧ�����淴Ӧʱ��仯��ʾ��ͼ������������ʾ��ͼ������ϵ���

A. ��Ӧ��ƽ��ʱ������Ӧ���ʺ��淴Ӧ�������
B. �÷�Ӧ�ﵽƽ��̬I������Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��̬II
C. �÷�Ӧ�ﵽƽ��̬I������Ӧ���ѹǿ��ƽ�ⷢ���ƶ����ﵽƽ��̬II
D. ��ƽ��̬I��ƽ��̬IIʱ��ͬһ�ַ�Ӧ��Ũ�Ȳ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽��������̼�ں�����ת�ƺ��ޣ��ǵ������ѧ�о���ǰ�������о����������ں�ˮ�Ķ�����̼��Ҫ����̼��ʽ���ڣ�����HCO3-ռ95%����ѧ��������ͼ��ʾװ�ôӺ�ˮ����ȡCO2�������ڼ��ٻ����������庬����

����˵������ȷ����
A. a����OH-�ڵ缫���ϱ�����
B. b�ҷ�����Ӧ�����ӷ���ʽΪ��H+ + HCO3- = CO2�� + H2O
C. ��·��ÿ��0.2mol ����ͨ��ʱ������0.2mol�����Ӵ�c������b��
D. ��������ȼ�ϵ�ع��磬���ظ������ܷ����ķ�ӦΪ��H2 + 2OH- - 2e- =2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ A��B Ԫ�ص�ԭ�ӽṹʾ��ͼ������˵��������ǣ�������

A.B ��ԭ�ӽṹʾ��ͼ�� x Ϊ 12
B.A �� B �ֱ����ڷǽ���Ԫ�غͽ���Ԫ��
C.A ��ԭ�Ӻ� B ��ԭ�ӷֱ��γɼ����ӵĹ�����ͬ
D.A �� B ����ɻ�ѧʽΪ BA2 �Ļ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��������ͼװ��̽��ͭ��ŨH2SO4�ķ�Ӧ���г�װ�ú�A�м���װ�����ԣ��������Ѽ��飩��
���ϣ���Cu2+�����NaOH��Һ������Ӧ��Cu2++4OH =[Cu(OH)4]2��[Cu(OH)4]2���ڸ����γ����������ɫ��Һ��

��� | ʵ����Ʒ | ʵ������ | |
I | 10mL 15mol/L ŨH2SO4��Һ | ����ͭƬ | ���ҷ�Ӧ��Ʒ����Һ��ɫ��150��ʱͭƬ�������������ɫ�������������ȣ�250��ʱ��ɫ������ʧ�� |
II | 10mL 15mol/L ŨH2SO4��Һ | ����ͭƬ | ���ҷ�Ӧ��Ʒ����Һ��ɫ��150��ʱͭƬ�������������ɫ�������������ȣ�250��ʱ��ɫ������ʧ�� |
��1��A�з�Ӧ�Ļ�ѧ����ʽ��________��
��2����װ��C�������������������Լ�________��
��3��ʵ��I�У�ͭƬ����ĺ�ɫ�������ܺ�CuO��Cu2S��CuS��Ϊ̽����ɫ�����ijɷ֣�ȡ����Ӧ���ͭƬ����ˮС�ij�ϴ�������в�����
|
|
i. ��ɫ�������䣬һ��ʱ����ϲ���Һ����ɫ�� | ii. ��ʼʱ���ϲ���Һ����ɫ��һ��ʱ����ϲ���Һ�ʵ���ɫ�� |
����Ϊͨ����������ʵ��֤����ɫ��������CuO��������________��
����ͬѧ��Ϊ��ͨ����ɫ�жϲ��ܵó��������ۣ�������______����Ҫ����ʵ��iii��˵����ɫ��������CuO��ʵ��iii�IJ�����������_______��
��4����ͬѧ�Ժ�ɫ�����ɷּ���̽������ȫʵ�鷽����
��� | ʵ����� | ʵ������ |
iv | ȡϴ����ĺ�ɫ��������������_____��Һ�����ȡ� | ��ɫ����ȫ���ܽ⣬�Թ��ϲ����ֺ���ɫ���壬�ײ��е���ɫ�������ɡ� |
��5��������������ɫ�����ijɷ֣��������£�
150��ȡ�� | 230��ȡ�� |
ͭԪ��3.2g����Ԫ0.96g�� | ͭԪ��1.28g����Ԫ0.64g�� |
230��ʱ��ɫ�����ijɷ���__________��
��6��Ϊ̽����ɫ������ʧ��ԭ��ȡ230��ʱ�ĺ�ɫ����������ŨH2SO4��������250��ʱ����ɫ�����ܽ⣬�д̼�����ζ���������ɣ��Թܵײ����ֵ���ɫ���壬��Һ�������û�ѧ����ʽ����ԭ��____��
��7���ۺ�����ʵ����̣�˵��Cu��ŨH2SO4����������Ӧ�⣬����������������Ӧ��Ϊ�˱��⸱��Ӧ�ķ�����Cu��ŨH2SO4��Ӧ��ʵ�鷽����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij�Ƽ��о�С���״����һ�����͵�Li+�����ϵ��ԭ��ʾ��ͼ���¡�����ϵ�������ú���I-��Li+��ˮ��Һ���������ù����л��ۺ���������Һ����LiNO3��Һ���ۺ��������ӽ���Ĥ��Ϊ��Ĥ��Һ̬������̬�����ָ���(��֪![]() ��ˮ��Һ�гʻ�ɫ)�������й��ж���ȷ����
��ˮ��Һ�гʻ�ɫ)�������й��ж���ȷ����
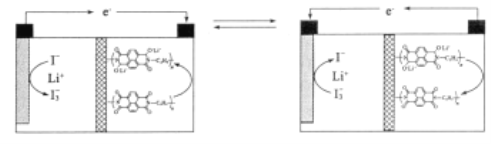
A. ��ͼ��ԭ��ع���ԭ��ͼ
B. �ŵ�ʱ��Li+��������ͨ���ۺ������ӽ���Ĥ
C. �ŵ�ʱ���������������Һ����ɫ����
D. ���ʱ�������ĵ缫��ӦʽΪ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҩƷ��¶�ڿ������ױ���Ϊ�����е����ʣ����в������ڷ���������ԭ��Ӧ��������ǣ� ��
A.![]() B.
B.![]()
C.![]() D.
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. 298Kʱ����Ӧ2Mg(s)��CO2(g)===C(s)��2MgO(s)���Է����У���÷�Ӧ�Ħ�H>0
B. ��ⷨ����ͭʱ����ͭ����������ͭ������
C. �����ᱵ����Һ�м�����������Na2CO3��Һ�����������ó����м������������������˵��Ksp(BaSO4)>Ksp(BaCO3)
D. �����£�pH��Ϊ5���������Ȼ����Һ�У�ˮ�ĵ���̶���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��������ӵ�ص��ܷ�ӦΪ��2Li+FeS= Fe +Li2S�����ҺΪ��LiPF6��SO(CH3)2���л���Һ��Li+������ͨ������ijС���Ըõ��Ϊ��Դ����ˮ����õ�����������ԭ����ͼ��ʾ��

���з�����ȷ����
A. ������ӵ��������ӦΪFeS+2Li++2e-=Fe +Li2S
B. X���ص�Li�缫����
C. ��������c(BaC12)���ֲ���
D. ��ȥ��������Ĥ���������Һϲ�����X�缫�ķ�Ӧ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com