
| n |
| V |
| n |
| V |
| ||
| VL |
| 1 |
| a |
| 1 |
| a |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ��ʼ����ʱ��PH | ��ȫ����ʱ��PH |
| Fe��OH��3 | 1.9 | 3.2 |
| Cu��OH��2 | 4.7 | 6.7 |
| Fe��OH��2 | 6.3 | 9.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
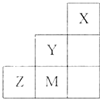
| A����̬�⻯���ȶ���Ϊ��Y��Z��M |
| B�����Ӱ뾶��M-��Z2-��Y- |
| C��ZM2�����и�ԭ�ӵ�����������8�����ȶ��ṹ |
| D������Ԫ���У�Y�ķǽ�������ǿ��Y������������ˮ�����������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
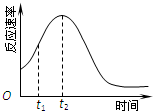 �̲���������KMnO4��H2C2O4�����ᣩ��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ����ӷ���ʽΪ��2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��һʵ��С����ͨ���ⶨ��λʱ��������CO2�����ʣ�̽��ij��Ӱ�컯ѧ��Ӧ���ʵ����أ����ʵ�鷽�����£�KMnO4��Һ���ữ����
�̲���������KMnO4��H2C2O4�����ᣩ��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ����ӷ���ʽΪ��2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��һʵ��С����ͨ���ⶨ��λʱ��������CO2�����ʣ�̽��ij��Ӱ�컯ѧ��Ӧ���ʵ����أ����ʵ�鷽�����£�KMnO4��Һ���ữ����| ʵ����� | A��Һ | B��Һ |
| �� | 20mL 0.1mol?L-1H2C2O4��Һ | 30mL 0.01mol?L-1KMnO4��Һ |
| �� | 20mL 0.2mol?L-1H2C2O4��Һ | 30mL 0.01mol?L-1KMnO4��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com