
【题目】短周期元素A、B、C、D、E的原子序数依次增大,已知:
①C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐;
②A的氧化物是生活中最常见液体,A、E同主族,C与B、D相邻;
③A、B、C、D四种元素组成一种离子化合物F,其组成原子数之比为5︰1︰1︰3。
请回答下列问题:
(1)C的气态氢化物的电子式为___,A在周期表中的位置___。
(2)化合物E2D2中阴、阳离子个数比为___,F含有的化学键类型为___。
(3)F溶液与足量EDA的稀溶液混合,其离子方程式为___。
(4)氯气与C的气态氢化物相遇有白烟及C2生成,写出其化学反应方程式___。
(5)C2A4空气燃料电池是一种环境友好的碱性燃料电池,电解质溶液是20%~30%KOH溶液。该燃料电池的负极反应式为___。
【答案】![]() 第一周期、第IA族 1:2 离子键和共价键 2OH-+HCO3-+NH4+=CO32-+H2O+NH3·H2O 3Cl2+8NH3=6NH4Cl+N2 N2H4+4OH--4e-=4H2O+N2↑
第一周期、第IA族 1:2 离子键和共价键 2OH-+HCO3-+NH4+=CO32-+H2O+NH3·H2O 3Cl2+8NH3=6NH4Cl+N2 N2H4+4OH--4e-=4H2O+N2↑
【解析】
由题干信息,A、B、C、D、E为原子序数依次增大的短周期元素,①C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐,说明C是N元素,最高价氧化物的水化物是硝酸,氢化物是氨气,氨气与硝酸反应生成硝酸铵,属于盐;②A的氧化物是生活中最常见液体,则A是H元素,其氧化物为水,A、E同主族,则E是Na元素;C与B、D相邻,则B是C元素,D是O元素;据此分析解答。
(1)根据上述分析可知,C为N元素,其气态氢化物是氨气,为共价化合物,所以电子式为![]() ,H元素位于元素周期表的第一周期第IA族,故答案为:
,H元素位于元素周期表的第一周期第IA族,故答案为:![]() ;第一周期第IA族;
;第一周期第IA族;
(2)化合物Na2O2中阴离子是O22-,阳离子是Na+,所以阴、阳离子个数比为为1:2,NH4HCO3是离子化合物,含有离子键,但N与H、C与O原子之间是共价键,所以F中含有离子键和共价键,故答案为:1:2;离子键和共价键;
(3)碳酸氢铵与氢氧化钠溶液反应,生成碳酸钠、一水合氨和水,离子方程式为2OH-+HCO3-+NH4+=CO32-+H2O+NH3·H2O,故答案为:2OH-+HCO3-+NH4+=CO32-+H2O+NH3·H2O;
(4)氯气与氨气相遇有白烟及氮气生成,白烟为氯化铵固体,则化学反应方程式为3Cl2+8NH3=6NH4Cl+N2,故答案为:3Cl2+8NH3=6NH4Cl+N2;
(5)N2H4的燃料电池,在碱性条件下,负极为N2H4发生氧化反应,生成氮气和水,所以电极反应式为N2H4+4OH--4e-=4H2O+N2↑,故答案为:N2H4+4OH--4e-=4H2O+N2↑。


科目:高中化学 来源: 题型:
【题目】根据量子力学计算,氮化碳结构有五种,其中一种β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示。下列有关氮化碳的说法不正确的是
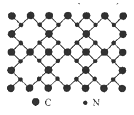
A. 该晶体中的碳、氮原子核外都满足8电子稳定结构
B. 氮化碳中碳显+4价,氮显-3价
C. 每个碳原子与四个氮原子相连,每个氮原子和三个碳原子相连
D. 氮化碳的分子式为C3N4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,X比Y的原子系数小1,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A.Y原子能形成四核18电子的电中性分子
B.元素非金属性的顺序为X>Y>Z
C.W的单质与氧气反应不能产生含共价键的化合物
D.该新化合物中Y不满足最外层8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的有几个()
①质子数相同的微粒一定属于同一种元素
②同一元素的核素种数由中子数决定
③18gH2O中含有的中子数为10NA
④标准状况下,等体积CH4和HF所含的分子数相同
⑤通过化学变化可以实现![]() 与
与![]() 之间的相互转化
之间的相互转化
A.2个B.3个C.4个D.5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示。请回答下列问题:

(1)电极X的材料是________;
(2)X电极发生的电极反应式为____________________;银电极上发生的电极反应为________(填“氧化”或“还原”)反应。
(3)外电路中的电子________(填“流出”或“流向”)Ag电极。
(4)当有3.2 g铜溶解时,银电极增重________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法中,正确的有( )
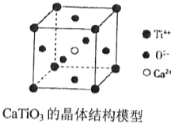
(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
①分子晶体中都存在共价键②在晶体中只要有阳离子就一定有阴离子③铯、钾、钠、钠-钾合金的熔点依次降低④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-相紧邻⑥12g石墨中含有的C-C键的个数为1.5NA(NA为阿伏加德罗常数)⑦晶体中分子间作用力越大,分子越稳定⑧离子晶体CaO的晶格能比KCl高,熔点KCl比CaO低
A. 2种B. 3种C. 4种D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物K是某药物的前体,合成路线如图所示:
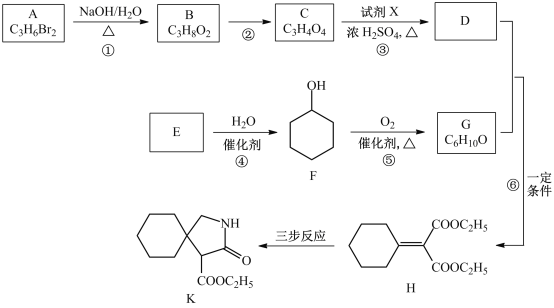
已知:R-CN![]()
![]() ;
;
![]()
![]() +
+![]()
(1)A的名称是_____________。
(2)反应①的化学方程式是___________________。
(3)反应②的类型是__________________。
(4)反应③中的试剂X是________________。
(5)E属于烃,其结构简式是_________________。
(6)H中所含的官能团是_________________。
(7)反应⑥的化学方程式是_____________________。
(8)H经三步反应合成K,写出中间产物I和J的结构简式______________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. PCl3的空间构型为平面三角形
B. HF、HCl、HBr、HI的熔沸点依次升高
C. 乳酸(![]() )有一对手性异构体,因为其分子中含有一个手性碳原子
)有一对手性异构体,因为其分子中含有一个手性碳原子
D. 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碱性电池的总反应为:3HO2-+2Al=OH-+2AlO2-+H2O,工作原理如图所示。下列叙述错误的是
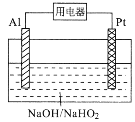
A.电子迁移方向:Al→用电器→Pt
B.电池工作时,负极附近溶液pH减小
C.正极反应式为:HO2-+3H+ +2e-=2H2O
D.负极会发生副反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com