
| 元素编号 | 元素性质或原子结构 |
| A | A原子所处的周期数、族序数、原子序数均相等 |
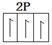
| B | 核外电子有6种不同运动状态 |
| C | 最简单氢化物的水溶液呈碱性 |
| D | 基态原子的S轨道电子数等于P轨道电子数 |
 所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
所得ABCD的结构式为________,分子中C原子的杂化类型是______________。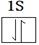
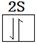
 (2分) (2)N>O>C>H (2分)
(2分) (2)N>O>C>H (2分) NH4++OH- (2分)
NH4++OH- (2分)

 (4)H—C N H—C N→O SP H—O—C N SP3 (5分)
(4)H—C N H—C N→O SP H—O—C N SP3 (5分)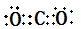 H—N=C=O SP2 (3分) (6)相同(1分)
H—N=C=O SP2 (3分) (6)相同(1分)
 NH4++OH- 。
NH4++OH- 。 。由于分子中氮原子还有1对孤对电子,所以能和氧原子形成配位键,即
。由于分子中氮原子还有1对孤对电子,所以能和氧原子形成配位键,即 。如果没有配位键,要满足稳定结构,则氧原子必需分别和氢原子及碳原子形成共价键,即结构式为
。如果没有配位键,要满足稳定结构,则氧原子必需分别和氢原子及碳原子形成共价键,即结构式为 。该化合物分子中氧原子形成的化学键全部是单键,所以氧原子是sp3杂化。
。该化合物分子中氧原子形成的化学键全部是单键,所以氧原子是sp3杂化。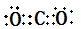 。将D原子换成等电子的
。将D原子换成等电子的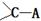 ,则要满足稳定结构,结构式就必需是H—N=C=O,由于该化合物分子氮原子形成1个单键和 1个双键,所以是sp2杂化。
,则要满足稳定结构,结构式就必需是H—N=C=O,由于该化合物分子氮原子形成1个单键和 1个双键,所以是sp2杂化。

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.黑点密度大的区域电子的数目大 | B.黑点密度大的区域电子出现的概率大 |
| C.该图表达了电子呈球形的客观事实 | D.该图表达的是氢原子所特有的电子云 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用金属钠分别与水和乙醇反应,确定水和乙醇分子中羟基氢(-OH)的活泼性强弱 |
| B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱 |
| C.进行H2O和H2S 的热分解实验,确定硫和氧两种元素的非金属性强弱 |
| D.根据Na2CO3和Na2SO3水溶液酸碱性强弱,确定碳和硫两元素非金属性的强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
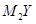 。下列说法正确的是( )
。下列说法正确的是( )| A.还原性:X的氢化物>Y的氢化物>Z的氢化物 |
| B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子 |
C.YX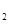 、M 、M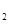 Y都是含有极性键的分子 Y都是含有极性键的分子 |
| D.Z元素的最高价氧化物的水化物的化学式为HZO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.四种元素的原子半径由小到大的顺序为:r(X)<r(Y)<r(Z)<r(W) |
| B.X、Y、Z既能形成离子化合物,又能形成共价化合物 |
| C.X与其余三种元素之间形成的核外电子总数为10的微粒只有4种 |
| D.H2Z的熔点比H2W高,是因为它们的晶体类型不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com