
【题目】铁及其氧化物是日常生活生产中应用广泛的材料,请回答下列问题:
(1)基态铁原子的价电子排布式为_________。
(2)Fe3+、Co3+与N3+、CN-等可形成络合离子。
①C、N、O中第一电离能最大的为________,其原因是_____________________。
②K3[Fe(CN)6]可用于检验Fe2+,1mol K3[Fe(CN)6]中含有σ键的数目为________________。
(3)铁的另一种配合物Fe(CO)x的中心原子价电子数与配体提供的电子数之和为18,则x=_____。已
知该配合物的熔点为-20.5 ℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)x晶体属于_____________(填晶体类型)。
(4)金属铁晶体中原子采用_________堆积,铁晶体的空间利用率为______(用含π的式子表示)。
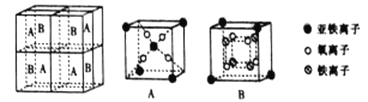
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B 方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为_______________(填最简整数比);已知该晶体的密度为d g·cm-3,阿伏加德罗常数的值为NA,则晶胞参数a为_______________nm(用含d和NA的代数式表示)。
【答案】 3d64s2 N 氮原子2p轨道上的电子半充满,相对稳定,更不易失去电子 12NA 5 分子晶体 体心立方 ![]() π 1∶2∶4
π 1∶2∶4 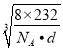 ×102
×102
【解析】(1)基态铁原子的价电子排布式为: 3d64s2
(2)①C、N、O的第一电离能随核电荷数递增呈增大趋势,因N的2p轨道为半充满结构,更不易失去电子,第一电离相对较大,则C、N、O的第一电离最大的为N;
②在配合物![]() 中,
中,![]() 与铁离子之间有6个配位键,在每个
与铁离子之间有6个配位键,在每个![]() 内部有一个σ键,所以
内部有一个σ键,所以![]() 该配合物中含有
该配合物中含有![]() 键的数目为
键的数目为![]() 个或
个或![]() ,
,
(3)配合物![]() 的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,
的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,![]() ,
,![]() ,分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体, 因此,本题正确答案是:5;分子晶体;
,分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体, 因此,本题正确答案是:5;分子晶体;
(4)金属铁晶体原子采用体心立方堆积.铁晶体的晶胞含有2个铁原子,设晶胞边长为a,金属原子半径为r,则面对角线长![]() a,体对角线长
a,体对角线长![]() a=4r,空间利用率=
a=4r,空间利用率=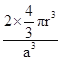 =
=![]() 。
。
(5)A含有1.5个亚铁离子、4个氧离子,B含有0.5个亚铁离子、4个氧离子、4个铁离子,则该氧化物中Fe2+、Fe3+、O2-的个数比为1:2:4。
晶胞含有Fe2+、Fe3+、O2-的个数分别是为4、8、16,它们的相对质量之和是8×232,根据m=ρV可得8×232 g=d×g/cm3a3×NA,a =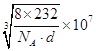 nm。
nm。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃、101kPa时,有以下能量转化图,下列说法不正确的是( )
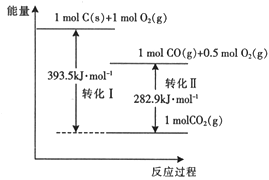
A. 转化Ⅱ的热化学方程式2CO(g)+O2(g)=2CO2(g) △H=-282.9 kJ·mol-1
B. 相同条件下,1mol C(s )和0.5 mol O2(g)总能量高于1mol CO(g)的能量
C. 由C→CO 的热化学方程式2C(s)+O2(g)=2CO(g) △H=-221.2 kJ·mol-1
D. CO2(g)分解为C(s)和O2(g)是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如下:
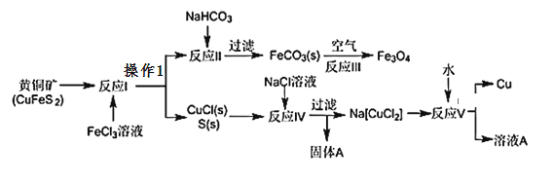
(1)黄铜矿中Cu的化合价是______,反应I中________molFeC13 可氧化0.1mol CuFeS2。
(2)实验室在进行操作1时,除使用烧杯外,还需使用的玻璃仪器有___________。
(3)工业生产中的过滤操作多采用倾析法(倾析法:先把清液倾入漏斗中,让沉淀尽可能地留在烧杯内)分离出固体物质,下列适合用倾析法的有____________。
a.沉淀的颗粒较大 b.沉淀呈胶状 c.沉淀容易沉降 d.沉淀呈絮状。
(4)固体物质A的成分________(写名称),本流程中可实现循环使用的物质除水外还有_______________
(5)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.凡是放热反应的发生均无需加热B.物质发生化学反应都伴随着能量变化
C.凡是需要加热后才能发生的反应是吸热反应D.伴有能量变化的物质变化都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是
加入的物质 | 结论 | |
A | 50mL 1 mol/LH2SO4 | 反应结束后,c(Na+)=c(SO42-) |
B | 0.05molCaO | 溶液中c(OH-) /c(HCO3-) 增大 |
C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
D | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.Na+、Mg2+、Cl﹣、SO42﹣
B.Cu2+、Cl﹣、NO3﹣、OH﹣
C.Ca2+、Na+、CO32﹣、NO3﹣
D.K+、Fe3+、NO3﹣、SCN﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】初中阶段:物质得氧和失氧的反应是氧化还原反应;高中阶段:凡是有元素化合价升降的化学反应都是氧化还原反应。元素化合价升高的为还原剂,发生氧化反应;元素化合价降低的为氧化剂,发生还原反应;氧化反应和还原反应同时发生的,这样的反应称为氧化还原反应。请回答下列问题:
(1)根据化合价改变判断下列四种基本反应类型,一定不是氧化还原反应的是____。(选填宇母序号)
A.化合反应B.分解反应C.置换反应 D.复分解反应
(2)在化学反应Fe+CuSO4=Cu+FeSO4中,该反应的还原剂是_____(填化学式)。
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是________。(多选,选填字母序号)
A.C12+2NaOH=NaCl+NaClO+H2OB.4P+5O2![]() 2P2O5
2P2O5
C.Zn+CuCl2=Cu+ZnCl2 D.3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量V2O5 及一定量Ag2SO4 固体置于恒容真空密闭容器,在一定温度下发生反应: Ag2SO4(s)![]() Ag2O(s) + SO3(g) 2SO3(g)
Ag2O(s) + SO3(g) 2SO3(g)![]() 2SO2(g) + O2(g),10min 后反应达平衡,此时c(SO3)=0.4mol/L,c(SO2)=0.1mol/L。下列说法中,不正确的是
2SO2(g) + O2(g),10min 后反应达平衡,此时c(SO3)=0.4mol/L,c(SO2)=0.1mol/L。下列说法中,不正确的是
A. 平衡时,容器内气体密度为40g/L。
B. 10min 内氧气的平均反应速率为0.005mol·(L·min)-1
C. 再加入少量AgSO4 固体,则反应均向正反应方向移动
D. 该温度下,2Ag2SO4(s)![]() 2Ag2O(s) +2SO2(g) +O2(g)的平衡常数为5×10-4
2Ag2O(s) +2SO2(g) +O2(g)的平衡常数为5×10-4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,在容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
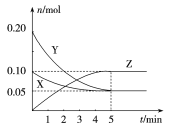
则下列叙述错误的是( )
A. 反应进行到5分钟时达到平衡
B. 25 ℃时,反应可表示为X(g)+3Y(g)![]() 2Z(g)
2Z(g)
C. 增大压强可使反应速率减小
D. 从反应开始到5 min,用Z表示的反应速率为0.01 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com