
����Ŀ������TiO2��Ϳ�ϡ��������ױƷ���������ż���㷺��Ӧ�á��Ʊ�����TiO2�ķ���֮һ��TiCl4ˮ������TiO2xH2O�������ˡ�ˮϴ��ȥ���е�Cl-���ٺ�ɡ����ճ�ȥˮ�ֵõ�����TiO2����������ԭ�ζ����ⶨTiO2������������ȡ17.2gTiO2��Ʒ��һ���������ܽⲢ��ԭΪTi3+������Һ��ˮϡ�����250mL��Һ��ȡ��25.00mL����Һ����ƿ�У��μ�KSCN��Һ��ָʾ������0.5mol/L��NH4Fe(SO4)2����Һ�ζ�Ti3+��ȫ������Ti4+����ش��������⣺
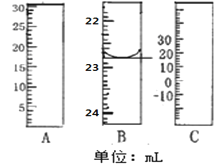
��1����ͼ�ֱ����¶ȼơ���Ͳ���ζ��ܵ�һ���֣�����A����������Ϊ________B����ȷ����Ϊ________��
��2��TiCl4ˮ������TiO2xH2O�Ļ�ѧ����ʽΪ________��
��3���жϵζ��յ��������_____________��
��4���ζ������յ�ʱ������ȥ0.5mol/L��NH4Fe(SO4)2����Һ40.00mL,��ԭ��Ʒ��TiO2��������______________��
��5���ж����в�����TiO2���������ⶨ�����Ӱ�죨����ƫ��������ƫ����������Ӱ��������
���������Ʊ���Һ�����У��ձ��е�NH4Fe(SO4)2��Һ������������ʹ�ⶨ���________��
�����ڵζ��յ��ȡ�ζ��ܶ���ʱ�����ӱ�ҺҺ�棬ʹ�ⶨ���__________��
���𰸡���Ͳ 22.80mL TiCl4��(2��x)H2O= TiO2��xH2O����4HCl �������һ��NH4Fe(SO4)2��Һ����Һ��ɺ�ɫ���Ұ���Ӳ��ָ�ԭ����ɫ 93% ƫ�� ƫ��
��������
��1�������ͼʾ��֪��A�����Ŀ̶��ϴ���С��Ϊ��Ͳ������B�Ŀ̶���С�´�Ϊ�ζ��ܣ�����C��0�̶ȣ�Ϊ�¶ȼƣ�
��2���������Ϣ��֪TiCl4����ˮ�ⷴӦ����TiO2xH2O���������
��3����NH4Fe(SO4)2����Һ�ζ�ʱ��Fe3+��Ti3+����������ԭ��Ӧ��Ti3+��������������Ti4+��Fe3+����ԭΪFe2+�����ﵽ�ζ��յ�ʱ���ټ���NH4Fe��SO4��2��Һ����Һ��Fe3+���������ɺ�ɫ��
��4���ɵ�ʧ�����غ��ԭ�Ӹ����غ����TiO2�����ʵ������ټ�������������
��5�����������Ʊ���Һ�����У��ձ��е�NH4Fe(SO4)2��Һ�������������������ʵ���Ũ�ȼ�С���ζ�ʱ����NH4Fe(SO4)2��Һ���������
�����ڵζ��յ��ȡ�ζ��ܶ���ʱ�����ӱ�ҺҺ�棬��ȡ��NH4Fe(SO4)2��Һ���ƫС��
��1�������ͼʾ��֪��A�����Ŀ̶��ϴ���С��Ϊ��Ͳ������B�Ŀ̶���С�´�Ϊ�ζ��ܣ��ɰ�Һ�����͵��֪����Ϊ22.80mL������C��0�̶ȣ�Ϊ�¶ȼƣ��ʴ�Ϊ����Ͳ��22.80mL��
��2���������Ϣ��֪TiCl4����ˮ�ⷴӦ����TiO2xH2O���������ᣬ��Ӧ�Ļ�ѧ����ʽΪTiCl4��(2��x)H2O= TiO2��xH2O����4HCl���ʴ�Ϊ��TiCl4��(2��x)H2O= TiO2��xH2O����4HCl��
��3������Ti3+����Һ�еμ�KSCN��Һ��ָʾ������Һ���Ժ�ɫ����NH4Fe(SO4)2����Һ�ζ�ʱ��Fe3+��Ti3+����������ԭ��Ӧ��Ti3+��������������Ti4+��Fe3+����ԭΪFe2+�����ﵽ�ζ��յ�ʱ���ټ���NH4Fe��SO4��2��Һ����Һ��Fe3+���������ɺ�ɫ���յ�������Ǽ������һ��NH4Fe(SO4)2��Һ����Һ��ɺ�ɫ���Ұ���Ӳ��ָ�ԭ����ɫ���ʴ�Ϊ���������һ��NH4Fe(SO4)2��Һ����Һ��ɺ�ɫ���Ұ���Ӳ��ָ�ԭ����ɫ��
��4���ɵ�ʧ�����غ��ԭ�Ӹ����غ��֪��n��Fe3+��=n��Ti3+��=n��TiO2��=0.5mol/L��0.04L=0.02mol����ԭ��Ʒ��TiO2��������Ϊ![]() ��100%��93%���ʴ�Ϊ��93%��
��100%��93%���ʴ�Ϊ��93%��
��5�����������Ʊ���Һ�����У��ձ��е�NH4Fe(SO4)2��Һ�������������������ʵ���Ũ�ȼ�С���ζ�ʱ����NH4Fe(SO4)2��Һ�������������TiO2��������ƫ�ߣ��ʴ�Ϊ��ƫ�ߣ�
�����ڵζ��յ��ȡ�ζ��ܶ���ʱ�����ӱ�ҺҺ�棬��ȡ��NH4Fe(SO4)2��Һ���ƫС������TiO2��������ƫ�ͣ��ʴ�Ϊ��ƫ�͡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������1.0 mol/L��NaOH��Һ950 mL������������������ȷ�����������������������ҺŨ��ƫ�ߵ���
A.��ȡ40.0gNaOH����
B.����ƿˮϴ��δ���ֱ��ʹ��
C.����ʱ����
D.ҡ�Ⱥ���Һ����ڿ̶��ߣ�������ˮ��Һ����̶���ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A.NaHS��ˮ�⣺HS��+ H2O![]() S2-+ H3O+
S2-+ H3O+
B.NaHCO3��ˮ��Һ�еĵ��룺HCO3+ H2O![]() H2 CO3+ OH
H2 CO3+ OH
C.NH4Cl��ˮ�⣺NH4+ + H2O �� NH3��H2O + OH
D.��������Һ��̼��������Һ��ϣ� Al3+ + 3HCO3 = Al(OH)3��+3CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1.00mol��L-1�������20.00mL1.00mol��L-1�İ�ˮ�У���ҺpH���¶��������������ı仯������ͼ��ʾ��
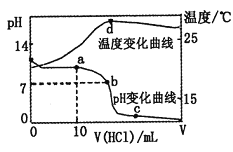
�����й�˵���в���ȷ���ǣ� ��
A. a����Һ������Ũ�ȴ�С��ϵ��c��NH4+����c��Cl-����c��OH-����c��H+��
B. b����Һ������Ũ�ȴ�С��ϵ��c��NH4+��=c��Cl-����c��H+��=c��OH-��
C. c����Һ������Ũ�ȴ�С��ϵ��c��NH4+��+c��H+��=c��Cl-��+c��OH-��
D. d��ʱ��Һ�¶ȴﵽ��ߣ�֮���¶������½���ԭ����NH3��H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����������Ķ������̺�40mL 10mol/LŨ�����ַ�Ӧ������������˵����ȷ����
A.��ʵ���й�����0.1 mol MnO2�����ɱ�״����2.24L����
B.�����ж����д̼�����ζ�����ó���ʯ��ˮ���ն��������
C.���������������ſ���������ˮ���ռ�
D.�ڸ÷�Ӧ�ж�����������������Ũ��������ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л��������ͼ��ʾ��ת����ϵ���й�˵��������ǣ� ��

A.�л���������9��ԭ�ӹ�ƽ��
B.�л���ڿ��Է���ȡ����Ӧ���ӳɷ�Ӧ�ͼӾ۷�Ӧ
C.�л���ۺ��л���ܻ�Ϊͬ���칹��
D.�л���٢ڢۢܶ���ʹ����KMnO4��Һ��ɫ������Ư����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������߶������й���Ӧ���¹ڷ�������ʱ����ȡ�Ĵ�ʩ�����������Ҫ�Ի������г�����������������(ClO2������ɫ������ˮ�����壩��һ�ְ�ȫ�ȶ�����Ч�Ͷ�������������ҵ��ͨ�����Ե缫����Ȼ�狀�����ķ����Ʊ�ClO2��ԭ����ͼ��ʾ������˵����ȷ���ǣ� ��
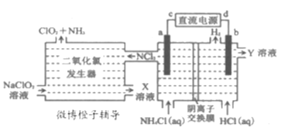
A.cΪ��Դ�ĸ�������b����������Y��Һ��Ũ����
B.����a���Ϸ����ĵ缫��ӦΪNH4+-6e-+3Cl-=NCl3+4H+
C.�������ȷ������ڣ�������������ԭ��Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ6��1
D.����0.3mol������ͨ�����ӽ���Ĥʱ���������ȷ������в���1.12LNH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��±��Ԫ���Ƿǽ����Ժ�ǿ��һ��Ԫ�أ����γɶ������ʡ�
��1�����������������ֻ�ԭ����ͬʱ���ʵ��������ֿɷ�������������ԭ��Ӧ��
�ٽ�����������ͨ�뵽H2S��Һ�У��������õ���Һ�м����������ữ��BaCl2��Һ�ɵõ���ɫ������д��ǰһ����Ӧ�����ӷ���ʽ___________________________________��
�ڽ�0.1molCl2����ͨ�뵽amL��Ũ��Ϊ2mol/L��KOH��Һ�У�����ǡ�÷�Ӧ�꣬�����Һc(ClO��):c(ClO3��):c(Cl��)=2:1:7����a=_________��
��2��KClO3��һ����Ҫ������������ҵ���Ʊ�KClO3�ķ���֮һ���£�
![]()
��д�����ʱ��Ӧ�Ļ�ѧ����ʽ_____________________________________________��
����ͬ�¶��£����������ε��ܽ����Դ�С��NaClO3_____KClO3���������������
��KClO3��MnO2�Ĵ������¼��ȷֽ����������ķ�Ӧ�������£��벹�Ͽհ״���
2KClO3��2MnO2 ![]() 2KMnO4��Cl2����O2����2KMnO4
2KMnO4��Cl2����O2����2KMnO4 ![]() K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2����
K2MnO4 + Cl2��O2��+______________+_______________��
��Ӧ��������������뿪����Ҫ������________________________��
��3����֪Cl2O�������������Cl2Oͨ�뵽ˮ�пɵõ�һ��������Һ����д������Һ���еij��������һ�ֻ�ѧ����___________________������������ͨ�뵽NaOH��Һ��ǡ����ȫ��Ӧ������Һ�и�����Ũ���ɴ�С��˳��Ϊ_____________________��
��4����ͬѧ�ƻ���2L��ʳ��ˮ��AgCl�����������е�1molAg2CO3ת��ΪAgCl����ʽ�����ת����ƽ�ⳣ��__________________________����֪Ksp(AgCl)=1.8��10��10��Ksp(Ag2CO3)=8.4��10��12����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ������˵����ȷ����
A.��H218O��D216O��ɵ�2.0g�������������ӡ���������ΪNA
B.0.1molFe�ֱ��������������������Ӧ��ת�Ƶĵ�������Ϊ0.2NA
C.0.1molAl������NaOH��Һ��Ӧ�������������Ϊ0.3NA
D.25�棬��0.1molCH3COONa����ϡ��������Һ������ʱ����Һ��CH3COO����С��0.1NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com