
【题目】依据事实,写出反应的热化学方程式或计算反应热.
(1)在25℃、101kPa下,1g液态甲醇燃烧生成CO2和液态水时放出22.5kJ热量.则该反应的热化学方程式为_____.
(2)已知下列反应的反应热为:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=﹣880kJ/mol.
②C(s)+O2(g)═CO2(g)△H2=﹣393 kJ/mol.
③H2(g)+![]() O2(g)═H2O(l)△H3=﹣285.8kJ/mol
O2(g)═H2O(l)△H3=﹣285.8kJ/mol
则反应:C(s)+2H2(g)+CO2(g)=CH3COOH(l)△H=_____kJmol﹣1.
【答案】CH3OH(l)+![]() O2(g)═CO2(g)+2H2O(l)△H=﹣725.8kJmol﹣1 ﹣84.6
O2(g)═CO2(g)+2H2O(l)△H=﹣725.8kJmol﹣1 ﹣84.6
【解析】
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,1mol甲醇完全燃烧生成二氧化碳和液态水放热为22.68kJ×32=725.8 kJ,所以甲醇燃烧热的热化学方程式为CH3OH(l)+![]() O2(g)═CO2(g)+2H2O(l)△H=﹣725.8 kJmol﹣1,故答案为:CH3OH(l)+
O2(g)═CO2(g)+2H2O(l)△H=﹣725.8 kJmol﹣1,故答案为:CH3OH(l)+![]() O2(g)═CO2(g)+2H2O(l)△H=﹣725.8 kJmol﹣1;
O2(g)═CO2(g)+2H2O(l)△H=﹣725.8 kJmol﹣1;
(2)据盖斯定律,②+③×2﹣①得C(s)+2H2(g)+CO2(g)=CH3COOH(l)△H=﹣393 kJ/mol+(﹣285.8kJ/mol×2)﹣(﹣880kJ/mol)=﹣84.6 kJ /mol,故答案为:﹣84.6.


科目:高中化学 来源: 题型:
【题目】某同学做“FeSO4被HNO3氧化”的实验,发现溶液变深棕色。猜想可能是生成的NO2或NO与Fe2+或Fe3+反应,使溶液变为深棕色,设计下列装置探究。下列说法错误的是
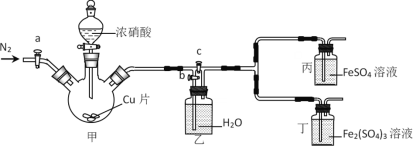
A.先检查装置气密性,加入药品后,关闭c,打开a和b,再通入一段时间N2
B.关闭a、c,打开b及分液漏斗活塞,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明NO与Fe2+反应
C.甲中反应一段时间后,更新丙、丁中试剂,关闭a和b,打开c,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明NO2也可与Fe2+反应
D.该实验的缺陷是缺少尾气吸收装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同条件下,同质量的X、Y两种气体,相对分子质量分别为A、B;则:
(1)X与Y的体积比为_______,分子个数比为 _______,密度比为________;
(2)相同条件下的X、Y两种气体体积相同,则X与Y的质量比为_______,物质的量比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,浓度均为1mol·L-1的CH3NH2和NH2OH两种碱溶液,起始时的体积都为10mL。分别向两溶液中加水进行稀释,所得曲线如图所示(V表示溶液的体积),pOH=-lg[c(OH-)]。下列说法正确的是( )
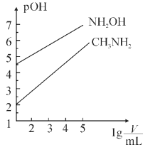
A.当两溶液均稀释至lg![]() =5时,溶液中水的电离程度:NH2OH<CH3NH2
=5时,溶液中水的电离程度:NH2OH<CH3NH2
B.常温下,用盐酸滴定NH2OH时,可用酚酞作指示剂
C.CH3NH3Cl溶液中存在关系:2c(H+)+c(CH3NH)=c(CH3NH2)+2c(OH-)+c(Cl-)
D.等浓度的CH3NH3Cl和NH3OHCl的混合溶液中离子浓度大小关系为:c(NH3OH+)>c(CH3NH+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的容器中进行反应N2(g)+3H2(g) ![]() 2NH3(g),若氮气浓度由0.1 mol·L-1降到0.06 mol·L-1需2 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为
2NH3(g),若氮气浓度由0.1 mol·L-1降到0.06 mol·L-1需2 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为
A. 等于1.8 s B. 等于1.2 s C. 大于1.8 s D. 小于1.8 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值,下列说法正确的是
A. 在标准状况下.11.2L丙烷含有的极性键数目为5NA
B. 7g锂在空气中完全燃烧时转移的电子数为NA
C. 1mol葡萄糖(C6H12O6)分子含有的羟基数目为6NA
D. 常温下,0.2L0.5mol/LNH4NO3溶液中含有的氮原子数小于0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为某研究性学习小组探究金属腐蚀条件的实验装置图,试分析实验并回答下列问题:
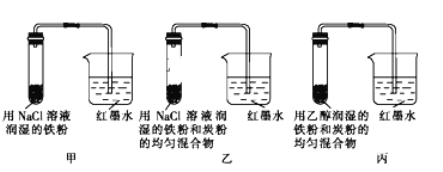
(1)起始时若甲、乙、丙三套装置的导管中液面高度相同,则过一段时间后导管中液面最高的是_____(填装置代号).
(2)通过甲、乙装置的对比实验说明,钢铁中碳的含量越_____(填“高”或“低”)越容易被腐蚀.
(3)乙装置中发生电化学腐蚀时正极的电极反应式为_____.
(4)为防止铁的锈蚀,工业上普遍采用的方法是_____(写出一点即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。下列几种生产乙苯的方法中,最符合原子经济性要求的是(反应均在一定条件下进行)( )
A.![]() +C2H5OH
+C2H5OH![]()
![]() +HCl
+HCl
B.![]() +C2H5OH
+C2H5OH![]()
![]() +H2O
+H2O
C.![]() +CH2=CH2
+CH2=CH2![]()
![]()
D.![]() +NaH
+NaH![]()
![]() +NaBr
+NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,22.4 LCC14中含CC14的分子数为NA
B.0.1 mol/L的NaOH溶液中含OH-的数目为0.INA
C.5.6 g Fe在0.1 mol Cl2中充分燃烧时转移的电子数为0.3NA
D.23 g钠在空气中充分燃烧时转移的电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com