
【题目】在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是
A. CH3OH(l)+3/2O2(g) ![]() CO2(g)+2H2O(l) ;ΔH=+725.8 kJ·mol-1
CO2(g)+2H2O(l) ;ΔH=+725.8 kJ·mol-1
B. 2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol-1
2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol-1
C. 2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) ;ΔH=-725.8 kJ·mol-1
2CO2(g)+4H2O(l) ;ΔH=-725.8 kJ·mol-1
D. 2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) ; ΔH=+1 452 kJ·mol-1
2CO2(g)+4H2O(l) ; ΔH=+1 452 kJ·mol-1
【答案】B
【解析】
A、甲醇燃烧是放热反应,焓变值为负值,则热化学方程式为:CH3OH(l)+3/2O2(g) ![]() CO2(g)+2H2O(l) ;ΔH=-725.8 kJ·mol-1,故A错误;
CO2(g)+2H2O(l) ;ΔH=-725.8 kJ·mol-1,故A错误;
B、1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1 452 kJ,热化学方程式为:2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol-1,故B正确;
2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol-1,故B正确;
C、1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1 452 kJ,热化学方程式为:2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol-1,故C错误;
2CO2(g)+4H2O(l) ;ΔH=-1 452 kJ·mol-1,故C错误;
D、甲醇燃烧是放热反应,焓变值为负值,热化学方程式为:2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) ; ΔH=-1 452 kJ·mol-1,故D错误。
2CO2(g)+4H2O(l) ; ΔH=-1 452 kJ·mol-1,故D错误。
综上所述,本题应选B。


科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰)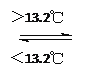 Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,在体积不变的5L密闭容器中,充入2molCO、3molH2发生反应:CO(g)+2H2(g)![]() CH3OH(g),平衡后CH3OH的物质的量为1mol。下列叙述正确的是
CH3OH(g),平衡后CH3OH的物质的量为1mol。下列叙述正确的是
A. 随反应的进行,气体的平均相对分子质量逐渐减小
B. H2的平衡转化率为50%
C. 该温度反应的平衡常数K=25L2·mol-2
D. 平衡后再往容器中通入3mol CO,平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g) + I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
A. 反应物的总能量高于生成物的总能量
B. 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
C. 断开2 mol H-I键所需能量约为(c+b+a) kJ
D. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,ΔS<0的是( )
A.氯化钠溶于水中
B.CaCO3(s)分解为CaO(s)和CO2(g)
C.干冰的升华
D.NH3(g)和HCl(g)反应生成NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据SO2通入不同溶液中的实验现象,所得结论错误的是( )
选项 | 溶液 | 现象 | 结论 |
A | H2O2溶液 | 无明显现象 | SO2与H2O2不反应 |
B | H2S溶液 | 产生淡黄色沉淀 | SO2有氧化性 |
C | 酸性KMO4溶液溶液 | 紫色褪去 | SO2有还原性 |
D | 滴有酚酞的NaOH溶液 | 溶液红色褪去 | SO2有酸性氧化物的性质 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和碳一样也存在一系列氢化物如NH3、N2H4、N3H5、N4H6等。
(1)N3H5的电子式为_______。
(2)已知4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH1=a kJ/mol K1①;
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ΔH2=b kJ/mol K2②;
写出N2与O2反应生成1 mol NO气体的热化学方式程式为________________________;
(3)已知NH3·H2O为一元弱碱,N2H4·H2O为二元弱碱,在水溶液中的一级电离方程式表示为N2H4·H2O+H2O![]() N2H5·H2O++OH-,则可溶性盐盐酸肼(N2H6Cl2)溶液中离子浓度由大到小的顺序为___________________________________。
N2H5·H2O++OH-,则可溶性盐盐酸肼(N2H6Cl2)溶液中离子浓度由大到小的顺序为___________________________________。
(4)如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器均发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
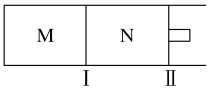
①向M、N中,各通入2 mol N2和6 mol H2。初始M、N容积相同,并保持温度不变。则到达平衡时H2的转化率α(H2)为M________N(填“>”“=”“<”)。
②若在某条件下,反应N2(g)+3H2(g)![]() 2NH3(g)在容器N中达到平衡,测得容器中含有1.0 mol N2、0.4 mol H2、0.2 mol NH3,此时容积为2.0 L。则此条件下的平衡常数为_______。
2NH3(g)在容器N中达到平衡,测得容器中含有1.0 mol N2、0.4 mol H2、0.2 mol NH3,此时容积为2.0 L。则此条件下的平衡常数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在人们的生活经常出现
(1)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下,1mol N2和1molO2完全反应生成NO,会_______________(填“吸收”或“放出”)________kJ能量。
(2)一定温度下,在体积为0.5 L的恒容密闭容器中,氮的气态氧化物X和Y之间反应过程中各物质的物质的量与时间的关系如图所示。
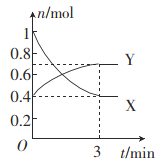
①该反应的化学反应方程式:______________________。
②在0~3 min内,用Y表示的反应速率为____________。
③下列叙述能说明该反应已达到化学平衡状态的是________(填字母)。
a.容器内压强不再发生变化
b.X的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolY的同时生成2nmol X
④反应达到平衡后,若降低温度,则υ(正)______,υ(逆)________。(填“增大”“减小”或“不变”)。
(3)反应 A(g)+3B(g)═2C(g)+3D(g)在四种不同情况下的反应速率分别为:
①υ (A)=0.015mol (Ls)﹣1 ②υ (B)=0.09mol (Ls)﹣1
③υ (C)=2.4mol (Lmin )﹣1 ④υ (D)=0.045mol (Ls)﹣1
该反应在四种不同情况下速率由大到小的顺序为(用序号填空)________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com