
【题目】《化学与生活》
(1)国庆是传统的节日。在外地的人们会乘坐各种交通工具回家与亲人团圆。
① 航空旅行舒适快捷。制造飞机轮胎的主要材料是 (填字母)。
a.铝合金 b.橡胶 c.玻璃
② 铁路是主要的交通工具。建设铁路需要大量水泥。工业上生产水泥的主要原料是石灰石和 (填字母)。
a.黏土 b.纯碱 c.石英
③ 轮船也是重要的交通工具。为保护钢板不受腐蚀,在船尾钢板上镶嵌的金属块是 (填字母)。
a.铜块 b.锌块 c.锡块
(2)国庆节期间聚会要注意饮食健康,保证身体健康。
①平时要多喝水。水在人体中有重要的生理功能。下列物质在人体中可以水解的是 (填字母)
a.葡萄糖 b.氨基酸 c.油脂
②合理选择饮食。鸡、鸭、鱼、肉是常见食材,它们富含的营养物质是油脂和 ;富含淀粉的面点老少皆宜,淀粉的化学式是 ;蔬菜和水果富含维生素C,是人体所必须的。医用维生素C片常在药片外包裹一层“糖衣”,其作用除了改善口感外,更重要的作用是 。
③橙汁是家宴的常用饮品。某品牌橙汁中含有白砂糖、精制盐、柠檬黄和苯甲酸钠,这几种物质中属于着色剂的是 。
④饮食不当会引起胃痛。胃舒平[主要成分是Al(OH)3]可治疗胃酸过多,写出Al(OH)3与胃酸反应的离子方程式 。
(3)国庆期间,在娱乐、购物、旅游时要讲究文明、保护环境。
①蓝天白云是假日出行的最佳天气,“阅兵蓝”为2015年科技热词。较多排放下列气体不利于蓝天出现的是 (填字母)。
a.N2 b. NO2 c.CO2
②用过的聚乙烯塑料食品袋要投入贴有可回收物标志的垃圾箱中。聚乙烯的结构简式是 。
③私家车给假日旅游带来方便,但添堵、污染不可回避。汽车尾气中的CO和NO2在催化剂的作用下可转化为无害气体排出,其化学方程式为 。
【答案】(1)①b(1分)②a(1分)③b(1分)
(2)①c②蛋白质 (C6H10O5)n(1分);防止维生素C被氧化(1分)
③柠檬黄(1分) ④Al(OH)3+3H+=Al3++3H2O(2分)
(3)①b(1分)②![]() ③4CO+2NO2
③4CO+2NO2![]() 4CO2+N2
4CO2+N2
【解析】
试题分析:(1)①制造飞机轮胎的主要材料是橡胶,答案选b;
②工业上生产水泥的主要原料是石灰石和黏土和辅助原料,答案选a;
③为保护钢板不受腐蚀,在船尾钢板上镶嵌的金属的活泼性应该强于铁,铜和锡的金属性弱于铁,锌的金属性强于铁,答案选b;
(2)①a.葡萄糖是单糖,不能水解,a错误;b.氨基酸不能水解,b错误;c.油脂是高级脂肪酸的甘油酯,水解生成甘油和高级脂肪酸,答案选c;
②鸡、鸭、鱼、肉是常见食材,它们富含的营养物质是油脂和蛋白质;淀粉的化学式是(C6H10O5)n;医用维生素C片常在药片外包裹一层“糖衣”,其作用除了改善口感外,更重要的作用是防止维生素C被氧化。
③白砂糖、精制盐、柠檬黄和苯甲酸钠中属于着色剂的是柠檬黄。
④Al(OH)3是两性氢氧化物,与胃酸反应的离子方程式为Al(OH)3 + 3H+ =Al3+ + 3H2O;
(3)①NO2过多排放不利于蓝天出现,答案选b。
②乙烯发生加聚反应生成聚乙烯,聚乙烯的结构简式是![]() 。
。
③汽车尾气中的CO和NO2在催化剂的作用下可转化为无害气体排出,根据原子守恒可知两种气体是氮气和CO2,所以反应的其化学方程式为4CO+2NO2![]() 4CO2+N2。
4CO2+N2。


科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 在化学反应过程中,发生物质变化的同时不一定发生能量变化
B. 破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为吸热反应
C. 生成物的总能量大于反应物的总能量时,反应吸热,ΔH>0
D. ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含丰富的、以离子形式存在的碘元素。如图是实验室从海藻里提取碘的流程的一部分下列判断正确的是( )
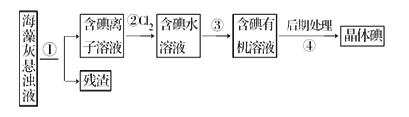
A. 可用淀粉溶液检验步骤②的反应是否进行完全 B. 步骤③中加入的有机溶剂是乙醇
C. 步骤④的操作是过滤 D. 步骤①、③的操作分别是过滤、萃取分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如下 图所示:
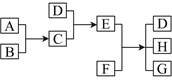
(1)、B在A中燃烧的实验现象为___________,其化学方程式为_____________。
(2)、实验室可用C的浓溶液与一种黑色粉末反应制取A,该反应的离子方程式______________,若反应中转移0.5 mol电子,则生成A的体积(标准状况)为__________L,被氧化的C的物质的量为_________mol。
(3)、E和F反应生成D、H和G的化学方程式为______________,实验室可通过多种方法制备D,用下图所示装置收集D,下列关于制取及收集D实验的叙述正确的是______________(填序号)。
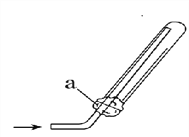
①D气体不能用排水法收集
②实验室用E一种药品可以制取D
③右图中的a为浸有稀H2SO4的棉花
④可用D的浓溶液和生石灰为原料制取D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料,为了分析某AlN样品(样品中的杂质不与NaOH溶液反应)中AlN的含量,某实验小组设计了如下两种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
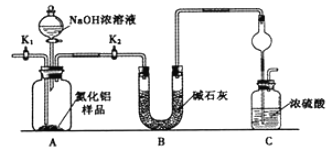
(1)上图C装置中球形干燥管的作用是________________________。
(2)完成以下实验步骤:组装好实验装置,首先检查装置的气密性,再加入实验药品。接下来的实验操作是________,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______________。
(3)由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见_________________。
【方案2】按以下步骤测定样品中A1N的纯度:
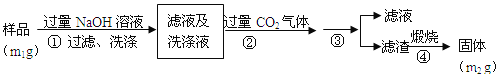
(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作是__________。A1N的纯度是___________(用m1、m2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)乙酸的沸点明显高于乙醛的主要原因是________________。
(2)已知元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2,元素Y基态原子的3p轨道上有4个电子,元素Z的最外层电子数是其内层的3倍。
则①与YZ![]() 互为等电子体的分子的化学式________(任写一种)。
互为等电子体的分子的化学式________(任写一种)。
②X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
③Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是__________________。
(3)已知苯酚( )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________Ka(苯酚)(填“>”或“<”),其原因是______________________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________Ka(苯酚)(填“>”或“<”),其原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一支50mL酸式滴定管,其中盛有溶液,液面恰好在10mL刻度处,现把管内液体全部流下排出,用量筒接收,所得溶液的体积( )
A. 不能确定 B. 为40mL C. 为10mL D. 大于为40mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.非自发反应在任何条件下都不能实现
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.凡是放热反应都是自发的,吸热反应都是非自发的
D.熵增加且放热的反应一定是自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在接触法制硫酸的生产中,SO2转化成SO3转化率的大小直接决定生产效率。某研究小组用下图装置模拟生产过程中测定SO2转化成SO3的转化率。已知SO3的熔点是16.8℃,沸点是44.8℃。装置Ⅰ中所涉及反应的化学方程式为: 。
(1)Ⅱ中的试剂是 ,仪器Ⅵ的名称为 。装置Ⅲ发生反应的化学方程式是 。
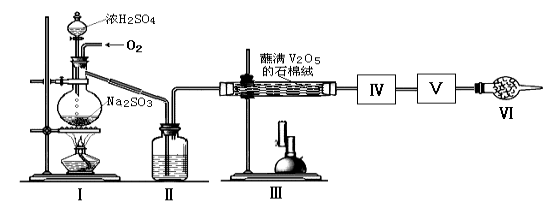
(2)根据实验需要,应该在Ⅳ、Ⅴ处连接合适的装置。请从下图A~D装置中选择最适合装置并将序号填入下面的空格中,Ⅳ、Ⅴ处连接的装置分别是 、 。
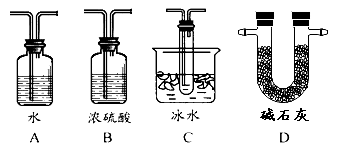
(3)为了提高SO2的转化率,实验时在:①滴加浓硫酸;②加热催化剂的步骤中,应采取的操作是先后顺序_____________(填编号)。
(4)实验结束后,如果把收集SO3的试管敞口露置于空气中,能够看到管口有大量的白雾,产生此现象的原因是 。
(5)用18.9gNa2SO3粉末与足量较浓的硫酸进行此实验,当反应结束时,继续通入O2一段时间后测得装置Ⅴ增重了7.2g,则实验测得SO2的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com