
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号) 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式) 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系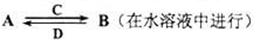
其中C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式 ;D的电子式 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 ;
由A与过量的C反应转化为B的离子方程式 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是 。
(1)Na>Al>C>O>H; (2)C2H2; (3)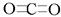 ;
; 
① NaAlO2; AlO2?+2H2O+CO2=Al(OH)3↓+HCO3?。
② CO32?+H2O HCO3?+OH?; c(Na+) >c(HCO3?) >c(CO32?) >c(OH?) >c(H+)。
HCO3?+OH?; c(Na+) >c(HCO3?) >c(CO32?) >c(OH?) >c(H+)。
解析试题分析:根据题意可推知这五种元素分别是X:H;Y:C;Z:O;Q:Na;R:Al. (1)对于电子层数相同的元素来说,原子序数越大。原子半径越小;对于电子层数不同的元素来说,电子层数越多,原子半径越大。所以这五种元素原子半径由大到小的顺序是Na>Al>C>O>H。(2)H与C能形成多种化合物CaHb,其中既含极性键又含非极性键,且相对分子质量最小的物质C2H2. (3) C是溶于水显酸性的气体,是CO2。D是淡黄色固体Na2O2.A为NaAlO2;B为Al(OH)3. CO2的结构式是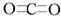 ;淡黄色固体Na2O2的电子式是
;淡黄色固体Na2O2的电子式是 。①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为NaAlO2;由A与过量的C反应转化为B的离子方程式AlO2?+2H2O+CO2=Al(OH)3↓+HCO3?。②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。则A是Na2CO3;B是NaHCO3。Na2CO3是强碱弱酸盐,弱酸根离子水解消耗水电离产生的H+,破坏了水的电离平衡,使水继续电离,最后当达到电离平衡时整个溶液中C(OH-)>C(H+).溶液显碱性的原因用离子方程式表示为CO32?+H2O
。①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为NaAlO2;由A与过量的C反应转化为B的离子方程式AlO2?+2H2O+CO2=Al(OH)3↓+HCO3?。②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。则A是Na2CO3;B是NaHCO3。Na2CO3是强碱弱酸盐,弱酸根离子水解消耗水电离产生的H+,破坏了水的电离平衡,使水继续电离,最后当达到电离平衡时整个溶液中C(OH-)>C(H+).溶液显碱性的原因用离子方程式表示为CO32?+H2O HCO3?+OH?;Na2CO3和NaHCO3浓度均为0.1mol/L的溶液混合。由于二者水解都使溶液显碱性,所以C(OH-)>C(H+),Na2CO3水解的程度比NaHCO3大,所以c(HCO3?) >c(CO32?);Na+不水解,而且二者都电离产生。所以它的浓度最大。因此离子浓度由大到小的顺序c(Na+) >c(HCO3?) >c(CO32?) >c(OH?) >c(H+)。
HCO3?+OH?;Na2CO3和NaHCO3浓度均为0.1mol/L的溶液混合。由于二者水解都使溶液显碱性,所以C(OH-)>C(H+),Na2CO3水解的程度比NaHCO3大,所以c(HCO3?) >c(CO32?);Na+不水解,而且二者都电离产生。所以它的浓度最大。因此离子浓度由大到小的顺序c(Na+) >c(HCO3?) >c(CO32?) >c(OH?) >c(H+)。
考点:考查元素、化合物的推断、转化、盐的水解、离子浓度的大小比较的知识。


科目:高中化学 来源: 题型:填空题
硫酸亚锡(SnSO4)、四氯化锡(SnCl4)常用于印染和电镀工业。
(1)某研究小组设计SnSO4制备路线如下: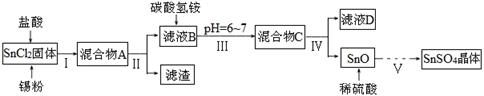
已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化;SnCl2极易水解。
①SnCl2酸溶后加入Sn粉的作用是 。
②步骤Ⅱ中用到的玻璃仪器除烧杯外还有 ;步骤Ⅳ中需要洗涤固体SnO中含有的杂质,检验SnO中的Cl-是否洗涤干净的操作为 。
③步骤Ⅴ涉及到的操作有:a.过滤 b.洗涤 c.蒸发浓缩 d.冷却结晶 e.低温干燥,则其正确的操作顺序为 。
(2)实验室拟用以下装置,用熔融的金属锡与干燥纯净的氯气制取无水SnCl4(SnCl4熔点-33℃,沸点114.1℃,遇潮湿空气极易水解),此反应过程放出大量的热。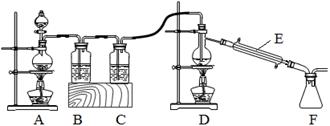
①装置C中应加入试剂为___________;仪器E的名称为____________________。
②反应开始生成SnCl4时,可以先熄灭___(填字母序号)处的酒精灯,理由是________。
③该实验装置设计尚存在缺陷,改进的方法是(包括仪器、试剂及连接位置等)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
完成下列填空
(1)向煤中加入适量的 ,可以大大减少燃烧产物中SO2的量。
(2)铝制品具有良好抗腐蚀性的原因是 。
(3)在少量的胆矾晶体中加入3 mL浓硫酸,片刻后变白色,证明浓硫酸具有 性。
(4)区别氯化铁溶液与氢氧化铁胶体的实验名称是 实验。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)亚硫酸钠中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、Na2S溶液、
Na2SO3溶液、稀硫酸、NaOH溶液、氨水。
(1)要证明Na2SO3具有还原性,应选用的试剂有________,看到的现象是 ________,反应的方程式为___________________________
(2)实验室制取氯气的化学方程式: 括号中为杂质,填上除杂试剂:Cl2中(HCl) 。
(3)由SiO2制取粗硅的化学方程式
(4)将ag由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为 ag (> ;< ;=)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A、B、C、D、E五种主族元素分属三个短周期,且原子序数依次增大。A、C同主族,可形成离子化合物CA;B、D同主族,可形成DB2、DB3两种分子。请回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A、B两种元素能形成两种常温下呈液态的化合物M、N,具有强氧化性的化合物M的电子式可表示为 ;化合物N在同主族元素形成有具有相同结构的物质中,具有较高的沸点,其原因是 。
(3)A、B、C、D中的三种或四种元素能形成多种离子化合物,其水溶液呈碱性的有 (写出所有化合物,用化学式表示,下同),呈酸性的有 (写出所有化合物)。
(4)元素B、E的单质或两元素之间形成的化合物可作水消毒剂的有 (写出其中两种物质的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
五种元素原子半径最大是(写元素符号)
X与Z形成的化合物中,既含极性键又含非极性键的是(写分子式)————
由以上某些元素组成的化合物A、B、C、D有如下转化关系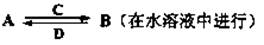
①其中C是溶于水显酸性的气体;D是淡黄色固体。写出C与D反应的化学方程式
②如果A由四种元素组成、B均由三种元素组成,B为两性不溶物,则A为(填名称)
由A与过量C反应转化为B的离子方程式
③如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。则B为(填化学式) 。A、B浓度均为0.1mol/L的混合溶液,碱性较强的是(填溶液名称)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系: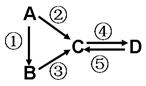
⑴若A是淡黄色固体,C、D是氧化物, C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的两个用途 。
⑵若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式 。
⑶若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置是 。
⑷若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式 。D的化学式是 。
⑸若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是周期表中短周期的一部分。已知X原子最外层电子数比次外层电子数少3个,Z的单质是黄绿色气体。则下列说法中正确的是
| | W | |
| X | Y | Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com