
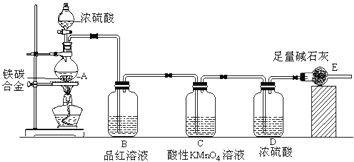
| ||
| ||
| bg |
| 44g/mol |
| 3b |
| 11 |
| 3b |
| 11 |
mg-
| ||
| mg |
| 11m-3b |
| 11m |


 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
| A、分子数 | B、电子数 |
| C、原子数 | D、中子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol?L-1 |
| B、2.0 mol?L-1 |
| C、1.5.mol?L-1 |
| D、1.0 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
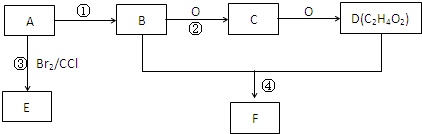
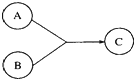 Ⅰ有机物A、B、C有如图所示转化关系,A的分子式为C3H4O2,A可与溴的四氯化碳溶液发生加成反应,1molA能与1molNaHCO3溶液恰好完全反应.B所含元素种类与A相同,是厨房的调味品,其中碳的质量分数为52.2%,氢的质量分数为13%.试回答下列问题,
Ⅰ有机物A、B、C有如图所示转化关系,A的分子式为C3H4O2,A可与溴的四氯化碳溶液发生加成反应,1molA能与1molNaHCO3溶液恰好完全反应.B所含元素种类与A相同,是厨房的调味品,其中碳的质量分数为52.2%,氢的质量分数为13%.试回答下列问题,
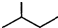 的名称为
的名称为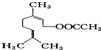
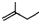
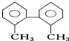 最多
最多查看答案和解析>>
科目:高中化学 来源: 题型:
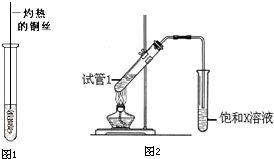
查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 7.54 | 15.08 | 35.00 |
| 二氧化硫的体积/L | 0.672 | 1.344 | 2.688 |
| 硫的质量/g | 0.80 | 1.60 | 3.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原子半径的大小为:Z>Y>X |
| B、气态氢化物的还原性:Z<Y |
| C、若Y可作半导体材料,则X、Z的单质常温下均为气体 |
| D、若Y与Z的核电荷数之和为X的4倍,则X、Z各自形成的氢化物熔沸点:X<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com