
【题目】将Ca(OH)2、NaAlO2、NaOH配成100.0mL混合溶液,向该溶液中通入足量CO2,生成沉淀的物质的量n(沉淀),与通入CO2的体积(标准状况下)V(CO2)的关系,如图所示,下列说法中正确的是( )
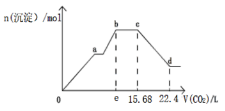
A. 混合溶液中c(NaOH)+c(NaAlO2)=0.4mol/L
B. e点的值为11.2
C. cd段表示Al(OH)3沉淀溶解
D. bc段的化学反应方程式为:NaOH+CO2=NaHCO3
【答案】B
【解析】
A. c点对应溶液为碳酸氢钠,碳元素守恒得到生成碳酸氢钠和碳酸氢钙共消耗二氧化碳![]() =0.7mol,因此碳酸氢钠物质的量=0.7mol0.3mol=0.4mol,钠元素守恒得到,混合溶液中n(NaOH)+n(NaAlO2)=0.4mol,混合溶液体积为100ml,溶液中c(NaOH)+c(NaAlO2)=4.0mol/L,故A错误;
=0.7mol,因此碳酸氢钠物质的量=0.7mol0.3mol=0.4mol,钠元素守恒得到,混合溶液中n(NaOH)+n(NaAlO2)=0.4mol,混合溶液体积为100ml,溶液中c(NaOH)+c(NaAlO2)=4.0mol/L,故A错误;
B. b点对应溶液含碳酸钠,c点对应溶液含碳酸氢钠,d点对应溶液含碳酸氢钠和碳酸氢钙,溶解碳酸钙消耗二氧化碳体积22.4L15.68L=6.72L,物质的量=![]() =0.3mol,原溶液中含0.3molCa (OH)2,c点对应溶液为碳酸氢钠,碳元素守恒得到生成碳酸氢钠和碳酸氢钙共消耗二氧化碳
=0.3mol,原溶液中含0.3molCa (OH)2,c点对应溶液为碳酸氢钠,碳元素守恒得到生成碳酸氢钠和碳酸氢钙共消耗二氧化碳![]() =0.7mol,因此碳酸氢钠物质的量=0.7mol0.3mol=0.4mol,钠元素守恒得到,混合溶液中n(NaOH)+n(NaAlO2)=0.4mol,b点消耗二氧化碳是与偏铝酸钠、氢氧化钙、氢氧化钠反应生成碳酸钙、氢氧化铝和碳酸钠的二氧化碳的总量,Ca (OH)2+CO2=CaCO3↓+H2O,2NaOH+CO2=Na2CO3+H2O,2AlO2+3H2O+CO2=2Al(OH)3↓+CO32,可知二氧化碳物质的量n(CO2)=n(Ca (OH)2)+
=0.7mol,因此碳酸氢钠物质的量=0.7mol0.3mol=0.4mol,钠元素守恒得到,混合溶液中n(NaOH)+n(NaAlO2)=0.4mol,b点消耗二氧化碳是与偏铝酸钠、氢氧化钙、氢氧化钠反应生成碳酸钙、氢氧化铝和碳酸钠的二氧化碳的总量,Ca (OH)2+CO2=CaCO3↓+H2O,2NaOH+CO2=Na2CO3+H2O,2AlO2+3H2O+CO2=2Al(OH)3↓+CO32,可知二氧化碳物质的量n(CO2)=n(Ca (OH)2)+![]() n(NaOH)+
n(NaOH)+![]() n(NaAlO2)=0.3mol+0.2mol=0.5mol,体积为11.2L,故B正确;
n(NaAlO2)=0.3mol+0.2mol=0.5mol,体积为11.2L,故B正确;
C. cd段发生反应CaCO3+CO2+H2O=Ca (HCO3)2,导致沉淀的减少,故C错误;
D. 由上述分析可知,bc段反应的离子方程式是CO32+CO2+H2O=2HCO3,故D错误;


科目:高中化学 来源: 题型:
【题目】有A、B、C、D 四种化合物,分别由K+ 、Ba2+ 、SO42 、CO32、OH中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D的化学式:
A____________;B____________;C_____________;D____________。
(2)写出下列反应的离子方程式:
C与盐酸反应___________________________________________________
B与盐酸反应_______________________________________________________
过量的E与澄清石灰水反应___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法错误的是
A. 实验①中,若5min时测得n(M) =0.05mol,则0至5min时间内,用N表示的平均反应速率v(N) =0.01 mol/( L·min)
B. 实验②中,该反应的平衡常数K= 1.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.06
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,实验操作步骤有:
A.在天平上称取所需硫酸铜固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并恢复至室温
B.把所得的溶液小心地转移到容量瓶中
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡
E.将容量瓶瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)___________________。
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒、药匙,还缺少的仪器是______、___________。
(3)实验过程中需用天平量取___________g无水硫酸铜。
(4)下列情况会使所配溶液浓度偏高的是(填序号)_________________。
a.某同学观察液面的情况如图所示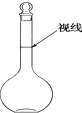
b.没进行上述的操作步骤D
c.加蒸馏水时,不慎超过了刻度线
d.砝码上沾有杂质
e.容量瓶使用前内壁沾有水珠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______,直到因加入一滴盐酸后,溶液由________色变为________色,并________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
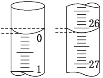
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为_______mL,终点读数为_______mL,所用盐酸溶液的体积为_______mL。
(4)某学生根据3次实验分别记录有关数据如下表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 盐酸的体积/mL | ||
滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在汽车尾气处理装置中发生如下反应:4CO+2NO2![]() 4CO2+N2。下列有关该反应的说法中正确的是
4CO2+N2。下列有关该反应的说法中正确的是
A. NO2是还原剂B. CO被氧化
C. NO2发生氧化反应D. CO得到电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)三月万物复苏,很多人会外出踏青旅游。
①自驾游出行方便。制造汽车轮胎的主要材料是____(填字母)。
a.铝合金 b.橡胶 c.玻璃
②高速列车出行快捷。建设铁路需要大量水泥。工业上生产水泥的主要原料是石灰石和____(填字母)。
a.黏土 b.纯碱 c.石英
③轮船出行舒适。为防止轮船钢板被腐蚀,可在钢板上镶嵌____(填字母)。
a.铜块 b.锡块 c.锌块
(2)旅游期间,在娱乐、购物、旅游时要讲究文明、保护环境。
①用过的聚乙烯塑料食品袋要投入贴有可回收物标志的垃圾箱中。聚乙烯的结构简式是____。
②不法商贩会用由铜锌合金打造的假金首饰欺骗消费者。请写出检验金首饰真假的化学方法和结论____。
③不能携带烟花爆竹乘坐公共交通工具。制作烟花爆竹的黑火药是用木炭、硝酸钾、硫磺配制,黑火药爆炸时会生成氮气、硫化钾和二氧化碳。写出该反应的化学方程式____。
(3)在外出行要注意饮食健康。
①面包、牛奶是常见的食物之一,面包对人体的主要作用是____。牛奶中的蛋白质在人体内水解可生成____。
②为保证营养均衡,应摄入适量蔬菜。蔬菜中的膳食纤维对人体的作用是____。
③橙汁是常用饮品。某品牌橙汁中含有维生素C、白砂糖、精制盐、柠檬黄和苯甲酸钠等成分,这几种物质中属于着色剂的是____。缺少维生素C可能会引发的疾病是____。
④饮食不当会引起胃痛。胃舒平[主要成分是Al(OH)3]可治疗胃酸过多,写出Al(OH)3与胃酸反应的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如图:
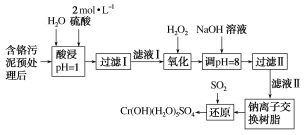
已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
③Cr(OH)(H2O)5SO4是难溶物。
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ | |
沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9)溶解 |
(1)实验室用18.4mol·L-1的浓硫酸配制480 mL2mol·L-1的硫酸,需要量取浓硫酸___mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需____。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:_____。
(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O72-转化为___(填微粒的化学式)。
(4)钠离子交换树脂的反应原理为Mn++nNaR=MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有___。
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式:__。
(6)沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-的浓度,可用标准AgNO3溶液滴定待测液,已知:
银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 黄 | 白 | 砖红 | 白 |
Ksp | 1.8×10-10 | 8.3×10-17 | 1.2×10-16 | 3.5×10-11 | 1.0×10-12 |
滴定时可选为滴定指示剂的是___(填编号),滴定终点的现象是___。
A.NaCl B.K2CrO4 C.KI D.NaCN
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com