
【题目】下列各组液体混合物,用分液漏斗不能分开的是( )
A.苯和水 B.四氯化碳和水 C.乙醇和水 D.正己烷和水
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式或离子方程式(是离子反应的,只写离子方程式).
(1)实验室制氯气: .
(2)氯气溶于水中: .
(3)用石英砂制粗硅: .
(4)用氯化铁溶液制作印刷电路板: .
(5)向偏铝酸钠溶液中通入过量的二氧化碳: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学方程式为 . 利用反应6NO2+8NH3 ![]() 7N2+12H2O也可以处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.
7N2+12H2O也可以处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.
(2)已知:
2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1
2NO (g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1
则反应NO2(g)+SO2(g)SO3(g)+NO (g) 的△H=kJmol﹣1 , 一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 .
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变 d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时的NO2与SO2体积比为1:6,则平衡常数K= .
(3)CO可用于合成甲醇,反应方程式为CO (g)+2H2(g)CH3OH (g).
①CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 .
②甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示:通入a气体的电极是原电池的极(填“正”或“负”),其电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常用做氯化剂或氯磺化剂,如芳香族化合物的氯化、羧酸的氯化及其他各种有机和无机化合物的氯化,也用于制造药品、燃料、表面活性剂等.硫酰氯通常条件下为无色液体,熔点为﹣54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”,100℃以上便开始分解为二氧化硫和氯气,工业上常采用氧化法合成硫酰氯,将干燥的二氧化硫和氯气在一定条件下进行反应,其反应原理和实验装置如下: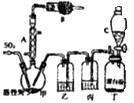
SO2(g)+Cl2(g) ![]() SO2Cl2(l)△H=﹣97.3kJmol﹣1 请回答下列问题:
SO2Cl2(l)△H=﹣97.3kJmol﹣1 请回答下列问题:
(1)仪器A的名称是
(2)干燥管B中盛放的药品是 , 作用是
(3)实验时从仪器C中放出液体的操作方法是
(4)装置乙中盛放的物质为 , 若缺少装置乙,对实验结果有什么影响?
(5)氯磺酸(ClSO3H)是一种无色的发烟液体,有刺激性臭味,沸点178℃,受热分解也能制得硫酰氯,同时还有另外一种物质生成,该反应的化学方程式为 , 分离产物的方法是
A.重结晶 B.过滤 C.蒸馏 D.萃取
(6)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有(填序号)
A.控制气流速度,宜慢不宜快
B.水浴加热三劲烧瓶
C.若三劲烧瓶发烫,可适当降温.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2mol水的摩尔质量和1mol水的摩尔质量
B.200mL1mol/L氯化钙溶液中c(Cl﹣)和100mL2mol/L氯化钾溶液中c(Cl﹣)
C.64g二氧化硫中氧原子数和标准状况下22.4L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在浓度均为1 mol·L-1的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测得其中c(NH![]() ) 分别为a,b,c(mol·L-1),则下列判断正确的是( )
) 分别为a,b,c(mol·L-1),则下列判断正确的是( )
A. c>a>b B. a>b>c C. b>a>c D. a>c>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl﹣、CO32﹣、NO3﹣、SO42﹣ , 且5种离子的物质的量浓度相等.为了进一步探究该水溶液的组成,某同 学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
A.无法确定溶液中是否存在Cu2+离子
B.原溶液中不含K+、Al3+、CO![]() 等离子
等离子
C.根据步骤②只能确定溶液中一定存在NO3﹣离子
D.步骤③所得到的白色沉淀共有2种钡盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.向澄清石灰水中加入等物质的量的NaHCO3溶液:Ca2++2OH﹣+2HCO ![]() ═CaCO3↓+CO
═CaCO3↓+CO ![]() +2H2O
+2H2O
B.向NH4HSO4稀溶液中加入NaOH稀溶液少量:OH﹣+NH ![]() ═NH3?H2O
═NH3?H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
D.向淀粉KI溶液中滴加酸性H2O2溶液,溶液变蓝色:H2O2+2I﹣+2H+═I2+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com