
【题目】某新型药物H(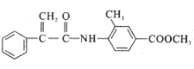 )是一种可用于治疗肿瘤的药物,其合成路线如图所示:
)是一种可用于治疗肿瘤的药物,其合成路线如图所示:

已知:①E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色
②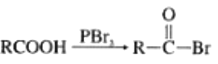 (R为烃基)
(R为烃基)
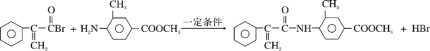
③ +HBr
+HBr
请回答下列问题:
(1)A的结构简式为______________;E的官能团的名称为_____________。
(2)①的化学反应类型是______________;④的反应类型是______________。
(3)写出C→D的化学方程式__________________________________________。
(4)写出F+G→H的化学方程式__________________________________________。
(5)E有多种同分异构体,同时满足下列条件的E的同分异构体有_________种。
ⅰ.能发生银镜反应 ⅱ. 能发生水解反应 ⅲ. 分子中含的环只有苯环
(6)参照H的上述合成路线,设计一条由乙醛和NH2CH(CH3)2为起始原料制备医药中间体CH3CONHCH(CH3)2的合成路线_____________________________________。
【答案】![]() 碳碳双键 羧基 加成反应 消去反应
碳碳双键 羧基 加成反应 消去反应 ![]()
 5
5 ![]()
【解析】
由B的结构简式逆推可知A为![]() ,B发生水解反应生成C为
,B发生水解反应生成C为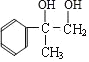 ,结合D的分子式可知C发生氧化反应生成D为
,结合D的分子式可知C发生氧化反应生成D为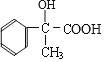 ,E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色,则D是发生消去反应生成E,故E为
,E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色,则D是发生消去反应生成E,故E为![]() ,E发生信息(2)中的反应生成F为
,E发生信息(2)中的反应生成F为![]() ,结合信息(3)及H的结构简式,可知G为
,结合信息(3)及H的结构简式,可知G为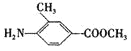 。
。
(1)通过以上分析知,A为![]() ; E为
; E为![]() ,D中官能团为碳碳双键、羧基,故答案为:
,D中官能团为碳碳双键、羧基,故答案为:![]() ;碳碳双键、羧基;
;碳碳双键、羧基;
(2)①的反应类型是加成反应;④的反应类型是消去反应,故答案为:加成反应;消去反应;
(3)C为 ,C发生氧化反应生成D
,C发生氧化反应生成D ,反应方程式为
,反应方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)F为![]() ,G为
,G为 ,F和G发生取代反应生成H为
,F和G发生取代反应生成H为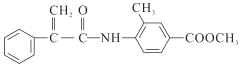 ,反应方程式为
,反应方程式为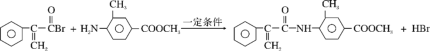 ,故答案为:
,故答案为: ;
;
(5)E(![]() )的同分异构体含有苯环,且同时满足下列条件:①能发生银镜反应②能发生水解反应,说明含有甲酸形成的酯基,③分子中含的环只有苯环,说明苯环侧链含有碳碳双键,只有一个取代基为CH=CHOOCH或C(OOCH)=CH2,有2个取代基为CH=CH2、OOCH,有邻、间、对3种,符合条件的共有5种,故答案为:5;
)的同分异构体含有苯环,且同时满足下列条件:①能发生银镜反应②能发生水解反应,说明含有甲酸形成的酯基,③分子中含的环只有苯环,说明苯环侧链含有碳碳双键,只有一个取代基为CH=CHOOCH或C(OOCH)=CH2,有2个取代基为CH=CH2、OOCH,有邻、间、对3种,符合条件的共有5种,故答案为:5;
(6)乙醛发生氧化反应生成乙酸,乙酸与PBr3作用生成![]() ,最后与NH2CH(CH3)2作用得到CH3CONHCH(CH3)2,合成路线流程图为:
,最后与NH2CH(CH3)2作用得到CH3CONHCH(CH3)2,合成路线流程图为:![]() ,故答案为:
,故答案为:![]() 。
。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O),其实验方案如下:
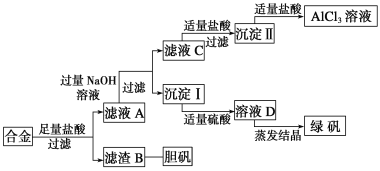
请回答下列问题:
(1)过滤用的玻璃仪器有___________________________________________________。
(2)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:______________________________________________。
写出由沉淀Ⅱ转化为AlCl3溶液的离子方程式:_____________________________。
(3)小组成员经过检测,发现制得的绿矾不纯,试分析其主要含有哪些杂质:_______________________________,要想由沉淀Ⅰ最终制得纯度较高的绿矾,应如何改进___________________________________
(4)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为_______________________________。
(5)有同学提出可将方案中最初溶解合金的盐酸改为烧碱,重新设计方案,也能最终制得三种物质,你认为第二种方案相对于第一种方案________(填“更合理”或“不合理”),理由是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在 100℃时,pH=6,该温度下 0.1molL﹣1 的 NaOH 溶液中,溶液的 pH=_____。
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为_____, 由水电离出的 c(OH﹣)=_____molL﹣1。
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是_____(填“强酸”或“弱酸”),理由是_____。

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
化学式 | 电离常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为________(填化学式)。
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的_________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种典型的强氧化剂,热分解产生锰酸钾、二氧化锰、氧气。完成下列填空:
I. 已知:①MnO2(s)=Mn(s)+O2(g) ΔH=+520kJ/mol
②S(s)+O2(g)=SO2(g) ΔH=-297kJ/mol
③Mn(s)+2O2(g)+S(s)=MnSO4(s) ΔH=-1065kJ/mol
(1)固体MnO2和二氧化硫气体反应生成MnSO4固体的热化学方程式为________________。
II.草酸钠滴定法测定高锰酸钾的质量分数涉及到的反应:
C2O42-+2H+→H2C2O4(草酸)
5H2C2O4+2MnO4-+6H+→2Mn2++10CO2↑+8H2O
(2)上述反应在75~80℃进行比较合适,当加热温度大于90℃时,会导致草酸钠消耗增多,其原因是______________________。
(3)将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应溶液中Mn2+的浓度随反应时间t的变化如图,Mn2+浓度变化由缓慢增大后迅速增大的原因是____________________________。

III .KMnO4是一种常用消毒剂。
(4)KMnO4消毒机理与下列物质相似的是__________(填序号)。
A. 双氧水 B.消毒酒精(75%) C.肥皂水 D. 84消毒液(NaClO溶液)
(5)KMnO4消毒效率(用单位质量转移的电子数表示)是NaClO的______倍(保留两位小数)。
(6)测定KMnO4产品的纯度可用标准Na2SO3溶液滴定。
①配制250ml0.1000mol/L标准Na2SO3溶液,需要使用的玻璃仪器有烧杯、胶头滴管、量筒、玻璃棒和____________。
②取某KMnO4产品0.7000g溶于水,并加入____________进行酸化。
A. 稀盐酸 B.稀硫酸 C.硝酸 D. 次氯酸
③将②所得溶液用0.1000mol/L标准Na2SO3溶液进行滴定,滴定至终点记录实验消耗Na2SO3溶液的体积。重复步骤②、③,三次平行实验数据如表:
实验次数 | 1 | 2 | 3 |
消耗Na2SO3溶液体积/ml | 19.30 | 20.98 | 21.02 |
(有关离子方程式为:2MnO4- + 5SO32- + 6H+ =5SO42- + 2Mn2+ + 3H2O)
计算该KMnO4产品的纯度为__________。(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2=-58 kJ/mol
CH3OH(g)+H2O(g) △H2=-58 kJ/mol
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3=+41 kJ/mol
CO(g)+H2O(g) △H3=+41 kJ/mol
回答下列问题:
(1)CO2的电子式是 。
(2)△H1= kJ/mol,①反应正向的熵变△S 0(填>、<或=)。
(3)在容积为2L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图像如图,下列说法正确的是__________(填序号)
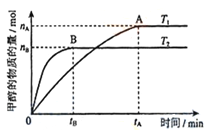
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tA mol/(L·min)
②当v(CH3OH) = v(H2O)时,说明反应达到平衡
③混合气体的平均相对分子质量A点大于B点
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入2L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;T1温度,反应CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)的平衡常数数值为__________。
CO2(g)+3H2(g)的平衡常数数值为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B. 室温下,1 L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.含![]() 个离子的固体
个离子的固体![]() 溶于水配成1L溶液,所得溶液中
溶于水配成1L溶液,所得溶液中![]() 的物质的量浓度为2
的物质的量浓度为2![]()
B.![]() 在空气中长期放置变浑浊的离子方程式为:
在空气中长期放置变浑浊的离子方程式为:![]()
C.可以用澄清石灰水鉴别![]() 和
和![]()
D.滴加KSCN显红色的溶液中存在:![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了研究氯气的性质,做以下探究实验。向KI溶液通入氯气溶液变为黄色;继续通入氯气一段时间后,溶液黄色退去,变为无色;继续通入氯气,最后溶液变为浅黄绿色,查阅资料:I2+I-I3-,I2、I3-在水中均呈黄色。

(1)为确定黄色溶液的成分,进行了以下实验:取 2~3 mL 黄色溶液,加入足量 CCl4,振荡静置,CCl4层呈紫红色,说明溶液中存在______,生成该物质的化学方程式为______,水层显浅黄色,说明水层显黄色的原因是______;
(2)继续通入氯气,溶液黄色退去的可能的原因______;
(3)NaOH 溶液的作用______,反应结束后,发现烧杯中溶液呈浅黄绿色,经测定该溶液的碱性较强,一段时间后溶液颜色逐渐退去,其中可能的原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com