
【题目】已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l),反应一段时间后测得c(AsO43-)为amol·L-1。下列说法能判断反应达到平衡状态的是
AsO43-(aq)+2I-(aq)+H2O(l),反应一段时间后测得c(AsO43-)为amol·L-1。下列说法能判断反应达到平衡状态的是
A.c(I-)=2a mol·L—1
B.v (I-)=2v(AsO43-)
C.c(AsO43-)/c(I-)不再变化
D.溶液的pH不再变化
【答案】D
【解析】
当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、含量不变,以及由此衍生的一些量也不发生变化。
A.该反应从反应物开始投料,AsO43-和I-同为生成物,c(AsO43-)和c(I-)的比例总是1:2,因此不能说明反应是否达到平衡状态,A项错误;
B.AsO43-和I-同为生成物,其速率之比始终是1:2,所以v (I-)=2v(AsO43-)不能作为平衡的判断依据,B项错误;
C.该反应从反应物投料开始,由离子方程式可知c(AsO43-)/c(I-)始终是1:2,所以c(AsO43-)/c(I-)不变不能作为平衡的判断依据,C项错误;
D.如果反应向右进行,则pH逐渐减小,因此当溶液pH不变时,也就是c(OH-)保持不变时,反应达到平衡状态,D项正确;
所以答案选择D项。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质,下列实验现象和结论一致且正确的是( )
A.使酚酞溶液变红,说明溶液显酸性
B.溶液呈现黄绿色,且有刺激性气味,说明有 Cl2 存在
C.先加入HCl溶液酸化,再加入AgNO3溶液产生白色沉淀,说明有 Cl-存在
D.新制氯水放置数天后酸性将减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列五组物质:A、 O2和O3 B 、![]() Cl和
Cl和![]() Cl C 、CH4 与C7H16 D、CH3CH2CH2CH3 与
Cl C 、CH4 与C7H16 D、CH3CH2CH2CH3 与 E、
E、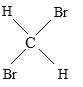 与
与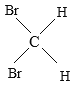
(1)______组两种物质互为同位素;
(2)______组两种物质互为同素异形体;
(3)______组两种物质互为同系物;
(4)______组两种物质互为同分异构体;
(5)______组两种物质实为同一物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是一种重要金属,号称国防金属。某设计小组利用硼镁矿制备镁和硼的流程如下:
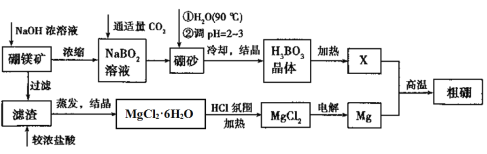
已知:硼镁矿的主要成分Mg2B2O5·H2O,硼砂的化学式为Na2B4O7·10H2O,回答下列问题:
(1)Mg2B2O5·H2O中B的化合价为________。在90℃的热水中,加入稀硫酸调节pH=2~3生成硼酸(H3BO3),反应的离子方程式为__________。
(2)硼的化合物种类繁多,NaBH4是有机合成中常见的还原剂,NaBH4的电子式为______。
(3)将MgCl2·6H2O置于HCl氛围中加热的目的是_____,Mg与X在高温下反应的化学方程式为________。
(4)若向硼镁矿中加入0.1 mol/L盐酸溶液,充分反应后测得溶液的pH=2时,溶液中c(Mg2+)为__________________________________(忽略溶液体积的变化)。
(5)电解熔融的无水氯化镁所得的镁蒸汽在特定的环境里冷却后即为固体镁,下列物质中可以作镁蒸汽的冷却剂的是_________(填字母序号)
A氦气 B氮气
C水蒸气 D二氧化碳气体 E氯气
(6)Mg-H2O2是一种以海水为电解质(加入一定量的酸)的新型电池。该电池的负极材料为_____,正极的电极反应为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.一定条件下,3molH2和1molN2充分反应后,可得2NA个NH3分子
B.室温下,1LpH=1的HCl溶液中,由水电离的H+数目为0.1NA
C.0.1mol金属Na在空气中完全氧化生成Na2O和Na2O2,转移的电子数为0.1NA
D.1mol/L的NaCN溶液中含CN-和HCN的数目之和为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AG表示溶液酸度:![]() 。常温下,用0.1mol/L的NaOH溶液滴定25 ml 0.1mol/L的CH3COOH滴定结果如图所示,下列分析正确的是()
。常温下,用0.1mol/L的NaOH溶液滴定25 ml 0.1mol/L的CH3COOH滴定结果如图所示,下列分析正确的是()
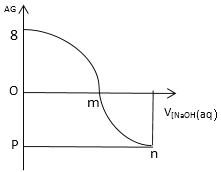
A.0.1mol/L的 CH3COOH溶液的pH=3
B.m点加入NaOH的体积为25mL
C.若pH=7,则溶液中水电离的c(OH-)=1.0×10-3.5 mol/L
D.随着NaOH溶液滴入,溶液中水的电离程度逐渐增大,m点最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产生活中常用84消毒液杀菌消毒。化学课外小组用Cl2和NaOH固体制取84消毒液。请回答下列问题:
(1)制取84消毒液的离子方程式为______________________。
(2)制取84消毒液需要4.0 mol·L-1的NaOH溶液100mL,配制时称量NaOH固体的质量为________,配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、_________。
(3)该消毒液也用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出化学反应方程式__________________。
(4)84消毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,化学课外小组同学向溶液中滴加紫色石蕊试液,出现______________现象,证明消毒液已失效。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。
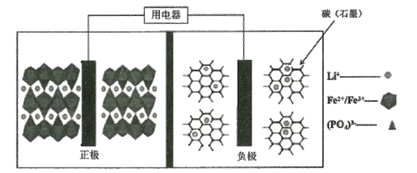
原理如下:(1-x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC。
LiFePO4+nC。
下列说法不正确的是
A.放电时,正极电极反应式:xFePO4+xLi++xe-=xLiFePO4
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式:xLi++xe-+nC=LixCn
D.充电时,当导线中传递l mol电子,理论上将有1 mol Li+向左移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com