
【题目】含有A+、B3+、C3+ 三种金属阳离子的水溶液发生了如下一系列变化后逐一沉淀出来,其中B3+转入白色沉淀:
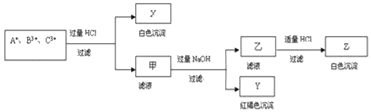
请通过分析回答(用化学符号填写):
(1)A+是__,B3+是__,C3+是__;
(2)X是__,Y是__,Z是__;
(3)写出下列离子方程式:
①生成Y沉淀:__;②B3+与过量氨水反应:__;
(4)写出下列化学方程式:单质铝和Y分解后的固体产物反应:__.
【答案】Ag+ Al3+ Fe3+ AgCl Fe(OH)3 Al(OH)3 Fe3++3OH﹣═Fe(OH)3↓ Al3++3NH3H2O═Al(OH)3↓+3NH4+ 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
【解析】
含有A+、B3+、C3+ 三种金属阳离子的水溶液,加入过量盐酸反应过滤得到白色沉淀X和滤液甲,白色沉淀只能是氯化银沉淀,说明A+离子为Ag+,滤液甲中加入过量氢氧化钠溶液过滤得到红褐色沉淀Y为Fe(OH)3,滤液乙中加入适量盐酸反应生成白色沉淀Z为Al(OH)3,其中B3+转入白色沉淀,则B3+、C3+ 离子分别为:Al3+、Fe3+,据此回答;
(1)由上述分析可知A+、B3+、C3+ 三种金属阳离子分别为:Ag+、Al3+、Fe3+,
答案为:Ag+;Al3+;Fe3+;
(2)分析可知对应X、Y、Z分别为:AgCl、Fe(OH)3、Al(OH)3;
故答案为:AgCl; Fe(OH)3;Al(OH)3;
(3)①生成Y沉淀的离子方程式为:Fe3++3OH﹣═Fe(OH)3↓;
故答案为:Fe3++3OH﹣═Fe(OH)3↓;
②Al3+与过量氨水反应生成氢氧化铝沉淀和铵根离子,离子方程式为:Al3++3NH3H2O═Al(OH)3↓+3NH4+;
故答案为:Al3++3NH3H2O═Al(OH)3↓+3NH4+;
(4)氢氧化铁分解产物是氧化铁,铝与氧化铁在高温下反应生成铁和氧化铝,放出大量的热,反应方程式为:2Al+Fe2O3![]() 2 Fe+Al2O3;
2 Fe+Al2O3;
故答案为:2Al+Fe2O3![]() 2 Fe+Al2O3。
2 Fe+Al2O3。


科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是
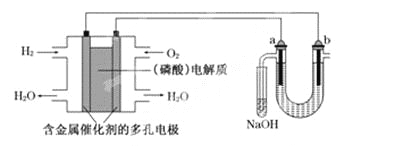
A. 电池工作时,正极反应式为: O2+2H2O+4e-===4OH-
B. 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C. 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D. 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用废弃旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示:

下列叙述错误的是( )
A. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2
B. 铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的H2O2
C. 与加入锌粉反应的离子为Cu2+、H+
D. “过滤”操作后,将滤液蒸干、高温灼烧即可制取纯净的ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为
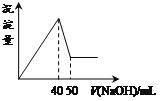
A.1:3B.1:2C.1:1D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑、FeSO4+H2C2O4+2H2O=FeC2O4·2H2O↓+H2SO4、2FeC2O4·2H2O+H2O2+H2C2O4+3K2C2O4=2K3[Fe(C2O4)3]+6H2O、2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O。回答下列问题:
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。下列吸收装置正确的是_____。
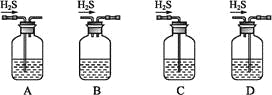
(2)在将Fe2+氧化的过程中,需控制溶液温度不高于40 ℃,理由是_______;得到K3[Fe(C2O4)3]溶液后,加入乙醇的理由是________。
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤__________(叙述此步操作),⑥计算。步骤③若未在干燥器中进行,测得的晶体中所含结晶水含量____(填“偏高”“偏低”或“无影响”);步骤⑤的目的是_______________。
(4)晶体中C2O42-含量的测定可用酸性KMnO4标准溶液滴定。称取三草酸合铁(Ⅲ)酸钾晶体m g溶于水配成250 mL溶液,取出20.00 mL放入锥形瓶中,用0.010 0 mol·L-1酸化的高锰酸钾溶液进行滴定。
①下列操作及说法正确的是___。
A.滴定管用蒸馏水洗涤后,即可装入标准溶液
B.装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量标准液,使尖嘴充满液体
C.接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴
②有同学认为该滴定过程不需要指示剂,那么滴定终点的现象为________,若达到滴定终点消耗高锰酸钾溶液V mL,那么晶体中所含C2O42-的质量分数为____(用含V、m的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷具有类似樟脑气味的无色晶体,其衍生物在医药方面有着重要的用途。以化合物X为起始原料没生一系列反应制得金刚烷(Z)的过程如图所示,下列说法不正确的是

A. X的分子式为C10H12
B. X生成Y的反应为还原反应
C. Y和Z互为同分异构体
D. Z和环已烷属于同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在新制氯水中滴加NaOH溶液,溶液中水电离出的的c(H+)与NaOH溶液的体积之间的关系如图所示,下列推断正确的是( )
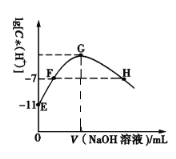
A. 可用pH试纸测定E点对应溶液,其pH=3
B. G点对应溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
C. H、 F点对应溶液中都存在:c(Na+)=c(Cl-)+c(ClO-)
D. 常温下加水稀释H点对应溶液,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是我们生活中必不可少的物质。将NaCl溶于水配成1 mol/L的溶液,溶解过程如图所示,下列说法正确的是
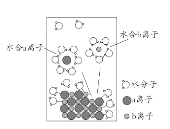
A.a离子为Na+
B.溶液中存在NaCl![]() Na++Cl-
Na++Cl-
C.溶液中含有NA个水合Na+和NA个水合Cl-
D.在水分子的作用下,NaCl溶解的同时发生了电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液态锂离子电池是指Li+嵌入化合物为正负极的二次电池。正极采用锂化合物LiCoO2,负极采用碳电极,充电后成为锂-碳层间化合物LixC6(0<x≤1),电解质为溶解有锂盐充电LiPF6、LiAsF6等的有机溶液。该电池的反应为:LiCoO2+6C![]() Li1-xCoO2+LixC6,下列有关说法不正确的是
Li1-xCoO2+LixC6,下列有关说法不正确的是
A.LiCoO2改写成为氧化物的形式为Li2O·Co2O3
B.该电池的电解质溶液使用有机溶剂主要是由于有机溶剂有良好的导电性
C.该电池放电时正极反应式:Li1-xCoO2+xe-+xLi+=LiCoO2
D.充电时,Li+从LiCoO2中脱嵌通过电解质溶液嵌入碳层
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com