
【题目】T K时,向2.0 L恒容密闭容器中充入1.0 mol COCl2,反应COCl2(g)![]() Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(Cl2) / mol | 0 | 0.16 | 0.19 | 0. 20 | 0.20 |
下列说法正确的是( )
A. 反应在前2 s 的平均速率v(CO)=0.080mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(Cl2) =0.11mol·L-1,则反应的ΔH<0
C. T K时起始向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,达到平衡前v正>v逆
D. T K时起始向容器中充入1.0 mol Cl2和0.9 mol CO,达到平衡时,Cl2的转化率为80%
【答案】C
【解析】
A、反应在前2s的平均速率![]() ,错误;B、平衡时
,错误;B、平衡时![]() , 升高温度,
, 升高温度,![]() ,说明平衡向正反应方向移动,则正反应应为吸热反应ΔH>0,错误;C、
,说明平衡向正反应方向移动,则正反应应为吸热反应ΔH>0,错误;C、
COCl2(g)![]() Cl2(g)+CO(g)
Cl2(g)+CO(g)
起始(mol·L-1):0.5 0 0
转化(mol·L-1):0.1 0.1 0.1
平衡(mol·L-1):0.4 0.1 0.1
该温度下![]() ,若起始向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,此时
,若起始向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,此时![]() <0.025,则反应达到平衡前正>v逆。正确;D、T K时起始向容器中充入1.0mol Cl2和1.0mol CO ,应等效于向2.0L恒容密闭容器中充入1.0mol COCl2,达到平衡时Cl2的转化率等于80%,如加入1.0mol Cl2和0.9mol CO,相当于在原来的基础上减小0.1mol CO,平衡在原来的基础上向正反应方向移动,则Cl2的转化率小于80%,错误;故选C。
<0.025,则反应达到平衡前正>v逆。正确;D、T K时起始向容器中充入1.0mol Cl2和1.0mol CO ,应等效于向2.0L恒容密闭容器中充入1.0mol COCl2,达到平衡时Cl2的转化率等于80%,如加入1.0mol Cl2和0.9mol CO,相当于在原来的基础上减小0.1mol CO,平衡在原来的基础上向正反应方向移动,则Cl2的转化率小于80%,错误;故选C。


科目:高中化学 来源: 题型:
【题目】按照如图所示接通线路,反应一段时间后,根据现象回答下列问题(假设所提供的电能可以保证反应顺利进行). 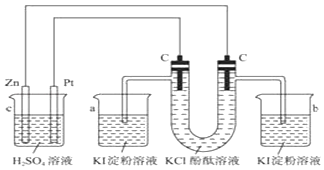
(1)标出电极名称:Zn;C(连Zn) .
(2)U型管中观察到的现象是 , 写出有关的反应方程式: .
(3)如果小烧杯中有0.508g碘析出,则烧杯中负极减轻 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
A.图①表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的p随加入酸体积的变化
B.图②中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 molL﹣1 KMnO4酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下。向20.00mL0.1mol/LHA溶液中滴入0.1mol/LNaOH溶液,溶液中由水电离出的氢离子浓度的负对数[-lgc水(H+)]与所加NaOH溶液体积的关系如图所示,下列说法不正确的是

A. 常温下,Ka(HA)约为10-5
B. M、P两点溶液对应的pH=7
C. b=20.00
D. M点后溶液中均存在c(Na+)>c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修5:有机化学基础]2017年治疗膀胱癌的有机小分子药物Aminolevulinic acid被批准使用,其合成路线如下:

已知:
请回答:
(1)A的名称为________,G中含氧官能团的名称为____________________________。
(2)⑤的反应类型为____________________,H的分子式为_____________________________。(3)①的化学方程式为__________________________________________。
(4)④的化学方程式为______________________________________________。
(5)D的同分异构体中,同时满足下列条件的共有____种(不含立体异构);
a.能与Na反应产生气体
b.既能发生银镜反应,又能发生水解反应
其中核磁共振氧谐有4组峰的物质的结构简式为________________(任写一种)。
(6)参照上述合成路线,设计由2-甲基丙酸和甲醇为起始原料制备2-甲基丙烯酸甲酯的合成路线(无机试剂任选)______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是 ( )
A | B | C | D | |
反应 装置或 图像 |
|
|
|
|
实验现 象或图 像信息 | 温度计的 水银柱不 断上升 | 反应物总能 量大于生成 物总能量 | 反应开始后, 甲处液面低 于乙处液面 | 反应开始 后,针筒活 塞向右移动 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)地下钢管连接镁块是金属防腐措施中的________________________法。
(2)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为_______________________;铅的最高价氧化物对应水化物的酸性比碳酸的_______(填“强”或“弱”)。
②PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________________。
③铅蓄电池放电时的正极反应式为__________________________________________ ,当电路中有2mol电子转移时,理论上两电极质量变化的差为_______ g。
(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图,石墨Ⅰ为电池的________极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为__________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的沸点,按由低到高顺序排列的是 ( )
A. NH3、CH4、NaCl、Na
B. H2O、H2S、MgSO4、SO2
C. CH4、H2O、NaCl、SiO2
D. Li、Na、K、Rb、Cs
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )

A. 铜电极上发生还原反应
B. 电池工作一段时间后,c(SO42-)向锌电极移动,甲池的c(SO42-)增大
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 电流的方向:由铜电极经过导线流向锌电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com