
����Ŀ������������������Ҫ��Fe2O3��SiO2���Ʊ��̷���FeSO4��7H2O������ͨ���̷��Ʊ�����[FeO(OH)]���������£�����֪FeS2��������������ˮ��
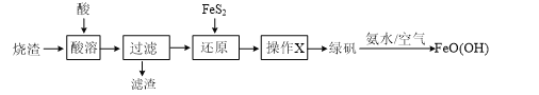
��1���������������У���ò���___________________�����������������������������������ܽ�������
��2��д������ԭ�����跢����Ӧ�����ӷ���ʽ��___________________��
��3���ԡ���ԭ�������Һ����������X�����ɵõ��̷���������X����ָ___________________�����ˣ�ϴ�ӣ����
��4���벹���������顰��ԭ����������Һ���Ƿ���Fe3+��ʵ�鷽����ȡ����ԭ������Һ���Թ��ڣ�___________________��
��5�����һ���Ʊ������ķ�Ӧ�У�������һ�ֿ������ʵ����ʣ����Ļ�ѧʽΪ___________________��
���𰸡� ���� 14Fe3����FeS2��8H2O=15Fe2����2SO![]() ��16H�� ����Ũ�������½ᾧ ����KSCN��Һ�������ֺ�ɫ����˵����Һ�к���Fe3�����������ֺ�ɫ����˵����Һ�в�����Fe3�� (NH4)2SO4
��16H�� ����Ũ�������½ᾧ ����KSCN��Һ�������ֺ�ɫ����˵����Һ�к���Fe3�����������ֺ�ɫ����˵����Һ�в�����Fe3�� (NH4)2SO4
����������1�����̷����������Ϊ��������ӣ����������������У���ò����������ܽ�������
��2������֪������������Ҫ��Fe2O3��SiO2����������������������ҺΪ��������Һ���������ԭ�����跢��FeS2��ԭFe3+�ķ�Ӧ���������������ԭ������X�õ��̷��ɵã�-1��S��������+6�۴�����SO42-�У�������ԭ�����跢����Ӧ�����ӷ���ʽΪ��14Fe3+��FeS2��8H2O=15Fe2+��2SO42-��16H+��
��3������ԭ����õ�����������Һ���ɾ�������Ũ�������½ᾧ�����̷�������������X����ָ������Ũ�������½ᾧ�����ˣ�ϴ�ӣ����
��4��������Fe3+��SCN-����Ϸ�Ӧ��������ԭ����������Һ���Ƿ���Fe3+������ʵ�鷽��Ϊ��ȡ����ԭ������Һ���Թ��ڣ�����KSCN��Һ������Һ���ֺ�ɫ����˵����Һ�к���Fe3+���������ֺ�ɫ����˵����Һ�в�����Fe3+��
��5�������У��̷��백ˮ������������������[FeO(OH)]��+2��Fe��������+3�ۣ����ݵ����غ㼰ԭ���غ�ɵã�4FeSO4+8NH3+6H2O+O2=4FeO(OH)+4(NH4)2SO4�����Ի�����һ�ֿ������ʵ�����Ϊ��(NH4)2SO4��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ӧ���ڼӳɷ�Ӧ���ǣ� ��
A.CH3CH3+Cl2 ![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
B.CH2�TCH2+HBr��CH3CH2Br
C.2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.CH3COOH+CH3CH2OH ![]() H3COOCH2CH3+H2O
H3COOCH2CH3+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����nAΪ�����ӵ���������ֵ������˵����ȷ����
A�������£�78g�ı�����3nA��![]() ˫��
˫��
B��1L 0��1 mol��L-1��NH4Cl��Һ����0��1nA��NH4+
C����״���£�22��4 L SO2��CO2����ﺬ��2nA��Oԭ��
D�������£�5��6 g����Ͷ������Ũ������ʧȥ0��3nA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. ��Ͷ��ˮ����Na��2H2O=Na+��2OH����H2��
B. �ô����ȥˮƿ�е�CaCO3��CO![]() +2H��=CO2����H2O
+2H��=CO2����H2O
C. Al����NaOH��Һ��2Al��2H2O +2OH��=2AlO![]() ��3H2��
��3H2��
D. Fe��ϡ���ᷴӦ��2Fe��6H��=2Fe3+��3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����ڹ�ũҵ�������ճ�������Ӧ�÷dz��㷺��
��1���ɻ�ͭ����ȡͭ�ķ�Ӧ����Ϊ��
2Cu2S��s��+3O2 ��g��=2Cu2O��s��+2SO2��g����H=��768.2kJmol��1 ��
2Cu2O��s��+Cu2S��s��=6Cu��s��+SO2��g����H=+116.0kJmol��1 ��
��д��Cu2S��O2��Ӧ����Cu��SO2���ȷ�Ӧ����ʽ�� ��
��2���Ȼ�ͭ��Һ��ͭ�����ֵķֲ�������ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ�������c��Cl���� �Ĺ�ϵ��ͼ1���ٵ�c��Cl����=9molL��1ʱ����Һ����Ҫ��3�ֺ�ͭ����Ũ�ȴ�С��ϵΪ �� 
����c��Cl����=1molL��1���Ȼ�ͭ��Һ�У�����AgNO3��Һ����ͭ���ּ�ת�������ӷ���ʽΪ����дһ������
��3�����Na2HPO3��Һ�ɵõ������ᣬװ����ͼ2
��˵������Ĥֻ����������ͨ������Ĥֻ����������ͨ����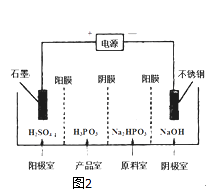
�������ĵ缫��ӦʽΪ�� ��
�ڲ�Ʒ���з�Ӧ�����ӷ���ʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���֮��Ϊ2��5��п��ϡ����ǡ����ȫ��Ӧ�������ᱻ��ԭ�IJ���ΪN2O����÷�Ӧ�б���ԭ��������δ����ԭ����������ʵ���֮����
A. 1��4 B. 1��5 C. 2��3 D. 2��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Ti)�Ļ�еǿ�ȸߣ�����ʴ����ǿ���С�δ��������֮�ơ���TiO2�ƽ����ѣ���Ҫ��Ӧ�У�
��TiO2��2C��2Cl2 ![]() TiCl4��2CO�� ��TiCl4��2Mg
TiCl4��2CO�� ��TiCl4��2Mg![]() 2MgCl2��Ti
2MgCl2��Ti
������������ȷ����
A. ��Ӧ����TiO2�������� B. ��Ӧ�ڱ����˽���þ��ԭ�ԱȽ�����ǿ
C. ��Ӧ����̼�ǻ�ԭ�� D. ��Ӧ�����������뻹ԭ�����ʵ���֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ����ȷ����
A. ��Fe(NO3)2ϡ��Һ�м������3Fe2����4H����NO![]() ===3Fe3����NO����2H2O
===3Fe3����NO����2H2O
B. ͭƬ��ŨHNO3��Cu��2NO![]() ��4H��===Cu2����NO2����2H2O
��4H��===Cu2����NO2����2H2O
C. �Ȼ��Ũ��Һ��ŨNaOH��Һ��Ϻ���ȣ�NH![]() ��OH��
��OH��![]() NH3����H2O
NH3����H2O
D. ̼�������Һ��������NaOH��Һ��Ϻ���ȣ�NH![]() ��OH��
��OH��![]() NH3����H2O
NH3����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ����ʹ�ϳɰ���Ӧ�������������( )
A.�����¶�
B.�����¶�
C.ʹ�ô���
D.��ʱ�����NH3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com