
【题目】有关物质结构、性质的说法中正确的是( )
①苯的密度比水的密度小
②C2H6、C4H10、C6H14在常温下均为气体
③1mol苯最多与3molH2发生加成反应,是因为苯分子含有3个碳碳双键
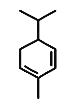
④水芹烯(桂皮中的一种成分)键线式如图,其分子式为C10H16
⑤CH2=CH2与CH2=CH-CH=CH2互为同系物
⑥甲烷与氯气在光照的条件下可以制取纯净的一氯甲烷
⑦所有卤代烃都能发生水解反应
A.①②⑤B.①④⑦C.③⑤⑥D.③④⑦
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是一种重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
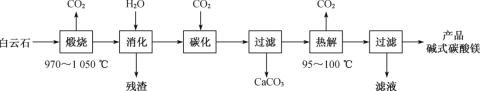
(1)“煅烧”时发生主要反应的化学方程式为___。
(2)常温常压下,“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
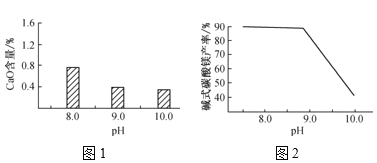
①应控制“碳化”终点pH约为___,钙元素的主要存在形式是___(填化学式)。
②根据图2,当pH=10.0时,镁元素的主要存在形式是___(填化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为___。
(4)该工艺为达到清洁生产,可以循环利用的物质是___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙炔与苯蒸气完全燃烧的热化学方程式如下所示:
①2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)+2600kJ
②2C6H6(g)+15O2(g)→12CO2(g)+6H2O(l)+6590kJ
下列说法正确的是
A.2mol C2H2(g) 完全燃烧生成气态水时放热大于2600kJ
B.2mol C6H6(l) 完全燃烧生成液态水时放热大于6590kJ
C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多
D.C2H2(g) 三聚生成C6H6(g) 的过程属于放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是 ( )
A. 浓硫酸稀释时溶液温度升高,说明浓硫酸稀释时只有水合过程
B. 蔗糖是非电解质,放入水中溶液温度没有明显变化,说明蔗糖溶于水既没有扩散过程又没有水合过程
C. 家用石碱(![]() )久置后,由块状变成粉末状,这一变化是风化的结果
)久置后,由块状变成粉末状,这一变化是风化的结果
D. 从冰箱中取出物品,表面很快出现水珠,这种现象叫潮解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2↑+ 7H2O ,若有0.1mol K2Cr2O7参加反应,下列说法正确的是( )
A.被氧化的HCl为51.1molB.转移电子1.806×1023个
C.氧化产物为7.3gD.还原剂占参加反应HCl的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国女药学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔医学奖,有关青蒿素的结构如图所示,下列关于靑蒿素的推断,不合理的是( )
A. 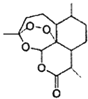 青蒿素的分子式是
青蒿素的分子式是![]()
B. 青蒿素所有碳原子均在同一平面上
C. 青蒿素在碱性条件下不能稳定存在
D. 青蒿素可以发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物对环境具有显著影响。
(1)已知汽车气缸中氮及其化合物发生如下反应:
N2(g)+O2(g)![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
N2(g)+2O2(g)![]() 2NO2(g) △H=+68 kJ/mol
2NO2(g) △H=+68 kJ/mol
则 2NO(g)+O2(g)![]() 2NO2(g) △H=__________ kJ/mol
2NO2(g) △H=__________ kJ/mol
(2)对于反应2NO(g)+O2(g)![]() 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:
第一步:2NO(g)![]() N2O2(g)(快速平衡)
N2O2(g)(快速平衡)
第二步:N2O2(g)+O2(g)![]() 2NO(g)(慢反应)
2NO(g)(慢反应)
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:υ正=k1 正·c2(NO),υ 逆=k1 逆·c(N2O2),k1正、k1 逆为速率常数,仅受温度影响。下列叙述正确的是__________
A. 整个反应的速率由第一步反应速率决定
B. 同一温度下,平衡时第一步反应的![]() 越大,反应正向程度越大
越大,反应正向程度越大
C. 第二步反应速率慢,因而平衡转化率也低
D. 第二步反应的活化能比第一步反应的活化能高
(3)在密闭容器中充入一定量的CO和NO气体,发生反应2CO(g)+2NO(g)![]() 2CO2(g)+N2(g) △H<0,图为平衡时NO的体积分数与温度、压强的关系:
2CO2(g)+N2(g) △H<0,图为平衡时NO的体积分数与温度、压强的关系:
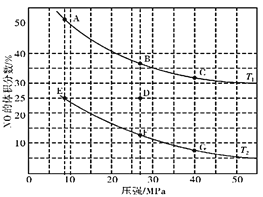
①温度:T1__________T2(填“>”、“<”或“=”)。
②若在D点对反应容器升温,同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的__________点(填字母)。
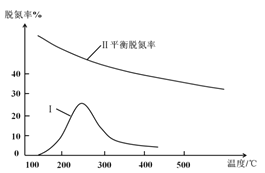
③某研究小组探究该反应中催化剂对脱氮率(即NO转化率)的影响。将相同量的NO和CO 以一定的流速分别通过催化剂a和b,相同时间内测定尾气,a结果如图中曲线I所示。已知:催化效率 b>a;b的活性温度约450℃。在图中画出b所对应的曲线(从300℃开始画) _______。
(4)在汽车的排气管上加装催化转化装置可减少NOx的排放。研究表明,NOx的脱除率除与还原剂、催化剂相关外,还取决于催化剂表面氧缺位的密集程度。以La0.8A0.2BCoO3+X(A、B 均为过渡元素)为催化剂,用H2还原NO的机理如下:
第一阶段:B4+(不稳定)+H2→低价态的金属离子(还原前后催化剂中金属原子的个数不变)
第二阶段:I . NO(g)+□→NO(a)
II . 2NO(a)→2N(a)+O2(g) III. 2N(a)→N2(g)+2□
IV. 2NO(a)→N2(g)+2O(a) V. 2O(a)→O2(g)+2□
注:□表示催化剂表面的氧缺位,g表示气态,a表示吸附态
第一阶段用氢气还原 B4+得到低价态的金属离子越多,第二阶段反应的速率越快,原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A.加入合金的质量可能为6.4g
B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为150mL
D.溶解合金时收集到NO气体的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往20ml1mol/L的AlCl3溶液中滴加0.2mol/L的NaOH溶液,最后有1.17克沉淀生成,则加入NaOH溶液的体积是
A.125mLB.275mLC.325mLD.450mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com