
 2,3,4-三甲基-3-乙基己烷
2,3,4-三甲基-3-乙基己烷 4-甲基-2-戊烯
4-甲基-2-戊烯 乙苯
乙苯


 .
. 分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长:选最长碳链为主链;
②多:遇等长碳链时,支链最多为主链;
③近:离支链最近一端编号;
④小:支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简:两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:(1)该有机物为烷烃,最长碳链含有5个C,质量为戊烷,编号从左边开始,在2、3号C各含有两个甲基,该有机物命名为:2,2,3,3-四甲基戊烷,
故答案为:2,2,3,3-四甲基戊烷;
(2)该有机物为烷烃,最长碳链含有6个C,质量为己烷,编号从左边开始,在2、3、4号C各含有一个甲基,3号碳上含有一个乙基,所以该有机物命名为:2,3,4-三甲基-3-乙基己烷,
故答案为:2,3,4-三甲基-3-乙基己烷;
(3)该有机物为烯烃,含有碳碳双键的最长碳链含有5个C,主链为戊烯,编号从距离碳碳双键最近的一端开始,碳碳双键在2号C,在4号C上含有1个甲基,该有机物命名为:4-甲基-2-戊烯,
故答案为:4-甲基-2-戊烯;
(4)该有机物为芳香烃烃,含有1个苯环和1个乙基,所以该有机物命名为:乙苯,
故答案为:乙苯;
(5)2,5-二甲基-2-庚烯,该有机物主链为庚烯,碳碳双键在2号C,在2、5号C上各含有1个甲基,其结构简式为 ,
,
故答案为: ;
;
(6)2,3-二甲基-1,3-丁二烯,该有机物主链为丁二烯,碳碳双键分别在1、3号C,在2、3号C上各含有1个甲基,其结构简式为 ,
,
故答案为: ;
;
(7)邻羟基苯甲酸,该有机物主链为苯甲酸,在羧基的邻位含有1个羟基,其结构简式为 ,
,
故答案为: ;
;
(8)苯乙烯可以是苯环上的一个氢原子被乙烯基代替,2,4,6-三甲基苯乙烯,以乙烯基为1号碳,2,4,6号C上各含有1个甲基,其结构简式为 ,
,
故答案为: .
.
点评 本题考查了有机物的命名,题目难度中等,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
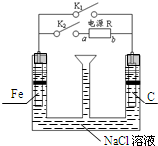
| A. | 若只关闭K1,则Fe发生析氢腐蚀 | |
| B. | 先只关闭K1,漏斗内液面下降,且有红褐色沉淀产生;再打开K1,仅关闭K2,则液面上升 | |
| C. | 若只关闭K2,只有一个电极产生气体,则a为电源负极 | |
| D. | 只关闭K1时,发生的总反应方程式为:2Fe+O2+2H2O═2Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果某化合物只含共价键,则其一定是共价化合物 | |
| B. | 焓变小于0而熵变大于0的反应肯定是自发反应 | |
| C. | 对于给定条件下反应物之间同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 绿色化学的核心是利用化学原理对产生的环境污染进行治理 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如图所示。
则下列说法正确
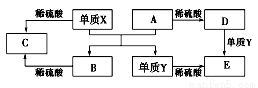
A.单质X与A反应的化学方程式:Al2O3+2Fe Fe2O3+2Al
Fe2O3+2Al
B.检验D溶液中金属阳离子的反应:Fe3++3SCN-=Fe(SCN)3↓
C.单质Y在一定条件下能与水发生置换反应
D.由于化合物B和C均既能与酸反应.又能与碱反应,所以两者均是两性化合物
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋中含有3%~5%的乙酸 | |
| B. | 黄酒变酸是因为部分乙醇氧化为乙酸 | |
| C. | 与甲酸甲酯互为同分异构体 | |
| D. | 通过乙酸乙酯的碱性水解直接获取 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
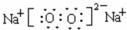 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | HX | HY | H2CO3 |
| 电离平衡常数 | 7.8×10-9 | 3.7×10-15 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | HX、HY两种弱酸的酸性:HX<HY | |
| B. | 相同条件下溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 | |
| C. | 结合H+的能力:CO32->Y->X->HCO3- | |
| D. | HX与Na2CO3反应,无气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该烃X与等质量的甲烷相比,X燃烧时消耗的氧气更多 | |
| B. | 分子中碳原子的化学环境有2种 | |
| C. | 分子中的氢原子分布在两个互相垂直的直线上 | |
| D. | 分子中既有C-C键也有C=C键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com