
����Ŀ�����ǿ�����ڡ�2018�����Ժ�����������桷��ǿ����������������������ŷ���Ҫ�½�3%�����о�����������(��NOx)������(��SO2)���Ż����Ļ������塣
��.���������ϰ�װ����ת���������䷴Ӧ���Ȼ�ѧ����ʽΪ��2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ��H=-746.50kJ��mol-1��T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У����¶Ⱥ�������䣬��Ӧ������(0~15min) NO�����ʵ�����ʱ��仯��ͼ��
2CO2(g)+N2(g) ��H=-746.50kJ��mol-1��T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У����¶Ⱥ�������䣬��Ӧ������(0~15min) NO�����ʵ�����ʱ��仯��ͼ��

��1��ͼ��a��b�ֱ��ʾ����ͬ�¶��£�ʹ��������ͬ���������ͬ�Ĵ���ʱ���ﵽƽ�������n (NO)�ı仯���ߣ����б�ʾ����������ϴ��������_______������a������b����
��2����a������ʾ��Ӧ�У�0~10min�ڣ�CO��ƽ����Ӧ����v(CO)=_________��T��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=__________��ƽ��ʱ�������¶Ȳ��䣬���������г���CO��CO2��0.2 mol����ƽ�⽫�ƶ�_____________(����������������������������)
��3��15minʱ, n (NO)����ͼ����ʾ�仯����ı������������_______������ţ�
A .��������COB .��N2Һ���Ƴ���ϵC .�����¶�D .�������
��4����. ��֪�����з�Ӧ��
��5O2(g)+ 4NH3(g)![]() 6H2O(g)+ 4NO(g) ��H1
6H2O(g)+ 4NO(g) ��H1
��N2(g)+O2(g)![]() 2NO(g) ��H2
2NO(g) ��H2
��2NO(g)+ O2(g)![]() 2NO2(g) ��H3
2NO2(g) ��H3
���ڸ�Ч���������¿ɷ���8NH3(g)+ 6NO2(g)![]() 7N2(g)+ 12H2O(g)�ķ�Ӧ����NO2���д�����÷�Ӧ�ġ�H=_________���á�H1����H2����H3��ʾ������S__________0��
7N2(g)+ 12H2O(g)�ķ�Ӧ����NO2���д�����÷�Ӧ�ġ�H=_________���á�H1����H2����H3��ʾ������S__________0��
��5��ij�¶��£���ij�����ܱ������г���һ������NH3��NO2�� ���գ�4����ԭ��ģ����Ⱦ��Ĵ������������й۲쵽________________������ţ������жϸ÷�Ӧ�ﵽƽ��״̬
A .���������ɫ���ٸı�
B .���������ܶȲ��ٸı�
C .�������Ħ���������ٸı�
D .NH3��NO2�����ʵ���֮�Ȳ��ٸı�
���𰸡�b 0.01mol/(L��min) 5 �� AB 2��H1 -7��H2 -3��H3 > AC
��������
(1)����������ϴ�Ӧ���ʿ죬�ﵽƽ������ʱ��̣�
(2)��ʼʱ��NOΪ4mol��ƽ��ʱNOΪ0.2mol�����ݷ���ʽ���ƽ��ʱCO��CO2��N2��Ũ�ȣ���Ӧ����v=![]() ������ƽ�ⳣ������ʽ���㣻����Qc��k����Դ�С������
������ƽ�ⳣ������ʽ���㣻����Qc��k����Դ�С������
(3)��ͼ���֪��NO��Ũ�ȼ�С��ƽ�����������ƶ���
(4)������ʽ2��-7��-3�۵�8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O���ʱ������Ӧ�ĸı䣻��������ʵ���������������
7N2(g)+12H2O���ʱ������Ӧ�ĸı䣻��������ʵ���������������
(5)�����淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ������䡢���ʵ���Ũ�Ȳ��䡢�ٷֺ����Լ��ɴ������һϵ������������.
(1)����������ϴ�Ӧ���ʿ죬�ﵽƽ������ʱ��̣���ͼ��֪��b���ߴ����������·�Ӧ���ʿ죬����b�Ĵ����ı������
(2)��ʼʱ��NOΪ0.4mol��ƽ��ʱNOΪ0.2mol��
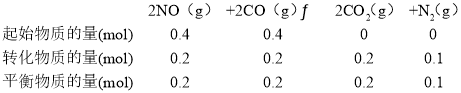
��ƽ��ʱ��Ũ�ȣ�c(NO)=0.1mol/L��c(CO)=0.1mol/L��c(CO2)=0.1mol/L��c(N2)=0.05mol/L��һ����̼��ʾ�ķ�Ӧ����v= =0.01mo/(Lmin)��k=
=0.01mo/(Lmin)��k=![]() =5(mol/L)-1��
=5(mol/L)-1��
ƽ��ʱ�������¶Ȳ��䣬���������г���CO��CO2��0.2mol����c(CO)=0.2mol/L��c(CO2)=0.2mol/L��Qc=![]() =5=k����ƽ�ⲻ�ƶ���
=5=k����ƽ�ⲻ�ƶ���
(3)��ͼ���֪��NO��Ũ�ȼ�С��ƽ�����������ƶ���2NO(g)+2CO(g)![]() 2CO2(g)+N2 ��
2CO2(g)+N2 ��
A����������CO һ��������С��ƽ��������У���A��ȷ��
B����N2Һ���Ƴ���ϵƽ��������У���B��ȷ��
C����ӦΪ���ȷ�Ӧ�������¶�ƽ��������У�һ����������C����
D����������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬һ�������������䣬��D����
�ʴ�ΪAB��
(4)������ʽ2��-7��-3�۵�8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O����H=2��H1-7��H2-3��H3����������ʵ���������������������S��0��
7N2(g)+12H2O����H=2��H1-7��H2-3��H3����������ʵ���������������������S��0��
(5)A����Ӧ��ֻ�ж���������ɫ�������������ɫ���ٸı�ʱ��˵����������Ũ�Ȳ��䣬�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����A��ȷ��
B����Ӧǰ�����������������䡢����������䣬���ܶ�ʼ�ղ��䣬���ܹؼ����������ܶ��ж�ƽ��״̬����B����
C����Ӧ�����������ʵ����������Է�Ӧǰ��������ƽ��Ħ��������С�����������Ħ���������ٸı䣬���淴Ӧ������ȣ��ﵽƽ��״̬����C��ȷ��
D��NH3��NO2�����ʵ���֮�Ȳ��ٸı�ʱ����Ӧ��һ���ﵽƽ��״̬���뷴Ӧ���ʼ���ʵ����йأ����Բ����ж�ƽ��״̬����D����
�ʴ�ΪAC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ����100mL0.1mol/LNH4HSO4��Һ����εμ�0.1mol/LNaOH��Һ���õ���ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��������Һ������мӺ��ԣ������з�����ȷ����
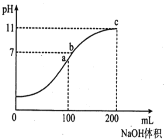
A.ab�κ�bc�η��������ӷ�Ӧһ����ͬ
B.ˮ�ĵ���̶�������c��
C.b����Һ�и�����Ũ���ɴ�С������˳����:C(Na+)>C(NH4+)>C(SO42-)>C(H+)=C(OH-)
D.NH4+��ˮ��ƽ�ⳣ��Kh��������Ϊ10��10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��IJ�����ԭ����������ȷ����![]()
A.��ȡ![]() ʱ����10g������������̣����������Ƶ�
ʱ����10g������������̣����������Ƶ�![]() ��λ��
���
B.������ˮ��Ӧ��ʵ��ʱ����ȡ�̶���С�Ľ����ƣ�����ֽ����������ú�ͣ������ձ��У��������η�̪��Һ���ټ�������ˮ��Ȼ��۲첢��¼ʵ������
C.���Թ��м���5mL��ˮ��2mL����![]() ���ۣ�������ã��۲��Թܵײ����ɺ�ɫ��״Һ��
���ۣ�������ã��۲��Թܵײ����ɺ�ɫ��״Һ��
D.Ϊ��֤���ŵ����ã��������ձ��зֱ�ʢ���������������Һ��ϡ���Ը��������Һ���������ʯī���õ����������������Ȼ����װ��![]() ������Һ����֬��U�����˲��������ձ��У�������ƫת��һ��ʱ�����������Һ��ɫ
������Һ����֬��U�����˲��������ձ��У�������ƫת��һ��ʱ�����������Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15.2 g ͭ��þ��ɵĻ�������250 mL4.0 mol L-1��ϡ�����У�������ȫ�ܽ⣬���ɵ�����ֻ��NO����������Һ�м���1.0 L NaOH��Һ����ʱ��������ǡ�ó�����ȫ����������Ϊ25.4 g������˵������ȷ����
A. ԭ���������У�Cu��Mg�����ʵ���֮��Ϊ2��1
B. ����������Һ��Ũ��Ϊ0.8 mol��L-1
C. �����ܽ�����Һ����������ʵ���Ϊ0.1mol
D. ���ɵ�NO�����ڱ���µ����Ϊ4.48L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ѧϰԪ�ػ�����֪ʶ�Ĺ����У����ֺ�����ͬԪ�ص����ʼ���һ�������´���
ת�����ɣ����Ƴ�����ת����ϵͼ��ͼ��A��B��C��D���ɶ�����Ԫ����ɵ����ʡ�

��ش�
��1����AΪ���ʣ�����ɫ��ӦΪ��ɫ��CΪ����ɫ���塣�����A��Ԫ�������ڱ��е�λ����__��C�ĵ���ʽΪ__��
��2����AΪ��ʹʪ���ɫʯ����ֽ���������壬CΪ����ɫ���塣
��A��B��Ӧ�Ļ�ѧ����ʽ��__��������A��ˮ��Һ��AlCl3��Һ��Ӧ���ӷ���ʽΪ__��
��A��C��Ӧ����E��ˮ��E�ǿ����к����������塣������19.6gEʱ��ת�Ƶ��ӵ����ʵ���Ϊ__mol��
��3����BΪ��ʹƷ����Һ��ɫ����ɫ�̼��Ե����壬B��C��Ӧ�Ļ�ѧ����ʽ��__��B��KMnO4��Һ��Ӧ���ӷ���ʽΪ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺϴ�����ҵ���������������ڱ�����������Լ��Դ����Ӧ 2NO��g��+2CO��g��2CO2��g��+N2��g�����ɼ�������β������Ⱦ����ŷţ��� 2L �ܱ������з����÷�Ӧʱ��n��CO2�����¶� T ��ʱ�� t �ı仯������ͼ��ʾ��

��1���÷�Ӧ��ƽ�ⳣ������ʽΪK=______���������¶ȣ�ƽ�ⳣ�� K ֵ______����������������С����������������˵������______��
��2���� T2�¶��£� 0��2s �ڵ�ƽ����Ӧ���� v��N2��=______��
��3����ҵ��ˮ�Ĵ��������кܶ࣬ʹ�� Fe2��SO4��3 ������ˮ�����Է�ˮ�е���������ѳ�����ȥ��������ӷ���ʽ��ƽ���ƶ�ԭ������ԭ��______���ɷ��Ʊ����ˮ�������������ƣ�Na2FeO4���ķ�Ӧԭ��Ϊ��2FeSO4+6Na2O2��2Na2FeO4+Na2O+2Na2SO4+O2�����÷�Ӧ��������Ϊ______��
��4�����ð�������������������ĸ���Ʒ______���û�ѧ����ʽ��ʾ��������Ʒ��ԭ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����ֵ������˵����ȷ����
A.12g![]() ��ԭ�Ӻ���������Ϊ6NA
��ԭ�Ӻ���������Ϊ6NA
B.9.0g�����Ǻ����ǵĻ�����к�̼ԭ�ӵ���ĿΪ0.3NA
C.25��ʱ��1LpH=2��H2C2O4��Һ�к�H+����ĿΪ0.02NA
D.��״���£�2.24LCO2������Na2O2��Ӧת�Ƶĵ�����Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������������һ����̼�������з�Ӧ��Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
��1���÷�Ӧ��ƽ�ⳣ������ʽΪK=________��
��2�����¶��£���2 Lʢ��Fe2O3��ĩ���ܱ�������ͨ��CO���壬10 min�������˵�����11.2 g����10 min��CO��ƽ����Ӧ����Ϊ________��
��3���÷�Ӧ�ﵽƽ�����Fe�ۣ�ƽ��________�ƶ������ֺ��º���ͨ��CO��ƽ����________�ƶ���������������ҡ�������
��4�������÷�Ӧ�Ѵ�ƽ��״̬����______________
A.��λʱ��������nmolCOͬʱ����nmolCO2 B.����ʱ��������ѹǿ����
C.������������������ D.CO2������������� E.Fe��Ũ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�������Ȼ�ѧ��Ӧ����ʽ��
(1)1molN2(g)������H2(g)��Ӧ����NH3(g)���ų�92.2kJ������______________��
(2)1molN2(g)������O2(g)��Ӧ����NO(g)������68kJ������_______________��
(3)1molCu(s)����һ������O2(g)��Ӧ����CuO(s)���ų�157kJ������__________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com