
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 mol/L NaHSO4溶液中,阳离子数目之和为0.2NA
B.标准状况下0.2 mol Cl2溶于水中,转移的电子数为0.2NA
C.常温常压下1.5 g NO与1.6 g O2充分反应后混合物中原子总数为0.2NA
D.标准状况下,4.48 L HF含有的分子总数为0.2NA
【答案】C
【解析】
A. 未给出体积,无法计算物质的量,A错误;
B. Cl2溶于水中,部分氯气与水反应生成次氯酸和氯化氢,转移的电子数小于0.2NA,B错误;
C. 1.5 g NO为0.05mol,1.6 g O2为0.05mol,充分反应,2NO+ O2= 2NO2,0.05mol NO全部反应生成0.05mol NO2,剩余O2为0.025mol,体系中还存在2NO2![]() N2O4,但化学反应原子守恒,所以0.05mol NO2中原子总数0.15 NA,为0.025mol O2中原子总数0.05 NA,反应后混合物中总共原子总数为0.2NA;C正确;
N2O4,但化学反应原子守恒,所以0.05mol NO2中原子总数0.15 NA,为0.025mol O2中原子总数0.05 NA,反应后混合物中总共原子总数为0.2NA;C正确;
D. 标准状况下,HF不是气体,无法计算,D错误;故答案为:C。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】锑(Sb)在自然界中一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe![]() Sb4O6+6FeS,
Sb4O6+6FeS,
②Sb4O6+6C![]() 4Sb+6CO↑。关于反应①、②的说法正确的是
4Sb+6CO↑。关于反应①、②的说法正确的是
A.反应①、②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3molFeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4 molSb时,反应①与反应②中还原剂的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分:
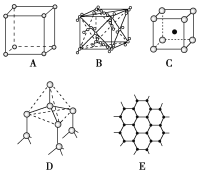
请回答下列问题:
(1)代表金刚石的是________(填编号字母,下同),其中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体。
(2)代表石墨的是________,每个正六边形占有的碳原子数平均为________个。
(3)代表NaCl的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。
(5)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
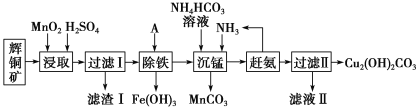
已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)滤渣I中的主要成分除了MnO2,S还有___________ (化学式),请写出“浸取”反应中生成S的化学方程式:_____。
(2)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为____,若加A后溶液的pH调为5,则溶液中Fe3+的浓度为____mol/L。
(3)写出“沉锰”(除Mn2+)过程中反应的离子方程式:_____。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是____(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,RSO4(s)+CO32-(aq)RCO3(s)+SO42-(aq)的平衡常数K=1.75×104,Ksp(RCO3)=2.80×10-9,下列叙述中正确的是
A.25℃ 时,RSO4的Ksp约为4.9×10-5
B.将浓度均为6×10-5mol/L的RCl2、Na2CO3溶液等体积混合后可得到RCO3沉淀
C.向c(CO32-)=c(SO42-)的混合液中滴加RCl2溶液,首先析出RSO4沉淀
D.相同温度下,RCO3在水中的Ksp大于在Na2CO3溶液中的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验方案的设计或评价合理的是( )
A. 经酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示具支试管中,一段时间后导管口有气泡冒出
经酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示具支试管中,一段时间后导管口有气泡冒出
B.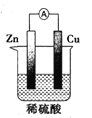 图中电流表会显示电流在较短时间内就会衰减
图中电流表会显示电流在较短时间内就会衰减
C.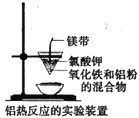 图中应先用燃着的小木条点燃镁带,然后插入混合物中引发反应
图中应先用燃着的小木条点燃镁带,然后插入混合物中引发反应
D.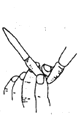 可用图显示的方法除去酸式滴定管尖嘴中的气泡
可用图显示的方法除去酸式滴定管尖嘴中的气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月,其电池反应为:2CH3OH+3O2+4OH﹣![]() 2CO32﹣+6H2O,则有关说法正确的是 ( )
2CO32﹣+6H2O,则有关说法正确的是 ( )
A.放电时CH3OH参与反应的电极为正极
B.放电时负极的电极反应为CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O
C.标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
D.放电一段时间后,通入氧气的电极附近溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向一个一定容积的密闭容器中放入3 mol X和2 mol Y,发生反应:X(g)+Y(g)![]() 2Z(g)+R(g),达平衡时X的转化率为φ1。维持温度不变,若把6 mol X和3 mol Y放入该容器中,达平衡时X的转化率为φ2,则φ1与φ2的关系是( )
2Z(g)+R(g),达平衡时X的转化率为φ1。维持温度不变,若把6 mol X和3 mol Y放入该容器中,达平衡时X的转化率为φ2,则φ1与φ2的关系是( )
A.φ1>φ2B.φ1<φ2C.φ1=φ2D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医学上在进行胃肠疾病的检查时,利用X射线对BaSO4穿透能力较差的特性,常用BaSO4做内服造影剂,这种检查手段称为钡餐透视。
Ⅰ.请写出BaSO4能作为钡餐透视的另外一个理由:__。
Ⅱ.请用文字叙述和离子方程式说明钡餐透视时为什么不用BaCO3?__。
Ⅲ.某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:①5mL水 ②20mL0.5mol·L-1的Na2SO4溶液 ③40mL0.2mol·L-1的Ba(OH)2溶液 ④40mL0.1mol·L-1的H2SO4溶液中,溶解至饱和。
(1)以上各溶液中,c(Ba2+)的大小顺序正确的是__,BaSO4的溶解度的大小顺序为__(填序号)。
A.③>①>④>② B.③>①>②>④
C.①>④>③>② D.①>③>④>②
(2)已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO42-)为__,溶液②中c(Ba2+)为__。
(3)某同学取同样的溶液③和溶液④直接混合,则混合溶液的pH为__(假设混合后溶液的体积为混合前两溶液的体积之和)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com