
【题目】2019年是深入实施“2025中国制造”年,而化学与人类的生产生活密切相关,下列有关说法错误的是![]()
![]()
A.3D打印中的石墨烯由离子构成,而金刚石由原子构成
B.“北斗组网卫星”所使用的碳纤维,是一种无机非金属材料
C.世界杯赞助商之一的蒙牛奶业,其生产的牛奶属于胶体,具有丁达尔效应
D.港珠澳大桥设计建造时采用了外接铝的牺牲阳极的阴极保护法
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在3种不同条件下,分别向容积为1L的恒容密闭容器中充入4molA和2molB,发生反应:2A(g)+B(g)![]() 2D(g) △H=QkJ/mol,相关条件和数据见表。下列说法正确的是( )
2D(g) △H=QkJ/mol,相关条件和数据见表。下列说法正确的是( )
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 3 | 3 | 2 |
化学平衡常数 | K1 | K2 | K3 |
A.实验Ⅲ达平衡后,恒温下再向容器中通入2 molA和2 molD,平衡正向移动
B.升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C.实验Ⅰ达平衡后容器内的压强是实验Ⅲ的0.9倍
D.K3<K2 =K1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 在容积为5L的密闭容器中,通入5 mol N2和8 mol H2,在一定条件下反应生成NH3,当反应进行到2 min时,测得容器内有4 mol NH3。则:
(1)2 min时,容器内n(N2)=________ ,c(H2)=___________。
(2)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为 _______。
Ⅱ.在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________。
(2)该反应为________(填“吸热”或“放热”)反应。
(3)能判断该反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。
(5)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,则下一时刻,反应将________(填“正向”或“逆向”)进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四个相同容积的密闭容器中分别充入一定量的CO、H2,发生反应:CO(g)+2H2(g)![]() CH3OH(g)。开始反应时,按正反应速率由大到小的顺序排列,正确的是
CH3OH(g)。开始反应时,按正反应速率由大到小的顺序排列,正确的是
①在500℃时,5 mol CO和10 mol H2反应
②在500℃时,加入催化剂,10 mol H2与5 mol CO反应
③在450℃时,6 mol H2和3 mol CO反应
④在500℃时,6 mol H2和3 mol CO反应
⑤在450℃时,4 mol H2和2 mol CO反应
A.②①③④⑤B.②①④③⑤C.⑤②①③④D.②④⑤③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素及其化合物叙述中不正确的是( )
A.氧化镁和氧化铝熔点均很高,常用作耐高温材料
B.在酒精灯加热条件下,![]() 和
和![]() 固体都能分解
固体都能分解
C.二氧化氯具有氧化性,可用于自来水杀菌消毒
D.电闪雷鸣的雨天,![]() 与
与![]() 会发生反应并最终转化为硝酸盐被植物吸收
会发生反应并最终转化为硝酸盐被植物吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,c(HCN)+c(CN-)=0.1 mol·L-1的一组HCN和NaCN的混合溶液,溶液中 c(HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是( )
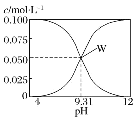
A.将 0.1 mol·L-1 的 HCN 溶液和 0.1 mol·L-1NaCN溶液等体积混合(忽略溶液体积变化):c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+)
B.W 点表示溶液中:c(Na+)=c(HCN)+c(CN-)
C.pH=8的溶液中:c(Na+)+c(H+)+c(HCN)=0.1 mol·L-1+c(OH-)
D.将0.3 mol·L-1 HCN溶液和0.2 mol·L-1NaOH溶液等体积混合(忽略溶液体积变化):c(CN-)+3c(OH-)=c(HCN)+3c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、能源、环境等密切相关。下列叙述正确的是![]()
![]()
A.油脂和蛋白质是人体必需的营养物质,都属于高分子化合物
B.食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用都是吸水,防止食品变质
C.电热水器用镁棒防止金属内胆腐蚀,原理是牺牲阳极的阴极保护法
D.屠呦呦用乙醚提取青蒿素的过程属于化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用 H2C2O4 溶液和酸性 KMnO4 溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
编号 | H2C2O4 溶液 | 酸性 KMnO4 溶液 | 温度℃ | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)已知反应后 H2C2O4 转化为CO2逸出,KMnO4溶液转化为MnSO4,每消耗1 mol H2C2O4转移__________mol 电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为 n(H2C2O4)∶n(KMnO4)≥______________。
(2)探究温度对化学反应速率影响的实验编号是____________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是____________。
(3)实验①测得 KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______________mol·L-1·min-1。
(4)已知50℃时c(MnO4-)~反应时间 t 的变化曲线如图。若保持其他条件不变,请在坐标图中,画出 25℃时c(MnO4-)~t的变化曲线示意图________。
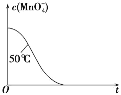
(5)高锰酸钾和草酸反应开始速率较慢,反应一会儿,速率突然加快,合理的原因是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g) ΔH<0,已知容器Ⅰ中反应在5 min时到达平衡。
COCl2(g) ΔH<0,已知容器Ⅰ中反应在5 min时到达平衡。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | a | 0.55 | 0 | 0.5 |
Ⅲ | T | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A.容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B.反应Ⅲ的温度T<500℃
C.容器Ⅱ中起始时CO的物质的量为1.0 mol
D.若起始时向容器Ⅰ加入CO 0.8 mol、Cl2 0.8 mol,达到平衡时CO转化率小于80%]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com