
����Ŀ��I.�о�������ʴ�ͷ�����ԭ��������ʵ���塣
(1)��ͼΪ�˽̰�̲���̽��������������ʴ��װ�á�ij��ȤС�鰴��װ��ʵ�飬������Һ�����������������д�ʩ���Ը���������۲쵽ˮ�������������______(�����)��
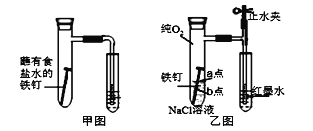
A.�ô����������Թ��ڿ��� B.�þƾ��Ƽ����Թ�����¶�
C.�������������ۺ�̿�ۻ�Ϸ�ĩ D.���ɸ�ϸ�ĵ��ܣ�ˮ�еμӺ�īˮ
(2)��С�齫��ͼװ�øĽ�����ͼװ�ò�����ʵ�飬�����к�īˮҺ���߶���ʱ��ı仯���±������������жϸ�ʴ��������ʱ����______(�����ӿ�����������������������)������ΪӰ������Ϊ_______��
ʱ��/min | 1 | 3 | 5 | 7 | 9 |
Һ���߶�/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
(3)Ϊ̽��������ʴʵ�� a��b �����������ķ�Ӧ����������ʵ�飬����ɱ���հף�
ʵ����� | ʵ������ | ʵ����� |
��NaCl��Һ�еμ�2~3�η�ָ̪ʾ�� | a�㸽����Һ���ֺ�ɫ | a��缫��ӦΪ_____ |
Ȼ���ٵμ�2~3�����軯����Һ | b����Χ������ɫ���� | b��缫��ӦΪ Fe -2e-=Fe2+ |
(4)�������װ���о������Ի����и�ʴ����Ҫ��ʽ���ⶨ��ƿ����ѹ�Ϳ��������������������ʱ��仯��ͼ����ͼ�пɷ�����t1~t2֮����Ҫ����_______��ʴ(������������)��ԭ��_______��
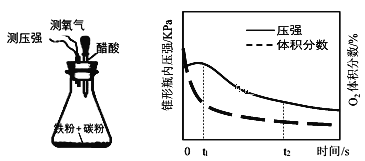
(5)���������ۻ���һ�ֵ绯ѧ������������Fe����������H2SO4��Һ�У�һ��������Fe�ۻ��γ�����Fe3O4����Ĥ����д���������缫��Ӧʽ______��
II.��֪���ᾧ��(H2C2O4��XH2O)������ˮ�����������Ը��������Һ��ȫ��Ӧ��2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O������������ԭ�ζ����ⶨ���ᾧ��Ľᾧˮ������X���������£�
���÷�����ƽ��ȡ���ᾧ��1.260g���������Ƴ�100.00mL���������Һ
������Һ����ȡ25.00mL���������Һ����ƿ�У����������������ữ
����Ũ��Ϊspan>0.1000mol/L��KMnO4 ����Һ���еζ������ν�����£�
��һ�εζ� | �ڶ��εζ� | �����εζ� | |
������Һ���(mL) | 25.00 | 25.00 | 25.00 |
����Һ���(mL) | 9.99 | 10.01 | 10.00 |
��֪H2C2O4����Է�������Ϊ90����ش��������⣺
(1)�ζ�ʱ��KMnO4����ҺӦ��װ��______(������ʽ��������ʽ��)�ζ����С�
(2)����ζ��յ�ı�־��________��
(3)�����������ݼ���X=_______��
(4)������(��ƫ�ߡ�ƫ�ͻ���Ӱ��)�����ζ���ʼʱ���ӵζ��̶ܿȣ��ζ�����ʱ���ӵζ��̶ܿȣ���Xֵ________��
���𰸡�ACD ���� ������Ũ�� O2+4e-+2H2O=4OH- ���� ����������ƿ��ѹǿ�����ͣ������Ҫ��������ʴ 3Fe-8e-+4H2O=Fe3O4+8H+ ��ʽ ���һ�α���Һ������ƿ�У���Һǡ������ɫ����Ϻ�ɫ����30���ڲ���ɫ 2 ƫ��
��������
I.(1)Ҫʹ������졢���������ɲ�ȡ����Ӧ���ʵȷ�����
(2)������ͼ��O2��Ũ�ȵı仯����ͬʱ����Һ���仯�߶ȷ�����
(3)O2�������ϻ�õ��ӣ���ΪOH-��ʹ��������Һ�Լ��ԣ�����Feʧȥ���ӱ�ΪFe2+��
(4)�������ⸯʴ����H2���壬ʹװ��������ѹǿ����������ʴ����������ʹװ���ڵ�����ѹǿ��С������
(5)���ʱ������Feʧȥ���ӣ���������������Fe3O4����Ĥ�������ۻ�����
II.(1)KMnO4����ǿ�������ԣ��ḯʴ��ʽ�ζ��ܵ��ܣ�
(2)KMnO4��Һ����ǿ�������ԣ�����ᷢ��������ԭ��Ӧ��������ɫMn2+������Ӧ��ȫ��������KMnO4��Һ������KMnO4��Һ��������ɫ��Ϊָʾ���жϵζ��յ㣻
(3)����������ԭ�ζ��������������ʵ������Ӷ�����X��ֵ��
(4)��c(��)= �����ݴ����������V(�ζ�)�ı仯������
�����ݴ����������V(�ζ�)�ı仯������
I.(1)�ô����������֧�Թ��ڵĿ�����������Ũ������Ӧ���ʼӿ죬A��ȷ��
B.�þƾ��Ƽ����Թ�����¶ȣ�������������¶����߶�������ͣ������ݳ��������ܿ�ð�����ݣ������жϷ�Ӧ������B����
C.�������������ۺ�̿�۵Ļ�������Ӧ��ĽӴ��������Ӧ���ʼӿ죬C��ȷ��
D.���ɸ�ϸ�ĵ��ܣ�ˮ�еμӺ�īˮ���ı���ͬ��ѹǿ���ı���ͬ�������ëϸ����������ĸ߶ȴ��ڲ������ܣ��Һ�īˮ��������ԣ�D��ȷ��
�ʺ���ѡ����ACD��
(2)��Ϊ��ͼ������װ����ʢ�е����������ʵ������䣬���ŷ�Ӧ�Ľ��У�������Ũ�����ͣ�ʹ��Ӧ���ʼ�С�������ͨ����ͬ��ʱ������Һ�������ĸ߶������õ�֤ʵ��
(3)���ݱ�������a�㸽����Һ���ֺ�ɫ��˵��a����ҺΪ���ԣ�a�㷢���ķ�ӦΪO2+4e-+2H2O=4OH-������a��Ϊ�������μ�2~3�����軯����Һ��b����Χ������ɫ��������������b�㷢����Ӧ��Fe -2e-=Fe2+��Fe2+�����軯����Һ����������Ӧ�������軯������ɫ������b��Ϊ������
(4)����ͼʾ��֪�����ŷ�Ӧ�Ľ��У�װ���ڵ�����������ƿ��ѹǿ�����ͣ�˵�������ĸ�ʴ��������ʴ��
(5)��Fe����������H2SO4��Һ�У�Feʧȥ���ӣ�������Fe3O4����Ĥ���������缫��ӦʽΪ��3Fe-8e-+4H2O=Fe3O4+8H+��
II.(1) KMnO4��Һ����ǿ�����ԣ����Ը�ʴ��Ƥ�ܣ�KMnO4��ҺӦװ����ʽ�ζ����У�
(2)���ᷴӦ��ϣ��ټ������һ��KMnO4��Һ����Һ��Ϊdz�Ϻ�ɫ����30s�ں�ɫ����ȥ��˵���ζ����յ㣻
(3)���εζ�����̫�����õζ�����������ø��������Һ�����Ϊ10.00mL��1.260g���ᾧ�����������Һ��������������ʵ���Ϊ��4��![]() ��0.1000mol/L��0.010L=0.010mol��X=
��0.1000mol/L��0.010L=0.010mol��X=![]() ��(
��(![]() )=2��
)=2��
(4)�ζ���ʼʱ���ӵζ��̶ܿȣ��ζ�����ʱ���ӵζ��̶ܿȣ������ı�Һ�����С����������ʵ�����С��������С����ᾧˮ����ƫ�࣬Xֵƫ�ߡ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ���������ֵ������˵����ȷ���ǣ� ��
A.��⾫��ͭʱ���������õ�������Ϊ2NA������������������64 g
B.0.1 mol KI��0.1 mol FeCl3����Һ�з�Ӧת�Ƶĵ�����Ϊ0.1NA
C.1 L 0.5 mol��L-1��������Һ����������������Ŀ����NA
D.0.1 mol��������(![]() )�к��й��ۼ�������ԼΪ0.3��6.02��1023
)�к��й��ۼ�������ԼΪ0.3��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������������γ����������꣬�������γɹ⻯ѧ�������Ժ��е�������ķ������д�����
(1)������������Һ�������շ����еĵ��������Ӧ�Ļ�ѧ����ʽ���£�
NO2��NO��2NaOH===2NaNO2��H2O��
2NO2��2NaOH===NaNO2��NaNO3��H2O��
�ڷ�Ӧ���У���������________________����ԭ����________________���ڷ�Ӧ���У��������ͻ�ԭ�������ʵ���֮��Ϊ___________________________________________��
(2)����β���к���CO��NO���������������ʶԴ�������Ⱦ�ķ����ǰ�װ��ת������ʹ���Ƿ�����Ӧ����N2��CO2���÷�Ӧ�Ļ�ѧ����ʽΪ____________________________��
(3)�ɷ�Ӧ���ж϶��������Ƿ�Ϊ����������(������������������)________��ԭ����________________________________________________________________________��
(4)Ŀǰ��һ��������������һ�������£��ð�������������ת��Ϊ����Ⱦ�����ʣ���д���÷�Ӧ�Ļ�ѧ����ʽ��________________________________________________���÷�Ӧ�У���������________������������________������1.4 mol����ʱ��ת�Ƶ��ӵ����ʵ���Ϊ_______________________________________________��
(5)Ϊ�˱�����������ҵ�ϳ�ͨ��NH3ʹ����������Ͱ�ת��Ϊ����N2������NO2��NO�Ļ������3 L��ͨ��3 L(ͬ��ͬѹ��)NH3��ǡ��ʹ����ȫת��ΪN2����ԭ���������NO2��NO�����ʵ���֮��Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ӵ������������Ҫ���Ƚϸߵ������̣�Ŀǰ��ҵ������������(�ơ�þ������)�����ߣ�������ͼ���̿���ȡ���Ƚϸߵ���������Һ��

��Ӧ��ʹ�������ɷ�����ij������Է�Ӧ��ǰ������ʺ��������(��350g/LMnSO4��)���£�
���� | ����ǰ/g | ������/g | ȥ����/% |
Fe2+��Fe3+ | 0.001275 | 0.001275 | �� |
Ca2+ | 0.490000 | 0.021510 | 95.61 |
Mg2+ | 0.252000 | 0.025100 | 90.04 |
(1)����x��������_____��
(2)�Է�����þȥ�������ͬ��ԭ��_____��
(3)����Һ�м���KMnO4���Խ�Fe2+����ΪFe3+��ͬʱ����Mn2+���÷�Ӧ�����ӷ���ʽΪ_____��
(4)��֪�������������������pH
Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
��ʼ����ʱ | 6.3 | 1.5 | 8.3 |
��ȫ����ʱ | 8.3 | 2.8 | 9.8 |
ע���������ӵ���ʼŨ��Ϊ0.1mol/L
���ݱ������ݽ��������Тڵ�Ŀ�ģ�_____��
(5)��һ���о������������Ӧ�ٺ���ֱ�Ӽ���KMnO4��ͬʱ���Ƽ����������Ӧ�����pH��Ȼ���ٹ��ˣ����Խ�һ����߸�þ��ȥ���ʣ���þȥ������ߵ�ԭ�������¼��裺
����I��Fe2+��������Fe3+��Fe3+ˮ�����ɵ�Fe(OH)3�����˳����
����II��Mn2+�뷴Ӧ���ɵĻ���MnO2�����˳����
ѡ���ʵ������Լ������ʵ����֤�����Ƿ����____________________��
(6)����ӵ�س�ŵ�����У����������������֮�������ƶ�������һ��ҡ�Σ�����ҡ��ʽ����������͵�����ӵ�ع���ԭ����ͼ��ʾ��

�ٷŵ�ʱLi+���ƶ������__________������_____(����a������b��)��
����֪�缫�ܷ�Ӧ��LiCoO2+C![]() Li1��xCoO2+CLix��д���ŵ�ʱ�����ĵ缫��Ӧʽ__��
Li1��xCoO2+CLix��д���ŵ�ʱ�����ĵ缫��Ӧʽ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��Ӧԭ���о�̼��������ĵ��ʼ��仯����ķ�Ӧ�Ի������Ⱦ����ԴΣ��������Ҫ���塣
I.��Ϊ��Ҫ�Ļ���ԭ�ϣ��й㷺��;��
(1)�ϳɰ��е������������з�Ӧ��ȡ��
a. CH4(g)+H2O(g)CO(g)+3H2(g) H1=+216.4kJ/mol
b. CO(g)+H2O(g)CO2(g)+H2(g) H2=-41.2kJ/mol
��ӦCH4(g)+2H2O(g)CO2(g)+4H2(g) H= _____________��
(2)��ʼʱͶ�뵪�������������ʵ����ֱ�Ϊ1mol��3mol���ڲ�ͬ�¶Ⱥ�ѹǿ�ºϳɰ���ƽ��ʱ������а�������������¶ȵĹ�ϵ��ͼ��

�ٺ�ѹʱ����Ӧһ���ﵽƽ��״̬�ı�־��_____________(�����)
A.![]() ��
��![]() ��ת������� B.��Ӧ��ϵ�ܶȱ��ֲ���
��ת������� B.��Ӧ��ϵ�ܶȱ��ֲ���
C.![]() ���ֲ��� D.
���ֲ��� D.![]()
��P1_____P2 (����>����=��������ȷ��������ͬ)����Ӧ��ƽ�ⳣ����B��_______D�㡣
��C��![]() ��ת����Ϊ________����A��B���������£��÷�Ӧ�ӿ�ʼ��ƽ��ʱ���ɵ�����ƽ�����ʣ���(A)__________��(B)��
��ת����Ϊ________����A��B���������£��÷�Ӧ�ӿ�ʼ��ƽ��ʱ���ɵ�����ƽ�����ʣ���(A)__________��(B)��
��.�ü�ӵ绯ѧ��ȥ��������NO��ԭ������ͼ��ʾ��
��֪��������Һ�����ԣ��������ĵ缫��ӦʽΪ_____________����Ӧ������ͨ�����ӽ���Ĥ(ab)��![]() Ϊ2molʱ�������������ɵ������ڱ�״���µ����Ϊ_____________L��
Ϊ2molʱ�������������ɵ������ڱ�״���µ����Ϊ_____________L��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������������ǵ�����������ʡ�
(1)�γ������ԭ��֮һ�ɼ�ʾ���£�
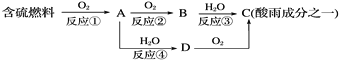
�ش��������⣺
�������pH________(���������������=��)5.6��
��D���ʵĻ�ѧʽΪ____________��
�۷�Ӧ�ڵĻ�ѧ����ʽΪ_________________________________________��
(2)��һ�������°��������������������ת��Ϊ����Ⱦ�����ʡ�д�������Ͷ���������һ�������·�Ӧ�Ļ�ѧ����ʽ��__________________����Ӧ����������____________����ԭ����_______________��
(3)������������Һ�������շ����еĵ��������Ӧ�Ļ�ѧ����ʽ���£�
NO2+NO+2NaOH===2NaNO2+H2O��2NO2+2NaOH===NaNO2+NaNO3+H2O
����VLijNaOH��Һ����ȫ����n molNO2��m molNO��ɵĴ�����Ⱦ�
�������ռ���Һ�����ʵ���Ũ������Ϊ________ mol��L1��
����������Һ��c(NO3��)��c(NO2��)=1��9����ԭ���������NO2��NO�����ʵ���֮��n��m=______��
���ú�n��m�Ĵ���ʽ��ʾ������Һ��NO3����NO2��Ũ�ȵı�ֵc(NO3��)��c(NO2��)=________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��С���������ʵ�飺
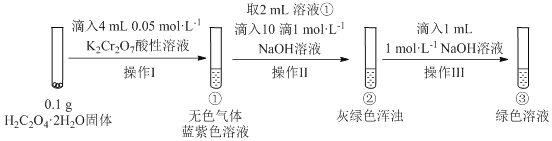
��֪��Cr2(SO4)3ϡ��ҺΪ����ɫ��Cr(OH)3Ϊ����ɫ���壬������ˮ�����й��ڸ�ʵ��Ľ��ۻ���������ȷ����
A.������������ɫ��Һ˵��K2Cr2O7�ڷ�Ӧ�б�����������
B.����II�н�������Ӧ��Cr3++3OH-�TCr(OH)3��
C.���������Һ�������ϻ��������ɫ���ǣ���������Cr3+��ˮ��ƽ���ƶ��й�
D.����������м���ϡ���ᣬ��Һ�п������±������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ķ����ģ��ش����⡣
ƽ�����»��Ļʽ�ϣ���2022����Լ���������ձ����̺��˷ḻ���й��Ļ���չ������ʱ���й�����


��èľż����èľż��2.35m��������Ϊ10kg�������Ͻ�ܲĺ�̼��ά������ܣ����LED���������ɡ����У�̼��ά�Ǻ�̼������90%�����Ͳ��ϣ��ܶȱ���С��ǿ�ȱȸִ�
���ܻ����ˣ��й���һ�����ܻ��������ֻ����߹��衢�������ڵ������ԡ����������Ժ�����Եȷ��棬ʵ�����˹�����������������¡�
ʯīϩ���ܷ��ȷ����������ܷ��ȷ�����20��������³�������4h��ʯīϩ��һ����̼ԭ�ӹ��ɵ������Ͷ�ά̼���ײ��ϣ����г���Ӳ�ȡ�ǿ�Ⱥ͵���ϵ�������ԡ�
���������϶��ģ��ж�����˵���Ƿ���ȷ����������������������
��1����èľż�����ܻ����ˡ�ʯīϩ���ܷ��ȷ�չ�������й��ǻ�����_____��
��2��̼��ά�������������ܣ����й㷺��Ӧ��ǰ����_____��
��3���й���һ�����ܻ������ڶ����������ȷ���ʵ�����˹�����������������¡�_____��
��4��ʯīϩ��ʯī��ͬ��Ԫ����ɣ������ǵ��������ʲ���ϴ�_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2��ת�����л���ʵ��̼ѭ�������ݻ�Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�����Ӧ��CO2��g����3H2��g��=CH3OH��g����H2O��g�������CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
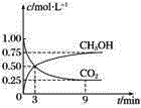
��1����3 min��9 min��v��H2����________ mol��L��1��min��1��
��2����˵��������Ӧ�ﵽƽ��״̬����________������ĸ����
A ��Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1��1����ͼ�н���㣩
B ���������ܶȲ���ʱ��ı仯���仯
C ��λʱ��������3 mol H2��ͬʱ����1 mol H2O
D CO2����������ڻ�������б��ֲ���
��3��һ���¶��£���9 minʱv����CH3OH��________��������������С������������������3 minʱv����CH3OH����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com