
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶 |
| 干燥 |


科目:高中化学 来源: 题型:
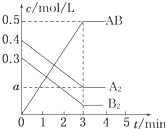 一定条件下,在一个容积为2L的密闭容器中加入0.8mol A2气体和0.6mol B2气体反应达平衡生成1mol AB气体并释放出热量,反应中各物质的浓度随时间的变化情况如图所示.下列说法不正确的是( )
一定条件下,在一个容积为2L的密闭容器中加入0.8mol A2气体和0.6mol B2气体反应达平衡生成1mol AB气体并释放出热量,反应中各物质的浓度随时间的变化情况如图所示.下列说法不正确的是( )| A、图中a点的值为0.15 |
| B、该反应的平衡常数K=0.03 |
| C、温度升高,平衡常数K值减小 |
| D、平衡时A2的转化率为62.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑤⑦⑧ | B、①②⑥⑦ |
| C、②③⑦⑧ | D、③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
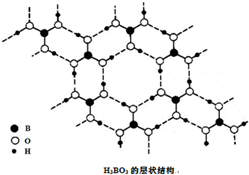 正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )| A、正硼酸晶体中只存在氢键 |
| B、H3BO3分子的稳定性与氢键有关 |
| C、分子中硼原子最外层为8电子稳定结构 |
| D、含1molH3BO3的晶体中有3mol氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液漏斗使用前要检验它是否漏水 |
| B、可以选用酒精作为萃取剂 |
| C、溴在萃取剂中的溶解度要大于在水的溶解度 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH溶液[Ba(OH)2]:用Na2SO4溶液 |
| B、CuO粉末[Fe粉]:用稀盐酸 |
| C、Mg粉[Al粉]:用NaOH溶液 |
| D、HNO3溶液[HCl]:用AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、点燃这种液体,然后观察火焰的颜色 |
| B、先加足量酸性高锰酸钾溶液,然后再加入溴水 |
| C、加入浓硫酸与浓硝酸后加热 |
| D、先加足量溴水,然后再加入酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1123K |
| 1023K |
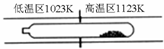
| A、在不同温度区域,TaI4的量保持不变 |
| B、在提纯过程中,I2的量不断减少 |
| C、该反应的平衡常数与TaI4和S2的浓度乘积成反比 |
| D、在提纯过程中,I2的作用是将TaS2从高温区转移到低温区 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com