
【题目】葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6![]() 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH![]() CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。

实验操作和现象:
操 作 | 现 象 |
点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 |
…… | |
实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有 性。
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是 ;
②乙根据现象认为实验中产生的SO2和 ,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)

现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是 ;乙设计的实验D中盛放的试剂是 ,装置连接顺序为 。
b.能说明确实是SO2使E中溶液褪色的实验是 。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是 。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时发生的化学方程式 。

(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤ mol·L-1。
【答案】(1)脱水性(1分)(2)①CH2=CH2+ Br2→ CH2Br—CH2Br(1分)②H2O (1分)③a.NaOH 溶液(1分)浓硫酸(1分)(d)cabe(f)(2分)b.加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2(2分)c.SO2+ 2H2O +Br2="=" 4H++2Br-+ SO42- 、SO42- + Ba2+="=" BaSO4↓或SO2+ 2H2O +Br2+ Ba2+="=" 4H++ 2Br-+ BaSO4↓(2分)(3)Na2S2O5+H2O=2NaHSO3(1分) 0.05(2分)
【解析】
试题(1)溶液慢慢变黑是因为浓硫酸将物质中的C和H以1:2的比例脱掉,所以表现浓硫酸的脱水性。
(2)①甲认为是C2H4,使B中溶液褪色是因为发生加成反应,反应的化学方程式是CH2=CH2+ Br2→ CH2Br—CH2Br;②乙根据现象认为浓硫酸同时可能被还原生成SO2和水;③a.甲设计实验中A、B间洗气瓶中盛放NaOH 溶液,将二氧化硫吸收,再通过Br2的CCl4溶液如若褪色,则说明是乙烯加成;将A中出来的气体通过浓硫酸除去水,再通过溴的四氯化碳,不褪色,再通过品红褪色,故连接为cabe(f);b.利用二氧化硫漂白的不稳定性,加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2;c. ,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+ 2H2O +Br2="=" 4H++2Br-+ SO42- 、SO42- + Ba2+="=" BaSO4↓。
(3)溶液的pH=4.5时,溶液中主要存在HSO3-,故Na2S2O5溶于水时发生的化学方程式:Na2S2O5+H2O=2NaHSO3。
(4)因为Ksp[BaSO4]=1×10-10,c(SO42-)≤1×10-5mol·L-1,故c(Ba2+)≥1×10-5mol·L-1,Ksp[BaSO3]=5×10-7,故c(SO32-)≤0.05 mol·L-1。


科目:高中化学 来源: 题型:
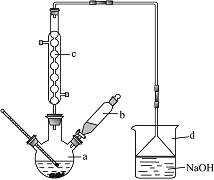
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了______气体。该反应为_______(填“吸热”或“放热”)反应,冷却水流向是_____________(填“上进下出”或“下进上出”),继续滴加至液溴滴完。其中仪器c的名称是________,其作用是:__________________________________。装置d的作用是:_____________________________________________________;烧瓶中发生的有机反应的方程式为:_______________________________________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL 10%的NaOH溶液、10mL水洗涤。洗涤、分离有机和无机试剂,需要用到的仪器是:_____________。第一次水洗除去大部分的HBr;用NaOH溶液洗涤的作用是______________;第二次水洗的目的是:____________;每一次洗涤,有机层从_________(填“下口放出”或“上口倒出”),棕黄色的溴苯经过提纯后恢复为无色。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________。
(3)经以上分离操作后,粗溴苯中还含有的主要杂质苯,要进一步提纯,下列操作中必须的是____(填入正确选项前的字母)。
A.蒸馏 B.渗析 C.分液 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示),下列说法错误的是

A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 常温下,(NH4)2Fe(SO4)2比FeSO4易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是

A. 图1表示10mL 0.01mol·L-1KMnO4酸性溶液与过量的0.1mol·L-1H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用)
B. 图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C. 图3表示示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀物质的量与盐酸体积的关系
D. 图4表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
(1)铝灰中氧化铝与硫酸反应的化学方程式为 。
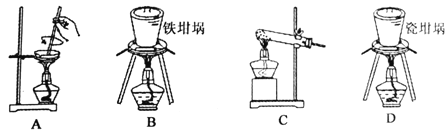
(2)用图中“滤渣”和NaOH焙烧制备硅酸钠,可采用的装置为 (填选项编号)。
(3)在实验流程中,加30%的H2O2溶液发生的离子反应方程式为 。
(4)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为 。
(5)若用调节pH溶液“沉铁”,则得到Fe(OH)3,已知:25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O![]() Fe(OH)3+3H+的平衡常数为 。
Fe(OH)3+3H+的平衡常数为 。
(6)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
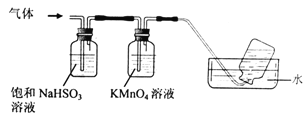
①集气瓶中收集到的气体是 (填化学式)。
②KMnO4溶液褪色,发生的离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分是Cu2(OH)2CO3。我国古人用孔雀石和焦炭混合共热的方法炼铜,其冶炼方法属于
A. 热还原法B. 湿法炼铜C. 热分解法D. 电解冶炼法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列无色溶液中,能大量共存的离子组是( )
A.Cu2+、H+、I-、SO42-B.Na+、Ba2+、NO3-、OH-
C.K+、Mg2+、CO32-、Cl-D.K+、H+、Cl-、MnO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用序号填空:
①13C与14C ②正丁烷与异丁烷
③CH3CH3与CH3CH2CH3 ④
(1)属于同位素的是______;
(2)属于同系物的是______;
(3)属于同分异构体的是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com