
【题目】氯化苄(C6H5CH2Cl)是一种重要的有机化工原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。
(1)写出甲苯与干燥氯气在光照条件下反应合成氯化苄的化学方程式________________。
(2)用下列方法分析氯化苄粗产品的纯度:
步骤I:称取2.555 g样品于烧瓶中,加入100.00 mL 4mol/L氢氧化钠溶液共热,冷却至室温。加入100.00 mL4mol/L硝酸,一段时间后,将烧瓶中的溶液全部转移至250.00 mL的容量瓶中,加水定容。
步骤II:从容量瓶中各取50.00 mL溶液于三只锥形瓶中,各加入25.00 mL0.2000mol/L硝酸银溶液。
步骤m:用硫酸铁铵作指示剂,用0.2000 mol/LNH4SCN溶液分别滴定剩余的硝酸银,所得滴定数据如下表。
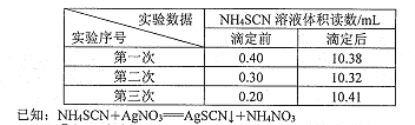
①加入硝酸的目的是____________。
②在步骤III操作中,判断达到滴定终点的现象是____。
③该样品中氯化苄的质量分数(写出计算过程)____。
④上述测定结果通常高于氯化苄中氯元素的理论含量,原因是___。
【答案】 C6H5CH3+Cl2![]() C6H5CH2Cl+HCl 中和NaOH使溶液呈酸性,防止OH—对下一步的干扰 当滴入最后一滴,溶液由无色变为红色,且半分钟内不褪色
C6H5CH2Cl+HCl 中和NaOH使溶液呈酸性,防止OH—对下一步的干扰 当滴入最后一滴,溶液由无色变为红色,且半分钟内不褪色 ![]() 甲苯与氯气在光照条件下可能生成多氯代物,Cl2或生成的HCl也会造成测定结果偏高
甲苯与氯气在光照条件下可能生成多氯代物,Cl2或生成的HCl也会造成测定结果偏高
【解析】(1)甲苯与干燥氯气在光照条件下反应合成氯化苄的化学方程式为C6H5CH3+Cl2![]() C6H5CH2Cl+HCl。(2)①溶液显碱性,则加入硝酸的目的是中和NaOH使溶液呈酸性,防止OH—对下一步的干扰。②铁离子能与SCN-反应使溶液显红色,则在步骤III操作中,判断达到滴定终点的现象是当滴入最后一滴,溶液由无色变为红色,且半分钟内不褪色。③三次实验中消耗标准液体积分别是9.98mL、10.02mL、10.21mL,第三次实验数据误差大,舍去,则消耗标准液体积的平均值是10.00mL,根据方程式可知剩余硝酸银是0.002mol,所以与氯离子反应的硝酸银是0.005mol-0.002mol=0.003mol,则水解生成的氯离子是0.003mol×250mL/50mL=0.015mol,因此该样品中氯化苄的质量分数为
C6H5CH2Cl+HCl。(2)①溶液显碱性,则加入硝酸的目的是中和NaOH使溶液呈酸性,防止OH—对下一步的干扰。②铁离子能与SCN-反应使溶液显红色,则在步骤III操作中,判断达到滴定终点的现象是当滴入最后一滴,溶液由无色变为红色,且半分钟内不褪色。③三次实验中消耗标准液体积分别是9.98mL、10.02mL、10.21mL,第三次实验数据误差大,舍去,则消耗标准液体积的平均值是10.00mL,根据方程式可知剩余硝酸银是0.002mol,所以与氯离子反应的硝酸银是0.005mol-0.002mol=0.003mol,则水解生成的氯离子是0.003mol×250mL/50mL=0.015mol,因此该样品中氯化苄的质量分数为![]() 。④由于甲苯与氯气在光照条件下可能生成多氯代物,且Cl2或生成的HCl也会造成测定结果偏高,因此上述测定结果通常高于氯化苄中氯元素的理论含量。
。④由于甲苯与氯气在光照条件下可能生成多氯代物,且Cl2或生成的HCl也会造成测定结果偏高,因此上述测定结果通常高于氯化苄中氯元素的理论含量。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】实验室现有一包粉末状药品,可能由NaCl、 FeCl3 、 Al2(SO4)3中的一种或多种组成,某同学为确定其组成,进行如下实验(所加试剂均为过量)。请回答下列问题:
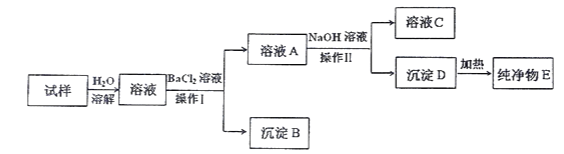
(1)操作Ⅰ的名称是___________。
(2)生产沉淀B的离子方程式为_________________________________。
(3)纯净物E是____________(填化学式,下同)。
(4)通过以上实验,确定该药品中一定含有______________,可能含有_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年科学家提出“绿色自由”构想。把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如图所示:
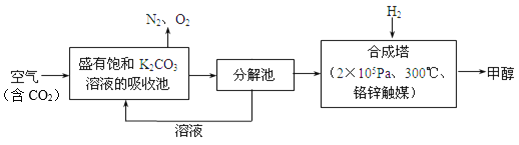
(1)分解池中主要物质是_______________。
(2)在合成塔中,若有4400 g CO2与足量H2反应,生成气态的H2O和甲醇,可放出5370 kJ的热量,写出该反应的热化学方程式_______________。
(3)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”_______________。
(4)一定条件下,往2L恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如下图所示:
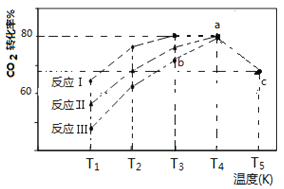
(图中c点的转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是________(填“反应I”,“反应II”,“反应III”)。
②b点v (正)_________v (逆)(填 “>”, “<”, “=”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是____________。
④c点时该反应的平衡常数K =____________________。
(5)科学家还研究了其它转化温室气体的方法,利用下图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为_______________。
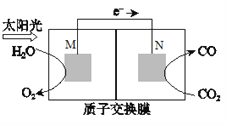
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A. 以铁作阳极,铂作阴极,电解饱和食盐水,可以制备烧碱
B. 25℃下,在NH3·H2O稀溶液中加水稀释,![]() 的值不变
的值不变
C. 工业生产硫酸时,接触室催化氧化S02时使用热交换器可以充分利用热量,降低生产成本
D. 反应![]() 室温下不能自发进行,则△H>0
室温下不能自发进行,则△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下(T2> Tl),在3个体积均为2.0 L的恒容密闭容器中反应 2NO(g)+ Cl2(g) = 2ClNO(g)(正反应放热)达到平衡,下列说法正确的是

A. 达到平衡时,容器I与容器II中的总压强之比为1:2
B. 达到平衡时,容器III中ClNO的转化率小于80%
C. 达到平衡时,容器II中c(ClNO(/ c(NO)比容器I中的大
D. 若温度为Tl,起始时向同体积恒容密闭容器中充入0.20 mol NO(g)、0.2 mol Cl2(g)和0.20 mol ClNO(g),则该反应向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是 ( )
A.将硝酸银溶液滴入浓氨水中制银氨溶液
B.蒸馏操作时应将温度计的水银球插入液面下
C.如果不慎将苯酚沾到皮肤上,应立即用酒精洗涤
D.向蔗糖溶液中加入几滴稀硫酸,水浴加热,然后向其中加入银氨溶液,观察到银镜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。实验室以木炭、浓硝酸、Na2O2为主要原料按照如图所示装置制各亚硝酸钠(加热装置及部分夹持装置已略去),反应原理为:2NO+Na2O2=2NaNO2。
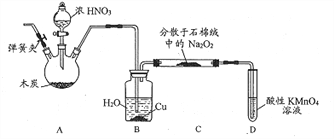
回答下列问题:
(1)A装置中反应的化学方程式为__________________。
(2)B装置中铜的作用是__________________。
(3)充分反应后,C中生成的固体除NaN02外,还可能有杂质生成,应在B、C之间加一个装置,该装置所盛放试剂的名称是_________________。
(4)检查装置气密性并装入药品后,以下实验操作步骤正确的顺序为____________________填标号)。
a.打开弹簧夹,向装置中通入N2 b.点燃酒精灯
c.向三颈烧瓶中滴加浓硝酸 d.熄灭酒精灯
e.关闭分液漏斗旋塞 f.停止通入N2
(5)D装置用于尾气处理,写出D中反应的离子方程式:___________________。
(6)利用改进后的装置,将7.8gNa2O2完全转化成NaNO2,理论上至少需要木炭____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。
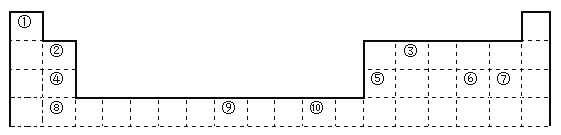
请回答下列问题:
(1)表中属于d区的元素是___________(填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_________。
(3)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是___________(用元素符号表示)。
(4)按原子轨道的重叠方式,③与⑥形成的化合物中σ键有______个,π键有______个。
(5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为_______;该元素与元素①形成的分子X的空间构形为___________。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是实验室蒸馏石油的实验装置,实验需要收集60~150℃和150~300℃的馏分。请回答下列问题:
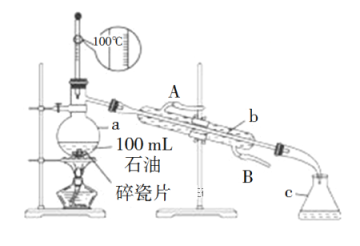
(1)仪器a的规格和名称:_______,仪器b、c的名称:b_______,c_______。
(2)温度计的使用是否正确_______(“正确”或“错误”)。
(3)实验时在仪器a中加入了少量碎瓷片,其目的是_______。
(4)实验时在仪器b中通入冷却水,请指明冷却水的流向_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com