
����Ŀ����һ�ݻ�Ϊ2�����ܱ������ڼ���0.2mol��N2��0.6mol ��H2 �� ��һ�������·������·�Ӧ��N2��g��+3H2��g��2NH3��g��+Q��Q��0������Ӧ��NH3�����ʵ���Ũ�ȵı仯���������ͼ��
��1��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v��NH3��Ϊ �� 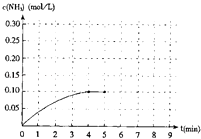
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ ��
��3����Ӧ�ﵽƽ���5����ʱ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ ��
A��0.20mol/L B��0.16mol/L C��0.10mol/L D��0.05mol/L
��4����Ӧ�ﵽƽ���5����ʱ�����������������䣬��ֻ�������������Сһ�룬ƽ���ƶ�������������ҡ�����������ѧƽ�ⳣ��K���������С�����䡱����
��5����5���Ӱ������������Сһ������ڵ�8���Ӵﵽ�µ�ƽ�⣨��ʱNH3��Ũ��ԼΪ0.25mol/L����������ͼ�л�����5���ӵ���ƽ��ʱNH3Ũ�ȵı仯���ߣ�
���𰸡�
��1��0.025mol/L��min
��2��K= ![]()
��3��A��C
��4������,����
��5��
���������⣺��1��v= ![]() =0.025 mol/L��min
=0.025 mol/L��min
���Դ��ǣ�0.025 mol/L��min��
��2����ѧƽ�ⳣ�� ![]()
���Դ��ǣ� ![]()
��3���÷�Ӧ�ǿ��淴Ӧ�����Է�Ӧ�ﲻ����ȫת��Ϊ�������������Ũ�Ȳ�����Ϊ0.20mol/L��Q��0�����Ը÷�Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ��������¶ȣ�ƽ��������Ӧ�����ƶ�����������Ũ�Ȳ�����Ϊ0.10mol/L����ѡAC��
��ѡ��A��C��
��4���÷�Ӧ�����������С�ķ�Ӧ���������������Сһ�룬�����˷�Ӧ��ϵ��ѹǿ������ѹǿ��ƽ�������������С�ķ����ƶ�����������Ӧ�����ƶ�����ѧƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ�����䣮
���Դ��ǣ����ң����䣮
��5���������������Сһ���˲�䰱����Ũ�ȣ�������Ũ�ȱ�Ϊ0.20mol/L��ƽ���Ũ��ԼΪ0.25mol/L��
���Դ��ǣ� 
�����㾫�������շ�Ӧ���ʵĶ�����ʾ�����ͻ�ѧƽ�ⳣ���ĺ����ǽ����ĸ�������Ҫ֪����Ӧ���ʵĵ�λ��mol/(L��min)��mol/(L��s) v=��c-��t��ָ��һ�������µĿ��淴Ӧ�����Ӧ���淴Ӧ��������ȣ���Ӧ������и���ֵ�Ũ�Ȳ����״̬��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȵ��������ȵ����壬���и��������ڵȵ�������
A��CO��CO2 B��NO��CO C��CH4��NH3 D�� OH- ��S2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ����ʹʳƷ��ɫ�����ʣ������Ӷ�ʳƷ���Ⱥü��̼�ʳ��������ء��������dz������ǹ���ѩ���ʳƷ����ɫ������Ҫ�ɷ֣��ṹ��ͼ��ʾ������˵����ȷ����

A. ����غͺ����ػ�Ϊͬ���칹��
B. һ�������º���غͺ����ض��ܷ����Ӿۺ����۷�Ӧ
C. ������к����Ѽ����ʻ������������ֺ���������
D. 1 mol�������������6 mol H2�����ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п����ΪʳƷпǿ������ԭ�ϡ���ҵ�ϳ�����п����������п����п�����Ҫ�ɷ���ZnCO3����������Fe2O3 ��FeCO3 ��MgO��CaO�ȣ�������������ͼ���£�
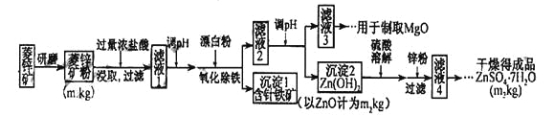
��1������п����ĥ�ɷ۵�Ŀ����___________________��
��2����������������������з�Ӧ�����ӷ���ʽ��
��Fe(OH)2+ ��____+ ��_____="=" ��Fe(OH)3+ ��Cl_
��3��������Goethite�����Ե¹�ʫ�˸�£�Goethe�����������ģ����Ԫ����Fe��O��H ����ѧʽʽ��Ϊ89����ѧʽ��_______ ��
��4�������±����ݣ���������Һ2����pHʱ�������Ͽ�ѡ�õ��������Ϊ______ ��
Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
��ʼ������pH | 10��4 | 6��4 | �� | �� |
������ȫ��pH | 12��4 | 8��0 | �� | �� |
��ʼ�ܽ��pH | �� | 10��5 | �� | �� |
Ksp | 5��6��10-12 | �� | 6��8��10-6 | 2��8��10-9 |
��5����ҵ�ϴ�����Һ3����ȡMgO�����У����ʵķ�Ӧ����_________��ѡ����ţ���
a������ʯ�� b��ʯ���� c��������Һ d���ռ���Һ
��6������Һ4��֮��IJ�������Ϊ ______ ��_______ �����ˣ�ϴ�ӣ����
��7������ͼ�����ݣ���п�����ZnC3���������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��Ⱥ������Ӽ����ֺ��зǼ��Լ����ǣ� ��
A.NaOH
B.Na2O2
C.MgCl2
D.H2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���в���ֱ�Ӳ��ʯī���������ɼ��鷴Ӧ�ķ�Ӧ�ȣ����ɲ�����飬ʯī������ȼ�յķ�Ӧ�ȣ�CH4��g��+2O2��g���TCO2��g��+2H2O��l����H1=��890.3kJ/mol
C��ʯī��+O2��g���TCO2��g����H2=��393.5kJ/mol
H2��g��+ ![]() O2��g���TH2O��l����H3=��285.8kJ/mol������ʯī���ɼ���ķ�Ӧ�ȣ�
O2��g���TH2O��l����H3=��285.8kJ/mol������ʯī���ɼ���ķ�Ӧ�ȣ�
C��ʯī��+2H2��g���TCH4��g����H4= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������л������Ũ�����Ժ�����ˮ����Ҫ����H+��Cl����Fe2+��Fe3+�ȣ��䴦������Ҫ�����������£�
��ش�
��1����ˮδ������ֱ���ŷŵ�Σ����������ĸ����
a��ʴˮ����ʩ bӰ��ˮ���������Ȼ����
��2��ʯ���������кͺ�����ˮ�е��ᣬд��ʯ���������ᷴӦ�Ļ�ѧ����ʽ�� ��
��3��������������Ҫ������������ĸ����a��ԭ�� b������
��4������ˮ������Ư�ۡ�Һ�ȡ��������ȡ���������Ϊ��������ɱ��ˮ�е�ϸ����Һ��ע��ˮ�к���ɱ��ˮ��ϸ�������������ѧʽ����
��5����ˮ�����е���Ҫ��ѧ�������кͷ������� ��
��6��ij�о�С��Ը�������Ũ�����Ժ�����ˮ���м��ʱ��ȡ������ϡ�ͣ�����й��������£�
���� | H+ | Cl�� | Fe2+ | Fe3+ |
Ũ�ȣ�molL����1 | 0.16 | 0.94 | 0.18 |
ϡ�ͺ����Һ��c��Fe2+��=mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�pH��12������������Һ��pH��4�Ĵ�����Һ�������Ϻ�ǡ���кͣ����Ի�Ϻ���Һ����ı仯������˵������ȷ���ǣ� ��
A.��Ϻ����Һ��c(Na��)��c(CH3COO��)
B.���ǰ�Ĵ���Լ1%��������
C.�������ƺʹ����Ũ�Ȳ����
D.��Ϻ����Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���˵���д������(����)
A. �γ���λ����������һ���пչ����һ���йµ��Ӷ�
B. ��λ����һ������Ĺ��ۼ�
C. NH4NO3��H2SO4���������
D. ���ۼ����γ������dzɼ�ԭ�ӱ�����δ�ɶԵ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com