
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是
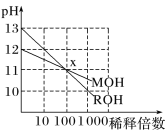
A. MOH是一种弱碱
B. 在x点,c(M+)=c(R+)
C. 稀释前,c(ROH)=10c(MOH)
D. 稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的10倍
【答案】C
【解析】
ROH开始的pH=13,稀释100倍pH=11,则ROH为强碱,而MOH开始的pH=12,稀释100倍pH=11,则MOH为弱碱。
A. MOH开始的pH=12,稀释100倍pH=11,则MOH为弱碱,A项正确;
B. 在x点时MOH和ROH溶液中c(H+)均为10-11 mol·L-1,c(OH-)均为10-3 mol·L-1,则根据电荷守恒知c(OH-)=c(M+)+c(H+)=c(R+)+c(H+),则c(M+)=c(R+),B项正确;
C. 稀释前,ROH pH=13,且ROH为强碱,则c(ROH)=0.1mol/L,而MOH pH=12,且MOH为弱碱,则c(MOH)>0.01mol/L,则c(ROH)<10c(MOH),C项错误;
D. 稀释前,ROH开始的pH=13,由水电离出的c(OH)=1013mol/L,MOH开始的pH=12,由水电离出的c(OH)=1012mol/L,则稀释前MOH溶液和ROH溶液中由水电离出的c(OH)前者是后者的10倍,D项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、Al2Cl7-和有机阳离子组成电解质溶液,其放电工作原理如图所示。下列说法正确的是
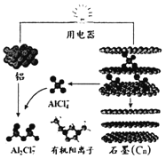
A.放电时电子由石墨电极经用电器流向铝电极
B.充电时铝电极上发生氧化反应
C.充电时,AlCl4-向铝电极方向移动
D.放电时,负极反应为Al-3e-+7AlCl4-═4Al2Cl7-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g (25℃),再加5 g水充分溶解,仍剩余固体4.80g(25℃)。
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为________________g(保留2位小数)
(2)若剩余的4.80g固体是MnO2和KCl的混合物,则25℃时KCl的溶解度为_____;原混合物中KClO3的质量为________________g(保留2位小数);所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为______mol/L(保留2位小数)。
(3)可用以下反应制备KIO3和K2H3IO6(高碘酸氢二钾):I2+2KClO3=2KIO3+Cl2① KIO3+Cl2+3KOH =K2H3IO6+2KCl ②最终制得的KIO3和K2H3IO6的物质的量之比x,若制得100molK2H3IO6, 共消耗ymolKClO3,试确定y与x的关系式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法正确的是( )
A.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质
B.工厂中常用的静电除尘装置是根据胶体带电这个性质而设计的
C.由于铝的导电性比铜、银都强,所以常用来制造电线、电缆
D.![]() 能氧化氮氧化物,可用于汽车尾气净化
能氧化氮氧化物,可用于汽车尾气净化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mol·L-1某一元酸HA的电离平衡常数约为1×10-7,下列叙述错误的是( )
A. 该溶液的pH=4
B. 此溶液中,HA约有0.1%发生电离
C. 加水稀释,HA的电离平衡向右移动,HA的电离平衡常数增大
D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在
转化规律,绘制出如下转化关系图,图中A、B、C、D是由短周期元素组成的物质。

请回答:
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体。则组成A的元素在周期表中的位置是__,C的电子式为__。
(2)若A为能使湿润红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是__。过量的A的水溶液与AlCl3溶液反应离子方程式为__。
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为__mol。
(3)若B为能使品红溶液褪色的无色刺激性的气体,B→C反应的化学方程式是__,B与KMnO4溶液反应离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于 2NaOH(s)+H2SO4(aq)→Na2SO4(aq)+2H2O(l)+Q kJ 说法正确的是( )
A.NaOH(s)溶于水的过程中扩散吸收的能量大于水合释放的能量
B.Q<0
C.NaOH(s)+1/2H2SO4(aq)→1/2Na2SO4(aq)+H2O(l)+1/2QkJ
D.若将上述反应中的NaOH(s)换成NaOH(aq),则Q′>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种国际公认的安全、无毒的绿色消毒剂,沸点11℃,凝固点-59℃。工业上,可用下列原理制备ClO2(液相反应):![]() 。设NA是阿伏伽德罗常数的值。下列说法正确的是( )
。设NA是阿伏伽德罗常数的值。下列说法正确的是( )
A.在标准状况下,2240mL ClO2含有原子数为0.3NA
B.若生成1.5mol Na2SO4,则反应后的溶液中Fe3+数目为0.2NA
C.48.0g FeS2完全反应,则上述反应中转移电子数为6NA
D.每消耗30mol NaClO3,生成的水中氢氧键数目为14NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系式为
4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系式为
A.4v(NH3)=5v(O2)B.5v(O2)=6v(H2O)
C.2v(NH3)=3v(H2O)D.4v(O2)=5v(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com