
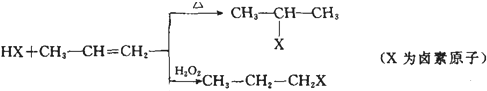
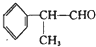
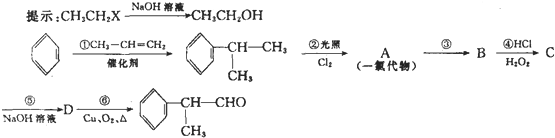
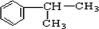 ,在光照条件下
,在光照条件下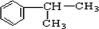 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为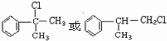 ,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为
,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为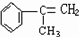 ,则C为
,则C为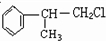 ,结合根据产物可知D为
,结合根据产物可知D为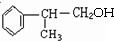 ,以此解答该题.
,以此解答该题.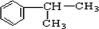 ,在光照条件下
,在光照条件下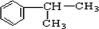 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为 ,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为
,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为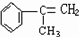 ,则C为
,则C为 ,结合根据产物可知D为
,结合根据产物可知D为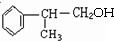 ,
, ,故答案为:
,故答案为: ;
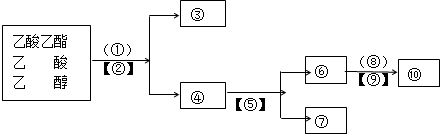
;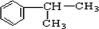 ,反应③是A(卤代烃)在氢氧化钠醇溶液、加热条件下发生消去反应,故答案为:加成反应;消去反应;
,反应③是A(卤代烃)在氢氧化钠醇溶液、加热条件下发生消去反应,故答案为:加成反应;消去反应;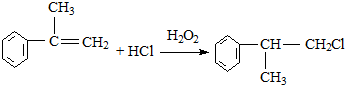 ,
,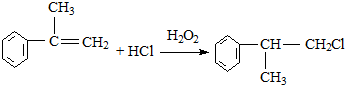 ;
;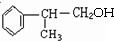 ,故答案为:
,故答案为: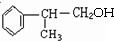 ;
; ,D为
,D为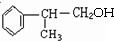 ,反应中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是:A的结构有2种,若直接转化为D,得到D的结构也有2种,其中一种不能转化为最终产品,原料利用率低,
,反应中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是:A的结构有2种,若直接转化为D,得到D的结构也有2种,其中一种不能转化为最终产品,原料利用率低,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
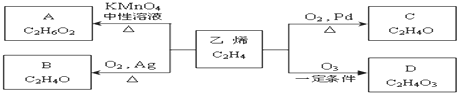
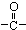 )化合物,如:RCH=CH-OH→R-CH2-CHO.取1.24g A与过量的金属钠完全作用后,生成448mL(标准状况)气体,B、C都可由A脱水生成,C能发生银镜反应而B不能.
)化合物,如:RCH=CH-OH→R-CH2-CHO.取1.24g A与过量的金属钠完全作用后,生成448mL(标准状况)气体,B、C都可由A脱水生成,C能发生银镜反应而B不能.查看答案和解析>>
科目:高中化学 来源: 题型:
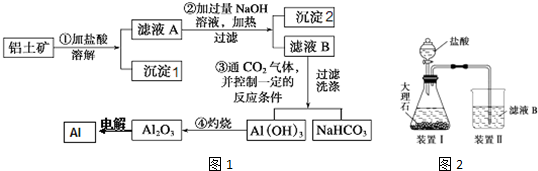
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、容器Ⅰ、Ⅲ中平衡常数相同 |
| B、容器Ⅱ、Ⅲ中正反应速率相同 |
| C、SO3的体积分数:Ⅱ<Ⅲ |
| D、容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com