
����Ŀ��(1).��һ���������İ�������������ܱ����������(���������������,��������������Բ���),�ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺H2NCOONH4(s)![]() 2NH3(g)+CO2(g)ʵ���ò�ͬ�¶��µ�ƽ�����������±���
2NH3(g)+CO2(g)ʵ���ò�ͬ�¶��µ�ƽ�����������±���
�¶�/�� | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
ƽ��������Ũ��/ (��10-3mol��L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
�ٰ�������立ֽⷴӦ���ʱ��H__________0(��">"��"<)
�ڿ����жϸ÷ֽⷴӦ�Ѿ��ﵽ��ѧƽ�����__________(����ĸ);
A.2v(NH3)=v(CO2)
B.�ܱ���������ѹǿ����
C.�ܱ������л��������ܶȲ���
D.�ܱ������а����������������
�۸��ݱ�������,����25.0��ʱ�ķֽ�ƽ�ⳣ��Ϊ__________.
(2).��֪25��ʱ,NH3��H2O���볣��Kb=1.8��10-5,Mg(OH)2���ܶȻ�����Ksp=1.8��10-11,����0.5mol��L-1��ˮ��pHԼΪ__________(��֪lg3��0.5)����ijMgCl2��Һ�м���һ������ijŨ�ȵİ�ˮ��,��û��Һ��pH=11,����¶��²�������Һ�е�c(Mg2+)=__________.
���𰸡��� ��> (1��)��Bc(2��)��1.64��10-8mol3/L3����д��λ���۷֣���λд��0�֣�(2��)
��11.5(2��) 1.8��10-5mol/L(2��,��ֵ��ȷ��λ��1��)
��������
�Ţ��ɱ������ݿ�֪���¶����ߣ�ƽ��ʱ������Ũ�ȱ��ƽ�������ƶ������������ȷ�Ӧ����H >0���𰸣�> ����A����ȷ������ȷ�����淴�����Ƿ���ȣ�������v��NH3������=2v��CO2��������B����ȷ��ֻҪƽ�ⷢ���ƶ���ѹǿ�ͷ����仯��C����ȷ����Ӧǰ����������������仯��D������ȷ������ƽ���Ƿ��ƶ���NH3�������������ռ2/3.��ƽ��ʱ��NH3��CO2��Ũ�ȷֱ�Ϊ4��8��10��3 mol/L��2/3=3.2��10��3 mol/L��4��8��10��3 mol/L��1/3=1.6��10��3 mol/L��K= ��3.2��10��3 mol/L��2��1.6��10��3 mol/L=1.64��10-8mol3/L3���𰸣�1.64��10-8mol3/L3��
��NH3��H2O![]() NH4����OH�D,Kb=1��8��10��5= c(NH4��)c(OH�D)/c(NH3��H2O)=c2(OH�D)/c(NH3��H2O),�ã�c(OH�D)=
NH4����OH�D,Kb=1��8��10��5= c(NH4��)c(OH�D)/c(NH3��H2O)=c2(OH�D)/c(NH3��H2O),�ã�c(OH�D)=![]() , pH=14��lg3��10-3=14-3��lg3=11.5;PH=11ʱ��c(OH�D)=10-3mol/L��c��Mg2+��=Ksp/c2(OH�D)=1��8��10��11/(10-3)2=1.8��10-5mol/L���𰸣�1.8��10-5mol/L��
, pH=14��lg3��10-3=14-3��lg3=11.5;PH=11ʱ��c(OH�D)=10-3mol/L��c��Mg2+��=Ksp/c2(OH�D)=1��8��10��11/(10-3)2=1.8��10-5mol/L���𰸣�1.8��10-5mol/L��
����:��ѧƽ�⼰���ڵ������Һ�е�Ӧ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Cl2��NaOH��CO(NH2)2 (����)��SO2Ϊԭ�Ͽ��Ʊ�N2H4��H2O(ˮ����)����ˮNa2SO3������Ҫʵ���������£�

��֪����Cl2+2OH![]() ClO+Cl+H2O�Ƿ��ȷ�Ӧ��
ClO+Cl+H2O�Ƿ��ȷ�Ӧ��
��N2H4��H2O�е�Լ118 �棬����ǿ��ԭ�ԣ�����NaClO���ҷ�Ӧ����N2��

(1)��ͼ��ʾ��ʯī���缫����һ�������µ�ⱥ��ʳ��ˮ��ȡCl2ʱ�������ϲ���Ҳ�����������ClO2�ĵ缫��Ӧʽ��________________________________�����һ��ʱ�䣬������������״��������112 mLʱ��ֹͣ��⣬��ͨ�������ӽ���Ĥ�����������ʵ���Ϊ________mol��
(2)������Ʊ�NaClO��Һʱ�����¶ȳ���40����Cl2��NaOH��Һ��Ӧ����NaClO3��NaCl�������ӷ���ʽΪ____________________________________��ʵ���п����¶ȳ��ñ�ˮԡ�⣬�����ȡ�Ĵ�ʩ��____________________________________��
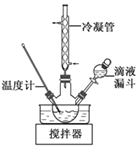
(3)�����ϳ�N2H4��H2O��װ������ͼ��ʾ��NaClO������Һ������ˮ��Һ��40 �����·�Ӧһ��ʱ�����Ѹ��������110 �������Ӧ��ʵ����ͨ����Һ©���μӵ���Һ��_________________��ʹ�������ܵ�Ŀ����_________________________________��
(4)������ò����õ��ĸ���ƷNa2CO3�Ʊ���ˮNa2SO3�����ⶨ�������Ʋ�Ʒ�Ĵ����������ʵ�鷽����������ʵ�顣ȷ��ȡ��������������Ʒm g���ձ��У�������������ˮ���100 mL������Һ����ȡ25.00 mL������Һ����ƿ�У���c mol��L��1����KMnO4��Һ�ζ������ζ��յ㡣�ظ�2�Σ�������ı���Һ�������ƽ��ֵΪV mL(�������ʲ���Ӧ)����Ʒ���������Ƶ���������Ϊ__________(�ú�m��c��V�Ĵ���ʽ��ʾ)��ijͬѧ��Ƶ����еζ���ʽ�У���������________(�гֲ�����ȥ)(����ĸ���)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������뽺��֪ʶ�ص���
A. ���Ȼ�����Һ�м����������������Һ�ῴ�����ɫ����
B. �����뺣�ڳ����������γ�
C. �ڵ�ӰԺ����Ӱ���ῴ���ӷ�ӳ�ҵ���Ļ�Ĺ���
D. ��±ˮ�㶹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3��g��+ 5O2��g��![]() 4NO��g��+ 6H2O��g��������������ȷ����
4NO��g��+ 6H2O��g��������������ȷ����
A. �ﵽ��ѧƽ��ʱ��4������O2��= 5������NO��
B. ����λʱ��������x mol NO��ͬʱ������x mol NH3 ����Ӧ�ﵽƽ��״̬
C. �ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ��������
D. ��ѧ��Ӧ���ʹ�ϵ�ǣ�2������NH3��= 3������H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦN2��3H2![]() 2NH3�������淴Ӧ���ʿ��ø���Ӧ���������Ũ�ȵı仯����ʾ�����и���ϵ����˵����Ӧ�Ѵﵽƽ��״̬����
2NH3�������淴Ӧ���ʿ��ø���Ӧ���������Ũ�ȵı仯����ʾ�����и���ϵ����˵����Ӧ�Ѵﵽƽ��״̬����
A. 3v��(N2)=v��(H2)B. 2v��(N2)=v��(NH3)
C. v��(N2)=3v��(H2)D. 2v��(H2)=3v��(NH3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����12�֣��±�ΪԪ�����ڱ���һ���֣������Ԫ���������ڱ��е�λ�ã��û�ѧ����ش��������⣺

��1��������������ԭ�Ӱ뾶�ɴ�С��˳��Ϊ___________________��
��2����������������ۺ������������ǿ������˳����____________��
��3�����������������е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ����д������һ�ֻ�����ĵ���ʽ��____________________��
��4���ɱ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬�������ϡҺ�ױ����ֽ⣬��ʹ�õĴ���Ϊ������ţ�_________________��
a.MnO2 b.FeCl3c.Na2SO3d.KMnO4
��5���ɱ���Ԫ���γɵij�������X��Y��Z��M��N�ɷ������·�Ӧ��
X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ_____________________��
N�����ĵ��ʵĻ�ѧ����ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽���ܴﵽ��Ӧʵ��Ŀ�ĵ���
ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
A | ����Fe2O3��Al2O3 | �������Ͷ������NaOH��Һ��Ȼ�����ν��й�����ϴ�ӡ������������������ |
B | ��֤������Һˮ������������ | �������Һ�м���ϡ���Ṳ�ȣ���ȴ���ټ�������Cu(OH)2����Һ������ |
C | �Ʊ���ˮAlCl3 | ��������ϡ���ᷴӦ�����Һ |
D | ����FeCl2�����Ƿ���ȫ���� | ȡ�������õ�FeCl2�������Թ�������μ������Ը��������Һ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���ѧʽ��ȷ��ʾ���ʷ�����ɵ���( )
A.�Ȼ��ƾ���(NaCl)B.�ɱ�(CO2)
C.ˮ��(SiO2)D.���(Ar)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��D���ɳ����Ķ����ڷǽ���Ԫ���γɵĵ��ʣ�������A�ǵ���ɫ��ĩ��B��D�����壬F��G��H����ɫ��Ӧ��Ϊ��ɫ��ˮ��Һ���Լ��ԣ�E��Ư���ԡ�����֮���ת����ϵ��ͼ��ʾ�����ֲ��P��Ӧ��������ȥ�����ش��������⣺
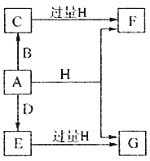
��1��A����Ԫ�������ڱ��е�λ��Ϊ______________��C�ĵ���ʽΪ_______________��
��2��A��H�ڼ��������·�Ӧ�Ļ�ѧ����ʽΪ__________________��
��3����A���ڷ��ڵ�G��Һ�п����Ƶû�����I��I��������Һ�в��ȶ��������ɵ����ʵ�����A��E��I����������������A��E�����ӷ���ʽΪ____________________��I����ǿ��ԭ�����ڷ�֯����ֽ��ҵ����Ϊ���ȼ�����I��Һ��ͨ�������ɷ�����Ӧ���μӷ�Ӧ��I�����������ʵ�����Ϊ1:4���÷�Ӧ�����ӷ���ʽΪ__________________��
��4������0.4molF��0.1molG�Ļ����Һ�м���������ᣬ��ȫ��Ӧ���ռ���aL����C����״������ȡ��Ӧ�������Һ���������FeCl3��Һ���õ�����3.2g����a=____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com