
【题目】常温时,100 mL 0.10 mol·L-1 H2A溶液用0.10 mol·L-1NaOH溶液滴定,滴定曲线如图所示。已知:p![]() = -lg
= -lg![]() 。下列说法不正确的是
。下列说法不正确的是

A.水的电离程度:Y>X>W
B.NaHA溶液呈酸性
C.反应H2A+A2- ![]() 2HA-的平衡常数K=105.6
2HA-的平衡常数K=105.6
D.Y点溶液中:c (Na+)=c (OH-)+3c (HA-)-c (H+)
【答案】C
【解析】
第一次反应终点:![]() ,第二次反应终点:
,第二次反应终点:![]() ,第二次反应终点pH=11.9,为碱性,即
,第二次反应终点pH=11.9,为碱性,即![]() 为强碱弱酸盐,
为强碱弱酸盐,![]() 为弱酸,且第一步电离为
为弱酸,且第一步电离为![]() ,
,![]() ,第二步电离为
,第二步电离为![]() ,
,![]() ,W点溶质为
,W点溶质为![]() 、
、![]() ,X点溶质为
,X点溶质为![]() ,Y点溶质为
,Y点溶质为![]() 、
、![]() 。
。
A. W、X、 Y三点均含![]() ,而W点还含
,而W点还含![]() ,酸对水的电离起抑制作用,而Y点还有
,酸对水的电离起抑制作用,而Y点还有![]() ,
,![]() 的水解对水的电离起促进作用,故水的电离程度:Y>X>W,A正确;
的水解对水的电离起促进作用,故水的电离程度:Y>X>W,A正确;
B. NaHA溶液中存在:![]() ,
,![]() 还存在:
还存在:![]()
![]() ,
,![]() >
>![]() 以电离为主,呈酸性,B正确;
以电离为主,呈酸性,B正确;
C. 反应H2A+A2-![]() 2HA-的平衡常数
2HA-的平衡常数![]() ,C不正确;
,C不正确;
D. Y点溶液中溶质为![]() 、
、![]() ,根据电荷守恒:c (H+)+c (Na+)=c (OH-)+c (HA-)+2 c (A2-),由图可知在Y点,c (HA-)=c (A2-),则c (H+)+c (Na+)=c (OH-)+3c (HA-),再移项得:c (Na+)=c (OH-)+3c (HA-)-c (H+),D正确。
,根据电荷守恒:c (H+)+c (Na+)=c (OH-)+c (HA-)+2 c (A2-),由图可知在Y点,c (HA-)=c (A2-),则c (H+)+c (Na+)=c (OH-)+3c (HA-),再移项得:c (Na+)=c (OH-)+3c (HA-)-c (H+),D正确。
答案选C。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】常温下,向![]() 的
的![]() 溶液中逐滴滴加
溶液中逐滴滴加![]() 的
的![]() 溶液。溶液
溶液。溶液![]() 随滴入
随滴入![]() 溶液体积变化如图所示。下列说法正确的是( )
溶液体积变化如图所示。下列说法正确的是( )
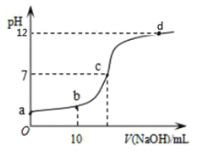
A.![]() 点的
点的![]()
B.![]() 点时,
点时,![]()
C.![]() 点时,
点时,![]()
D.从a→d,水的电离度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氧化铁样品中含有少量的硫酸亚铁。某同学要测定其中铁元素的质量分数,设计了如下实验方案。

(1)操作Ⅰ中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有__________(填仪器名称)。
(2)反应①中加入足量H2O2溶液,反应的离子方程式:_______________________________。
(3)检验沉淀中![]() 是否洗涤干净的操作是_______________________________________。
是否洗涤干净的操作是_______________________________________。
(4)将沉淀加热,冷却至室温,用天平称量坩埚与加热后固体的总质量为b1g,再次加热并冷却至室温称其质量为b2g,若b1-b2=0.3,还应进行的操作是_____________________。
(5)坩埚的质量为42.6 g,最终坩埚与加热后的固体的总质量为45.8 g,则样品中铁元素的质量分数为________________。
(6)有同学认为上述方案的实验步骤太繁琐,他认为,只要将样品溶于水充分搅拌,加热、蒸干、灼烧称量即可测得样品中铁元素的质量分数,你认为他的这个方案是否可行?__________(填“可行”或“不可行”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,以NH3作氢源,可实现电化学氢化反应。下列说法错误的是

A.a为阴极
B.b电极反应为:2NH3-6e-=N2+6H+
C.电解一段时间后,装置内H+数目增多
D.理论上每消耗1 mol NH3,可生成1.5mol![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于离子反应,又属于氧化还原反应的是( )
A. NaOH溶液与盐酸中和B. Zn与CuSO4 溶液的反应
C. 分解氯酸钾制氧气D. MgCl2溶液 与KOH溶液产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)![]() C(g) +D(g)发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是
C(g) +D(g)发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是
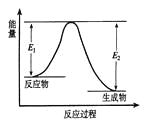
A. 反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B. 反应体系中加入催化剂,反应速率增大,△H不变
C. △H < 0,反应达到平衡时,升高温度,A的转化率增大
D. △H > 0,反应达到平衡时,升高温度,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )
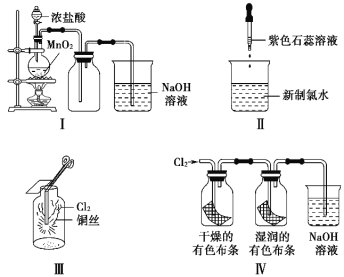
A. Ⅰ图:若MnO2过量,则浓盐酸可全部消耗完
B. Ⅱ图:证明新制氯水只有酸性
C. Ⅲ图:产生了棕黄色的雾
D. Ⅳ图:湿润的有色布条褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钾常用作食盐加碘剂以防止缺碘疾病,也是常用的基准物质和氧化剂。工业上碘酸钾可用如图所示装置进行制备。下列说法错误的是( )
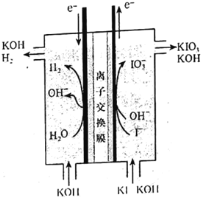
A.其阳极反应式是I-+3H2O-6e-=IO![]() +6H+
+6H+
B.该工业过程中KOH是循环利用的物质
C.制得21.4gKIO3产生标况下H26.72L
D.该工业过程使用阳离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com