
【题目】下列化合物中阳离子半径和阴离子半径之比最大的是( )
A. LiI B. NaBr C. KCl D. CsF
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列化学方程式或离子方程式,书写规范、正确的是(反应条件略)
A. 
B. 
C. 苯酚钠溶液中通入少量二氧化碳的离子方程式:![]() +H2O+CO2→
+H2O+CO2→![]() +HCO3-
+HCO3-
D. 乙酸与碳酸钠溶液反应的离子方程式:2H++CO32-=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)反—2-丁烯的结构简式____;
(2) ![]() 的名称为________;
的名称为________;
(3)丙氨酸在一定条件下发生缩聚反应的方程式:____________________;
(4)  单体的结构简式________________。
单体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用铁及其化合物有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是(______)
A.铁在冷的浓硝酸中钝化 B.生铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素 D.铁在一定条件下,可与水蒸气反应
(2)向沸水中逐滴滴加1 mol·L-1FeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为________________________________
(3) 焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生反应的体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
①写出并配平该反应的化学方程式:_________________________________
②发生氧化反应的物质是________,反应中4 mol的氧化剂能________(填“失去”或“得到”)________ mol电子。
③反应中产生了11.2 L(标准状况)的气体时,被还原的物质的质量为________。
(4)高铁酸钠Na2FeO4 是一种新型净水剂。
①高铁酸钠主要通过如下反应制取:
2Fe(OH)3+3NaClO+4NaOH===2Na2FeO4+3X+5H2O,则X的化学式为___________。
②高铁酸钠在水中可以发生如下反应:4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。
由此看来,高铁酸钠能够杀菌消毒是因为它具有________性,而能够除去水中悬浮物是因为_______________________________________________________
③下列物质能作净水剂(能除去水中的悬浮物)的有____________。
A.KAl(SO4)2·12H2O B.[Fe(OH)(SO4)]n C.ClO2 D.“84”消毒液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示石墨仅表示出其中的一层结构:
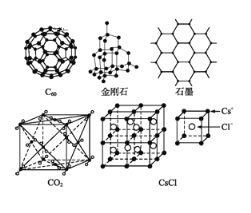
(1)C60、金刚石和石墨三者的关系是互为 ______ ;
A. 同分异构体 B.同素异形体C.同系物 D.同位素
(2)晶体硅的结构跟金刚石相似,1mol晶体硅中含有硅硅单键的数目是 ______ ![]() ;
;
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是 ______ ;
(4)观察![]() 分子晶体结构的一部分,每个
分子晶体结构的一部分,每个![]() 分子周围有 ______ 个与之紧邻且等距的
分子周围有 ______ 个与之紧邻且等距的![]() 分子;
分子;
(5)观察图形推测,CsCl晶体中两距离最近的![]() 间距离为a,则每个
间距离为a,则每个![]() 周围与其距离为a的
周围与其距离为a的![]() 数目为 ______ ,每个
数目为 ______ ,每个![]() 周围紧邻且等距的
周围紧邻且等距的![]() 数目为 ______ 。
数目为 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、M、R五种元素中,原子序数依次增大,其结构或性质信息如下表。请根据信息回答有关问题:
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 在元素周期表的各元素中电负性仅小于氟 |
M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子 |
R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
(1)元素M的原子核外有 ______ 种不同运动状态的电子;
(2)五种元素中第一电离能最高的是_______写元素符号;
(3)在Y形成的单质中,![]() 键与
键与![]() 键数目之比为______,在
键数目之比为______,在![]() 中Z原子的杂化方式为_____,其分子的空间构型为 ______;
中Z原子的杂化方式为_____,其分子的空间构型为 ______;
(4)R的一种配合物的化学式为![]() 。已知
。已知![]() 在水溶液中用过量硝酸银溶液处理,产生
在水溶液中用过量硝酸银溶液处理,产生![]() AgCl沉淀,此配合物最可能是 ______填序号。
AgCl沉淀,此配合物最可能是 ______填序号。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯用途广泛,工业上可通过下列流程合成二甘醇及其衍生物。已知:R-OH + SOCl2 → R-Cl + SO2 ↑+ HCl↑ 请回答:

(1)写出B的官能团的电子式________________________。
(2)写出有关物质的结构简式:A_________________D_________________。
(3)指出反应类型:②_________________。
(4)写出下列化学方程式:反应①______________;反应②___________。
(5)①二甘醇又名(二)乙二醇醚,根据其结构判断下列说法正确的是____(填序号)。
a. 难溶于水 b. 沸点较高 c. 不能燃烧
②E的同分异构体很多,写出其中能够发生银镜反应的两种异构体的结构简式_________________。
(6)请写出由1-氯丙烷合成丙酮的合成路线图并注明反应条件(无机试剂任选)________。合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() Br-CH2CH2-Br
Br-CH2CH2-Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢卤酸的能量关系如图所示下列说法正确的是

A. 已知HF气体溶于水放热,则HF的△H1<0
B. 相同条件下,HCl的△H2比HBr的小
C. 相同条件下,HCl的△H3+△H4比HI的大
D. 一定条件下,气态原子生成1molH-X键放出akJ能量,则该条件下△H2=+akJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com