
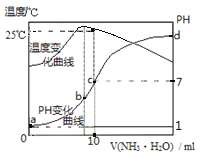
【题目】在某温度时,将nmol/L的氨水滴入10mL0.1mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
A.a点KW=1.0×10-14
B.水的电离程度:b>c>a>d
C.b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.25℃时,一水合氨的电离平衡常数为10-7/(10n-1)(用n表示)
【答案】D
【解析】
A、水的离子积与温度有关,a点时溶液温度小于25度,则水的离子积KW小于1.0×10-14,错误,不选A;
B、b点溶液温度最高,说明此时两溶液恰好反应生成氯化铵,铵根离子水解促进水的电离,则ad两点后抑制了水的电离,则b点水的电离程度最大,由于d点混合溶液的pH未知,则无法判断ad两点的水的电离程度,错误,不选B;
C、b点时溶液显酸性,则氢离子浓度大于氢氧根离子浓度,根据电荷守恒可知,氯离子浓度大于铵根离子浓度,溶液中的离子浓度顺序为:c(Cl-)>c(NH4+)> c(H+)>c(OH-),所以错误,不选C;
D、根据图像可知,25度时溶液的pH=7,则c(H+)=c(OH-)=10-7mol/L,铵根离子浓度为0.05mol/L,一水合氨的浓度为0.5n-0.05mol/L,则一水合氨的电离平衡常数= c(NH4+) c(OH-)/ c(NH3·H2O)= 0.05×10-7/(0.5n-0.05)=10-7/(10n-1)正确;
答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某同学用标准NaOH溶液来测定未知浓度的盐酸的浓度:
(1)先配制250mL 0.5mol/L的NaOH标准溶液所需的称量的质量NaOH为________ g,
需要的主要玻璃仪器有玻璃棒、量烧杯、胶头滴管、量筒和___________。
(2)用滴定管准确量取20.00mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点。在锥形瓶的待测液中滴加2~3滴酚酞试液,并开始滴定。
手眼:左手控制滴定管活塞,右手摇动锥形瓶,眼睛____________;
滴速:先快后慢,当接近终点时,应一滴一摇。滴定终点的判断:___________,即到终点,读出体积并记录数据。
(3)该同学进行了三次实验,实验数据如下表:
实验编号 | 盐酸的体积(mL) | 标准NaOH溶液的体积(mL) |
① | 均是20.00 | 16.90 |
② | 17.10 | |
③ | 18.20 |
滴定中误差较大的是第______次实验。造成这种误差的可能原因是__________(填选项编号)
a.滴定管在盛装标准NaOH溶液前未润洗
b.在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
c.达到滴定终点时,俯视溶液凹液面最低点读数
d.滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f.滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
(4)该同学所测得盐酸的物质的量浓度为_________。(结果保留三位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO2(红棕色)![]() N2O4(无色)△H<0.将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )
N2O4(无色)△H<0.将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )
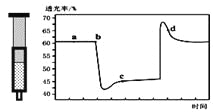
A. b点的操作是压缩注射器
B. c点与a点相比,c(NO2)增大,c(N2O4)减小
C. d 点:v(正)>v(逆)
D. 若不忽略体系温度变化,且没有能量损失,则T(b)>T(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理锂电池废料以节约资源、保护环境。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示:
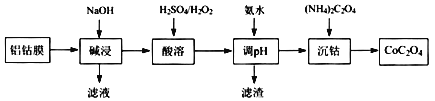
回答下列问题:
(l) Li元素在元素周期表中的位置为____________,LiCoO2中Co的化合价是____。
(2)“碱浸”时Al溶解的离子方程式为________。
(3)“酸溶”时加入H2O2的目的是____,调节pH后所得滤渣主要为____。
(4)“沉钴”的离子方程式为________。
(5)配制100 mL l.0 mol/L (NH4)2C2O4溶液,需要的玻璃仪器除玻璃棒、烧杯外,还需要_________。
(6)取CoC2O4固体4.41 g在空气中加热至300℃,得到钴的氧化物2.41 g,则该反应的化学方程式为 _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

图1 图2 图3 图4
A. 图1表示0.1molMgCl2·6H2O在空气中充分加热时固体质量随时间的变化
B. 图2表示用0.1000 mol·LˉlNaOH溶液滴定25.00 mLCH3COOH的滴定曲线,则c(CH3COOH)=0.0800 mol·Lˉ1
C. 图3表示恒温恒容条件下,2NO2(g)![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
D. 图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则常温下,NaA溶液的pH小于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家对一碳化学进行了广泛深入的研究并取得了一些重要成果。
(1)已知:CO(g)+2H2(g) ![]() CH3OH(g) △H1=-90.0kJ/mol;
CH3OH(g) △H1=-90.0kJ/mol;
3CH3OH(g) ![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol
CO与H2合成CH3CH=CH2的热化学方程式为________。
(2)甲醇(CH3OH)可作为新型汽车动力燃料,工业上可由CO与 H2在催化剂作用下合成甲醇。现向体积为2L的恒容绝热密闭容器中,充入1molCO 和2mo1H2发生反应:CO(g)+2H2(g) ![]() CH3OH(g) △H1=-90.0kJ/mol。当反应进行到5min时达到平衡状态,此时CH3OH的物质的量为0.6mol,则
CH3OH(g) △H1=-90.0kJ/mol。当反应进行到5min时达到平衡状态,此时CH3OH的物质的量为0.6mol,则
①5 min内反应的平均速率ν(H2) = _____ mol/(L·min)。
②达到平衡时放出的热量为________ kJ
③不能说明该反应已达到平衡状态的是____(选填字母标号)
a.CO的物质的量不再改变 b.容器内温度保持不变
c.CH3OH的消耗速率与生成速率相等 d.容器内的密度保持不变
(3)一种甲醇燃料电池如图,使用的电解质溶液是2mol·L-1的KOH溶液。
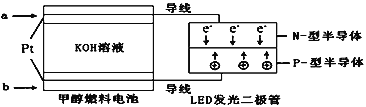
请写出加入(通入)a物质一极的电极反应式_____;每消耗9.6g甲醇转移的电子数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或对实验事实的叙述中存在错误的是 ( )
A.用50mL酸式滴定管准确量取23.20mL酸性KMnO4溶液,放入锥形瓶中待用
B.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
C.酸碱中和滴定时,锥形瓶未用待装液润洗。
D.用惰性电极电解NaCl溶液,一段时间后,再加盐酸,可使溶液与原溶液完全一样。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是

A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B.元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于P区
C.HF晶体沸点高于HCl,是因为 HCl共价键键能小于HF
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.常温下,l mol C6H12中含碳碳键的数目一定小于6NA
B.18g果糖分子中含羟基数目为0.6NA
C.4.0g由H218O与D216O组成的混合物中所含中子数为2NA
D.50g质量分数为46%的乙醇溶液与足量的钠反应,放出H2的分子数目为0.25NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com