
【题目】同温、同压下,若A容器中充满O2,B容器中充满O3。
(1)若所含分子总数相等,则A容器和B容器的容积之比是_______________________。
(2)若两容器中所含原子总数相等,则A容器和B容器的容积比是___________________________。
(3)若两容器的体积比为3∶2,则O2和O3物质的量之比为________________,质量之比为_____________,密度之比为___________________。
【答案】1∶1 3∶2 3∶2 1∶1 2∶3
【解析】
n=![]() =
=![]() 分析解答(1)和(2);
分析解答(1)和(2);
(3)根据n=![]() 计算物质的量,根据m=nM计算质量,根据ρ=
计算物质的量,根据m=nM计算质量,根据ρ=![]() 计算密度。
计算密度。
(1)同温同压下,气体的Vm相等,根据n=![]() =
=![]() 可知:气体的分子数之比等于气体的体积之比,若所含分子总数相等,则A容器和B容器的容积之比为1∶1,故答案为:1∶1;
可知:气体的分子数之比等于气体的体积之比,若所含分子总数相等,则A容器和B容器的容积之比为1∶1,故答案为:1∶1;
(2)若两容器中所含原子总数相等,则根据分子组成可知,两容器中的分子数之比等于3∶2,根据n=![]() =
=![]() 可知:气体的体积之比等于气体的分子数之比=3:2,故答案为:3∶2;
可知:气体的体积之比等于气体的分子数之比=3:2,故答案为:3∶2;
(3)若两容器的体积比为3∶2,根据n=![]() 可知O2和O3物质的量之比为3∶2,质量之比为3mol×32g/mol∶2mol×48g/mol=1∶1,根据ρ=
可知O2和O3物质的量之比为3∶2,质量之比为3mol×32g/mol∶2mol×48g/mol=1∶1,根据ρ=![]() ,密度之比为
,密度之比为![]() ∶
∶![]() =2∶3,故答案为:3∶2;1∶1;2∶3。
=2∶3,故答案为:3∶2;1∶1;2∶3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】36.5gHCl溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,NA表示阿伏加德罗常数的值,则下列叙述中正确的是( )
A. 所得溶液的物质的量浓度:c=1mol/LB. 所得溶液中含有NA个HCl分子
C. 36.5gHCl气体占有的体积为22.4LD. 所得溶液的质量分数w=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )

A. 用a趁热过滤提纯苯甲酸B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯D. 用d分离硝基苯与水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.质量数是将原子核内所有的质子和中子的相对质量取整数值之和
B.![]() X表示一种X元素的一种原子,中子数为A-Z
X表示一种X元素的一种原子,中子数为A-Z
C.![]() X中,A为该原子的相对原子质量的近似值
X中,A为该原子的相对原子质量的近似值
D.原子都是质子和中子、电子组成,原子不带电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无论是干重还是鲜重,组成水生动物、人体细胞的元素中含量最多的四种元素是
A.O、N、H、CaB.O、Ca、P、Mg
C.C、O、N、HD.C、Fe、Ca、P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用于分离或提纯物质的方法有:过滤、蒸发结晶、蒸馏、萃取、分液、洗气。根据需求填下列装置的序号:
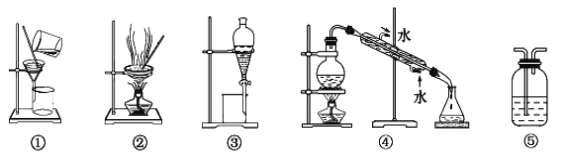
(1)分离Na2CO3溶液和CCl4,选_____(填序号),操作名称为________。
(2)用氢氧化钠溶液吸收O2中混有的杂质Cl2,选_______,操作名称为________。
(3)除去澄清石灰水中悬浮的CaCO3颗粒选______,操作名称为__________。
(4)制取蒸馏水,选________,操作名称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表中评价合理的是( )
选项 | 化学反应及其离子方程式 | 评价 |
A | NaHSO4溶液与Ba(OH)2溶液反应至SO42-沉淀完全:2H++ SO42-+Ba2++2OH==BaSO4↓+2H2O | 正确 |
B | 向碳酸镁浊液中加入足量稀盐酸:CO32- +2H+ | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O==Fe(OH)3↓+3H+ | 正确 |
D | 碳酸氢钠与足量澄清石灰水反应:2HCO3-+Ca2++2OH-==CaCO3↓+CO32-+2H2O | 正确 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨水、胆矾都是中学实验室中常见的化学试剂,它们在工农业生产上也都有广泛应用。某研究性学习小组为测定氨水的浓度,并用氨水作为提纯胆矾时的试剂,根据所查阅资料设计实验如下:
查阅资料:
①甲基橙的变色范围:pH<3.1红色,pH=3.1~4.4橙色, pH>4.4黄色
②酚酞的变色范围:pH<8.2无色 ,pH=8.2~10.0粉红色,pH>10.0红色
③已知:Fe3+、Fe2+、Cu2+转化为氢氧化物时相应的pH如下表:
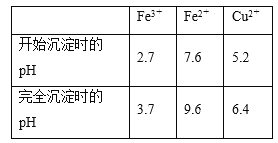
实验一 标定氨水的浓度
取25.00mL约为0.10 mol·L-1氨水于锥形瓶中,用0.1000 mol·L-1盐酸进行滴定,实验所得数据如下表所示:
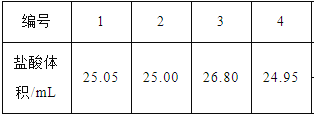
(1)滴定产物水解的离子方程式为____________________________________,由此可推知选择的滴定指示剂应为__________________。(填“甲基橙”或“酚酞”)
(2)该氨水的准确浓度为____________________mol·L-1。(精确到小数点后四位)
(3)编号3中溶液的离子浓度由大到小的顺序为__________________________________。
实验二 提纯胆矾晶体
某学习小组同学拟从含FeSO4、Fe2(SO4)3杂质的CuSO4溶液中提纯胆矾,其主要实验步骤如下:
第一步 往混合液中加入3% H2O2溶液充分反应后,再加入稀氨水调节溶液pH,过滤。
第二步 往滤液中加入稀硫酸调节溶液pH至1~2,提纯胆矾。
(4)加入3% H2O2溶液的作用是___________________________。
(5)加稀氨水调节pH应调至范围___________________________。
(6)下列物质可用来替代稀氨水的是___________________________。(填序号)
A.NaOH B.Cu(OH)2 C.CuO D.NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属的冶炼方法中,属于热还原法的是( )
A. 2Ag2O![]() 4Ag+O2↑B. Fe+CuSO4===FeSO4+Cu
4Ag+O2↑B. Fe+CuSO4===FeSO4+Cu
C. Fe2O3+3CO![]() 2Fe+3CO2D. MgCl2(熔融)
2Fe+3CO2D. MgCl2(熔融) ![]() Mg+Cl2↑
Mg+Cl2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com