
【题目】(1)某小组拟用酸性KMnO4溶液与H2C2O4溶液的反应(此反应为放热反应)来探究“条件对化学反应速率的影响,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。
限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、MnSO4、蒸馏水、试管、量筒、秒表、恒温水浴槽。
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L酸性KMnO4溶液)/mL | m(MnSO4)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.5 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题:
①写出上述反应的离子方程式:________________________。
②上述实验①②是探究____________对化学反应速率的影响;上述实验②④是探究____________对化学反应速率
影响。若上述实验②③是探究浓度对化学反应速率的影响,则a为______________;表格中的“乙”填写t/s,其测量的是______________________。
③实验①中对“乙”重复测量三次,所得数值分别13.6,13.5,13.4。忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=___________ 。
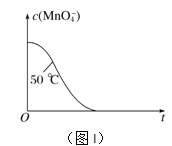
④已知实验①50℃时c(MnO![]() )~反应时间t的变化曲线如图I。若保持其他条件不变,请在坐标图中,画出实验②25℃时c(MnO
)~反应时间t的变化曲线如图I。若保持其他条件不变,请在坐标图中,画出实验②25℃时c(MnO![]() )~t的变化曲线示意图。______________
)~t的变化曲线示意图。______________
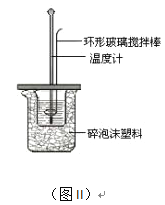
(2)测定中和热的实验装置如图II所示。
①写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式_______________________(中和热数值为57.3 kJ/mol):
②取60mL0.50mol/L NaOH溶液和50mL0.50mol/L硫酸溶液进行实验,实验数据如下表。
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.9 | |
2 | 26.2 | 26.4 | 26.3 | 30.6 | |
3 | 25.9 | 25.9 | 25.9 | 29.5 | |
4 | 26.4 | 26.2 | 26.3 | 30.0 | |
近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H=________________________kJ/mol(列出计算式)。
③能引起中和热偏高的原因是(填字母)__________。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.用50mL0.50mol/L醋酸代替了硫酸进行反应,
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
E. 量取硫酸溶液的体积时仰视读数
【答案】 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 温度 催化剂 0.5 溶液褪色所需时间 5.0×10-4 mol·L-1·s-1 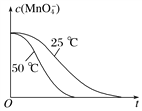 1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l) △H=-57.3kJ/mol 或H2SO4(aq)+2NaOH(aq)= Na2SO4(aq)+2H2O(l) △H=-114.6kJ/mol
1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l) △H=-57.3kJ/mol 或H2SO4(aq)+2NaOH(aq)= Na2SO4(aq)+2H2O(l) △H=-114.6kJ/mol 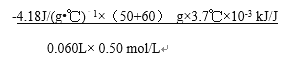 A
A
【解析】试题分析:(1)MnO4-被H2C2O4还原为Mn2+,H2C2O4被氧化为CO2气体;②实验①②的变量是温度;实验④比实验②多加0.1g催化剂 MnSO4;实验②③是探究H2C2O4溶液浓度对化学反应速率的影响,应控制KMnO4的浓度相同;要计算反应速率,需测量高锰酸钾溶液褪色所需时间;③根据![]() 计算v(KMnO4);④实验②的反应温度比实验①低,所以反应速率慢,褪色消耗时间多;(2)①中和热是生成1mol水放出的热量;②第2次实验数据明显偏离正常的误差范围,根据1、3、4三次实验数据计算平均温度差,根据Q=mc△T计算60mL0.50mol/L NaOH溶液和50mL0.50mol/L硫酸溶液反应放出的热量;③中和热是强酸和强碱反应生成1mol水时放出的热量,依据Q=Q=mc△T来逐项分析。
计算v(KMnO4);④实验②的反应温度比实验①低,所以反应速率慢,褪色消耗时间多;(2)①中和热是生成1mol水放出的热量;②第2次实验数据明显偏离正常的误差范围,根据1、3、4三次实验数据计算平均温度差,根据Q=mc△T计算60mL0.50mol/L NaOH溶液和50mL0.50mol/L硫酸溶液反应放出的热量;③中和热是强酸和强碱反应生成1mol水时放出的热量,依据Q=Q=mc△T来逐项分析。
解析:(1)MnO4-被H2C2O4还原为Mn2+,H2C2O4被氧化为CO2气体,反应的离子方程式是2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;②实验①②的变量是温度,所以实验①②是探究温度对化学反应速率的影响;实验④比实验②多加0.1g催化剂 MnSO4,所以实验②④是探究催化剂对化学反应速率影响;实验②③是探究H2C2O4溶液浓度对化学反应速率的影响,应控制KMnO4的浓度相同,所以需要加入0.5mL蒸馏水,故a=0.5;要计算反应速率,需测量高锰酸钾溶液褪色所需时间;③三次实验平均用时13.5s;④实验②的反应温度比实验①低,所以反应速率慢,褪色消耗时间多,所以图像是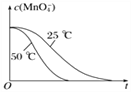 ;
;
(2)①中和热是生成1mol水放出的热量,稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式是H2SO4(aq)+2NaOH(aq)= Na2SO4(aq)+2H2O(l) △H=-114.6kJ/mol;②第2次实验明显偏离正常的误差范围,根据1、3、4三次实验数据,平均温度升高3.7℃,根据Q=mc△T,60mL0.50mol/L NaOH溶液和50mL0.50mol/L硫酸溶液反应放出的热量是(50+60)g![]() 4.18 J/(g·℃)
4.18 J/(g·℃) ![]() 3.7℃
3.7℃![]() kJ /J,60mL0.50mol/L NaOH溶液和50mL0.50mol/L硫酸溶液反应生成水的物质的量是0.06L
kJ /J,60mL0.50mol/L NaOH溶液和50mL0.50mol/L硫酸溶液反应生成水的物质的量是0.06L![]() 0.5mol/L,则△H=
0.5mol/L,则△H= 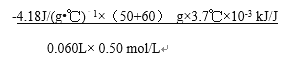 ;③A.实验装置保温、隔热效果差,测得中和热偏小,故A错误;B.量取NaOH溶液的体积时仰视读数,量取的氢氧化钠偏多,生成水的物质的量多,所以放出热量多,测得中和热数值偏大,故B正确;
;③A.实验装置保温、隔热效果差,测得中和热偏小,故A错误;B.量取NaOH溶液的体积时仰视读数,量取的氢氧化钠偏多,生成水的物质的量多,所以放出热量多,测得中和热数值偏大,故B正确;
C.用50mL0.50mol/L醋酸代替了硫酸进行反应,醋酸是弱酸,醋酸的电离是吸热的过程,所以导致实验测得中和热的数值偏小,故C错误;D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,会发生酸和碱的中和,温度计示数变化值减小,所以导致实验测得中和热的数值偏小,故D错误。E.由于硫酸本身就过量,量硫酸溶液的体积时仰视读数,生成水的物质的量不变,放热不变,实验测得中和热的数值无影响,故E错误。


科目:高中化学 来源: 题型:
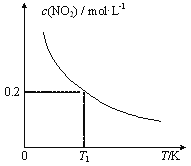
【题目】在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)![]() 2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
A. 该反应的ΔH<0
B. T1时,该反应的平衡常数为![]()
C. 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比小于1:2
D. 若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数小于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列有关该同学对实验原理的解释和所得结论的叙述不正确的是( )
A. 氧化性:ClO->I2>SO42—
B. 蓝色消失的原因是Na2SO3溶液具有漂白性
C. 淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2使淀粉变蓝
D. 若将Na2SO3溶液加入氯水中,氯水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用BaS的还原性提纯HBr溶液,并制取溴化镁的方案如下:
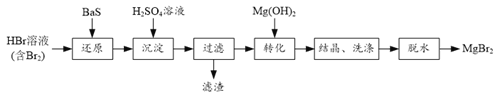
(1) “还原”步骤中BaS不宜过量太多的原因是______。
(2)滤渣的成分是______。
(3)结晶获得的MgBr2·6H2O用乙醇洗涤,从洗涤液中回收乙醇的实验方法是______。
(4)利用如图装置将MgBr2·6H2O脱水得到MgBr2。
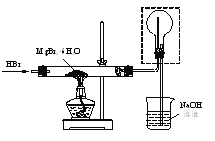
①通入HBr的目的是______。
②图中框内装置的作用是______。
(5)已知:BaS+H2O2=Ba(OH)2+S↓。请补充完整实验室由BaS制取高纯BaSO3的实验方案:取BaS加水浸出,边搅拌边在浸出液中加入过量H2O2,过滤,______,(实验中须使用的试剂有:SO2气体,溶有SO2的水,除常用仪器外须使用的仪器有:真空干燥箱、pH计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中不正确的是

A. 1mol NH4+ 所含的质子总数为10NA
B. 联氨(N2H4)中含有极性键和非极性键
C. 过程II属于氧化反应,过程IV属于还原反应
D. 过程I中,参与反应的NH4+与NH2OH的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量转化的认识不正确的是( )
A.通过植物的光合作用,太阳能转化为化学能
B.人类使用照明设备,将电能转化为光能
C.生物体内的化学变化过程,在能量转化上比在体外发生的一些能量转化更为合理有效
D.燃料燃烧,只是将化学能转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答问题。
C(g)+D(g)过程中的能量变化如图所示,回答问题。
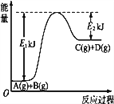
该反应是____(填“吸热”或“放热”)反应,该反应的ΔH=_____ kJ· mol-1(用含E1、E2的代数式表示)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l) =H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式___________________________。
(3)已知:H2(g)+Cl2(g)==2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为______kJ。
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)![]() 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示AE五种物质间的相互转化关系,其中A为淡黄色固体,B为单质。试推出各物质的化学式,并写出B→C、C→D、D→E反应的化学方程式。
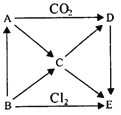
(1)写出B→C、C→D、D→E反应的化学方程式:
B→C:_______________;
C→D:_______________;
D→E:_______________;
(2)将3.9 gA投入到足量的水中充分反应,生成的气体在标准状况下的体积为_____L,将反应后的溶液配成1000mL溶液,所得溶液的物质的避浓度为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com