
【题目】下图是部分短周期元素的单质及化合物(或溶液)的转化关系:
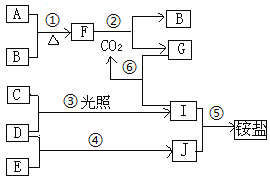
已知B、C、D、E是非金属单质,且在常温下都是气体;化合物G的焰色反应为黄色,化合物I、J通常状况下呈气态;反应④是化工生产中的一种重要固氮反应。请回答下列问题:
(1)写出A、B元素在周期表中的位置:A__________________ B__________________
(2)①~⑥反应中属于氧化还原反应的是 ___________________________________(填序号)
(3)写出②的化学方程式: _____________________________
⑥的离子方程式:______________________________________
(4)反应⑤的现象是________,J的另一种检验方法及现象是_______________。
【答案】 第三周期第ⅠA族 第二周期第ⅥA族 ①②③④ 2Na2O2 + 2CO2 = 2Na2CO3 + O2 CO32—+ 2H+ = CO2 ↑+H2O 产生白烟 用湿润的红色石蕊试纸检验,试纸变蓝色,证明是氨气
【解析】反应①是化工生产中的一种重要固氮反应,证明是氮气和氢气合成氨的反应,判断J为NH3,化合物I和J通常状况下呈气态,CD是非金属单质,依据反应条件是光照,推断为氢气和氯气生成氯化氢的反应,判断D为H2,E为N2,C为Cl2,I为HCl,J为NH3;化合物G的焰色反应为黄色说明含钠元素,G与HCl反应生成CO2,说明G为Na2CO3,气体单质B和A反应生成的F可以与二氧化碳反应生成碳酸钠和气体B单质,说明F中 含有钠元素,证明A为金属钠,推断B为O2,F为Na2O2。
(1)A为钠,在周期表中位于第三周期第ⅠA族,B为O,在周期表中位于第二周期第ⅥA族,故答案为:第三周期第ⅠA族;第二周期第ⅥA族;
(2)反应①为钠与氧气的反应,属于氧化还原反应,反应②为过氧化钠与二氧化碳的反应,属于氧化还原反应,反应③为氯气与氢气的反应,属于氧化还原反应,反应④为氢气与氮气的反应,属于氧化还原反应,反应⑤为氯化氢和氨气的反应,属于非氧化还原反应,反应⑥为碳酸钠与盐酸的反应,属于非氧化还原反应,其中属于氧化还原反应的有①②③④,故答案为:①②③④;
(3)反应②的化学方程式为2Na2O2 + 2CO2 = 2Na2CO3 + O2,故答案为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;反应⑥的离子方程式为CO32—+ 2H+ = CO2 ↑+H2O,故答案为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;CO32—+ 2H+ = CO2 ↑+H2O;
(4)反应⑤为氯化氢与氨气的反应,现象为产生白烟,检验氨气的方法及现象为用湿润的红色石蕊试纸检验,试纸变蓝色,证明是氨气,故答案为:产生白烟;用湿润的红色石蕊试纸检验,试纸变蓝色,证明是氨气。


科目:高中化学 来源: 题型:
【题目】下列有关生物体内水和无机盐的叙述正确的是( )
A. 不同种生物细胞的自由水和结合水的比值相同,它们的代谢强度也相同
B. 癌变细胞和衰老细胞内的水分减少,新陈代谢速率减慢
C. 给水中毒患者注射质量分数为1.8%的盐水,是为了降低细胞外液的渗透压
D. 血浆pH能维持相对稳定,与它含有的HCO、HPO等离子有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中有取之不尽的化学资源,从海水中可提取多种化工原料。下图是某工厂对海水资源的综合利用的示意图。

试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO![]() 等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
①粗盐溶液中加入过量的Na2CO3溶液:____________________;_____________________。
②滤液中加入盐酸至溶液呈中性:________________________;_______________________。
(2) 母液中含有K+、Na+、Mg2+等阳离子,从以上流程可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是_____________________;若加入石灰乳后所制取的产品中还混杂着熟石灰,那么将熟石灰从该产品中除去的方法是________________________。
②电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气的冷却剂的是________(填字母序号)。
A.H2 B.CO2 C.O2 D.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新的母液中加入一种常见的气态氧化剂,又抽取了重要的化工原料溴单质。
①生成溴单质的化学反应的离子方程式是___________________________________;生产中利用溴单质的挥发性将溴单质从化合物中分离出来的方法是________________________。
②以下是对生产溴单质所用的气态氧化剂寻找供货源的设想,其中合理的是_________(填字母序号)。
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环
③从多种经营、综合开发、打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A.室温下,测得氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C.用碳酸氢钠溶液检验水杨酸中的羧基:
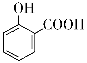 +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D.用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中正确的是( )
A.NaHCO3=Na++HCO3- B.Na2SO4=2Na++SO4-2
C.Ca(NO3)2=Ca2++2(NO3)2- D.KClO3=K++Cl-+3O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g) ![]() A2(g)+B2(g)达到平衡状态的标志是 ( )
A2(g)+B2(g)达到平衡状态的标志是 ( )
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示。判断下列说法中,正确的是( )
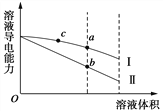
A. 两溶液稀释前的浓度相同
B. a、b、c三点溶液的pH由大到小顺序为a>b>c
C. a点的KW值比b点的KW值大
D. a点水电离的c(H+)大于c点水电离的c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com