
【题目】下列各组物质属于同分异构体是___;属于同素异形体是___;属于同位素是___;属于同一种物质是___。(写序号)
①红磷与白磷 ②12C与14C ③干冰与二氧化碳 ④CH4与CH3CH3 ⑤S2与S8 ⑥235U与238U ⑦![]() 与
与![]() ⑧乙醇(
⑧乙醇( )与二甲醚(
)与二甲醚(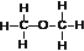 ) ⑨
) ⑨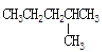 和
和![]() ⑩氰酸铵(NH4CNO)与尿素[CO(NH2)2]
⑩氰酸铵(NH4CNO)与尿素[CO(NH2)2]
科目:高中化学 来源: 题型:
【题目】如图当线路接通时,发现M(用石蕊试液浸润过的滤纸)a端显蓝色,b端显红色,且知甲中电极材料是锌、银,乙中电极材料是铂。回答:
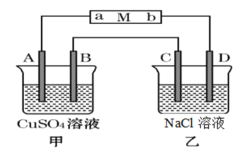
(1)甲、乙分别是什么装置_____________、______________。
(2)A电极材料为_____________,B电极上的电极反应为:______________。
(3)请解释a处变蓝的原因:________________
(4)已知乙中溶液体积为100 mL,当B上析出0.32 g红色物质时,此时乙中溶液的pH=__________(不考虑溶液体积的变化,温度为室温)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种金属组成的合金A,在合适的条件下可按下图进行反应(部分产物和水省略),已知F为红褐色沉淀,请回答:
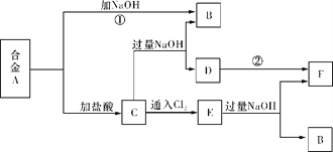
(1)溶液C的溶质主要是____________________(填化学式)。
(2)写出反应②的化学方程式_______________________________________________。描述D变F的实验现象_______________________________________________。
(3)写出反应C→E的离子方程式________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红色固体X由两种元素组成,为探究其组成和性质,设计了如下实验:

请回答:
(1)气体Y的一种同素异形体的分子式是______,红褐色沉淀的化学式______。
(2)X在隔绝空气条件下受高温分解为Y和Z的化学方程式____________。
(3)取黄色溶液W滴加在淀粉KI试纸上,试纸变蓝色,用离子方程式表示试纸变蓝的原因____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法不正确的是( )
A.C60与金刚石互为同素异形体
B.氢键属于化学键
C.金属元素和非金属元素形成的化合物在熔融状态下一定能导电
D.“NH4Cl”的意义是指氯化铵晶体由NH4+和Cl-构成,阴、阳离子个数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯容易发生聚合生成二聚体,该反应为:![]() 。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是( )
。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是( )

A.T1>T2
B.a点的正反应速率小于b点的逆反应速率
C.a点的反应速率小于c点的反应速率
D.反应开始至b点时,双环戊二烯平均速率约为:0.45molL-1h-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某结晶水合物含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的三种离子,实验小组为确定其化学式做了如下实验:
中的三种离子,实验小组为确定其化学式做了如下实验:
![]() 准确称取
准确称取![]() 样品,配制成
样品,配制成![]() 溶液X。
溶液X。
![]() 取
取![]() 溶液X,加入足量盐酸,无明显现象;再加足量
溶液X,加入足量盐酸,无明显现象;再加足量![]() 溶液,产生白色沉淀;将沉淀过滤、洗涤、干燥至恒重,得白色固体
溶液,产生白色沉淀;将沉淀过滤、洗涤、干燥至恒重,得白色固体![]() 。
。
![]() 取
取![]() 溶液X,加入适量稀硫酸酸化后,用
溶液X,加入适量稀硫酸酸化后,用![]() 溶液滴定至终点,重复滴定三次,测得消耗
溶液滴定至终点,重复滴定三次,测得消耗![]() 溶液体积的平均值为
溶液体积的平均值为![]() 。
。
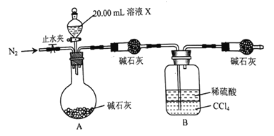
![]() 设计如图所示的装置,取
设计如图所示的装置,取![]() 溶液Ⅹ进行实验,实验前后B装置增重
溶液Ⅹ进行实验,实验前后B装置增重![]() 。
。
![]() 取少量溶液X,滴加
取少量溶液X,滴加![]() 溶液无明显现象,再向其中滴加
溶液无明显现象,再向其中滴加![]() 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
回答下列问题;
![]() 完成实验
完成实验![]() 所需要的玻璃仪器有;烧杯、玻璃棒、量筒、____________。
所需要的玻璃仪器有;烧杯、玻璃棒、量筒、____________。
![]() 实验
实验![]() 达到滴定终点的现象是_____________________。
达到滴定终点的现象是_____________________。
![]() 实验
实验![]() 的反应结束后,打开止水夹通入
的反应结束后,打开止水夹通入![]() 的作用是________________。
的作用是________________。
![]() 根据以上实验数据计算该结晶水合物的化学式为______________。
根据以上实验数据计算该结晶水合物的化学式为______________。
![]() 某同学查阅资料发现 AgSCN为白色难溶物,
某同学查阅资料发现 AgSCN为白色难溶物,![]() 可以氧化
可以氧化![]() 和
和![]() 。为探究
。为探究![]() 和
和![]() 的还原性强弱,该同学设计了如图实验装置并进行下列实验。
的还原性强弱,该同学设计了如图实验装置并进行下列实验。
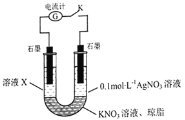
先断开电键K,向溶液X中滴加![]() 溶液,无明显现象,说明_____________;闭合电键K后,若观察到的实验现象有溶液X逐渐变红、右边石墨电极上有固体析出、电流计指针偏转,据此得出的结论是_____________,溶液变红的原因是___________
溶液,无明显现象,说明_____________;闭合电键K后,若观察到的实验现象有溶液X逐渐变红、右边石墨电极上有固体析出、电流计指针偏转,据此得出的结论是_____________,溶液变红的原因是___________![]() 用离子方程式表示
用离子方程式表示![]() ,该实验设计的优点是_______________。
,该实验设计的优点是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)![]() 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
②2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1
③H+(aq)+OH-(aq)![]() H2O(l) ΔH=-57.3 kJ·mol-1
H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
A. H2(g)的燃烧热为142.9 kJ·mol-1
B. 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C. 1/2H2SO4(aq)+1/2Ba(OH)2(aq)![]() 1/2BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
1/2BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D. 3H2(g)+CO2(g)![]() CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1
CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2O(g)===2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1 ②H2S(g)===H2(g)+S(g) ΔH=+20.1 kJ·mol-1下列判断正确的是( )
A. 氢气的燃烧热:ΔH=-241.8 kJ·mol-1
B. 相同条件下,充分燃烧1 mol H2(g)与1 mol S(g)的混合物比充分燃烧1 mol H2S(g)放热多20.1 kJ
C. 由①②知,水的热稳定性小于硫化氢
D. ②中若生成固态硫,ΔH将增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com