
【题目】下面的键线式表示维生素A的分子结构:
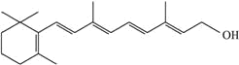
(1)维生素A分子式是_____。
(2)维生素A中氧的质量分数是____。
(3)维生素A的分子结构中含氧官能团的电子式是_____。
(4)关于维生素A的说法正确的是_____(填编号)。
①是一种酚
②属于芳香族化合物
③能与NaOH溶液反应
④能使溴水褪色
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗进行综合利用,不仅可以提高经济效益,而且还能防止环境污染。现按下列方式进行综合利用,回答问题。
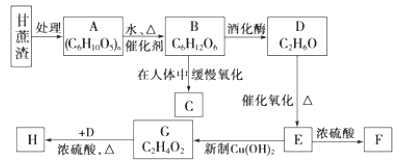
已知F、H均是具有香味的液体,F为E的三聚合物,并具有特殊的6元环状对称结构。
(1)A的名称_______________;H的名称______________;
(2)D→E的化学反应方程式______________________________;
(3)G→H的化学反应方程式_______________________________;
(4)E→ G的反应类型________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知异丙苯的结构简式如下![]() ,下列说法错误的是( )
,下列说法错误的是( )
A.异丙苯的分子式为C9H12
B.异丙苯的沸点比苯高
C.异丙苯的和苯互为同系物
D.异丙苯分子中一定共线的碳原子数为4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解可得烃D,其产量是一个国家石油化工发展水平的标志,已知D在标准状况下的密度为1.25 g·Lˉ1。有机物B可利用植物秸秆来生产,E为有香味的油状液体,它们之间的转化关系如图,请回答:

(1)C中所含官能团名称是____。
(2)写出反应④的化学方程式____。
(3)C与D在一定条件下可发生加成反应,生成具有酸性的物质F。F的结构简式为___。
(4)下列说法正确的是____。(填编号)
A.有机物E与F互为同分异构体
B.用新制氢氧化铜悬浊液无法区分有机物B和C
C.有机物A、D均能被酸性高锰酸钾溶液氧化
D.可用饱和NaOH溶液除去有机物E中混有的少量B、C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。
已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
该兴趣小组设计了下列实验装置,进行实验。请回答下列问题:
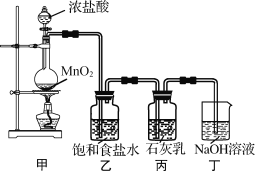
(1)①甲装置用于制备氯气,乙装置的作用是_________。
②实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法不正确的是__。(填字母)
A 若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5
B 若产物为NaClO、NaCl,则吸收后的溶液中n(NaClO)=n(NaCl)
C 若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,其可能原因是部分氯气未与石灰乳反应而逸出,以及温度升高。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢匀速地通入足量氯气,得出了Ca(ClO)2、Ca(ClO3)2两种物质的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。
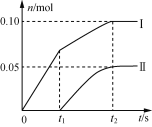
①图中曲线II表示____(填物质的化学式)的物质的量随反应时间变化的关系;
②所取石灰乳中含有Ca(OH)2的物质的量为____mol;
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA 表示阿伏加德罗常数的值)
A.71g Cl2 所含原子数为2NA
B.在常温常压下,22.4L 氦气含有分子数为NA
C.只有在标准状况下,14g氮气含有分子数才为0.5NA
D.在同温同压下,相同体积的任何气体单质所含原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知25℃、101 kPa时:
①2SO2(g)+O2(g)2SO3(g) ΔH1=-197 kJ/mol;
②H2O(g)=H2O(l) ΔH2=-44 kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式为__________。
(2)已知:温度过高时,WO2(s)转变为WO2(g):
①WO2(s)+2H2(g)W(s)+2H2O(g) ΔH1=+66.0 kJ·mol-1
②WO2(g)+2H2(g)W(s)+2H2O(g) ΔH2=-137.9 kJ·mol-1
则WO2(s)WO2(g)的ΔH=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO 和CO2 组成的混合气体18g ,充分燃烧后测得CO2 体积为11.2L (标准情况)。试计算:
(1)原混合气体中CO 的质量___;
(2)原混合气体中CO2 在标准状况下的体积___;
(3)原混合气体的平均摩尔质量___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以镍矿粉(主要成分为NiS,杂质FeS、CuS和SiO2等)为原料可制备NiCO3
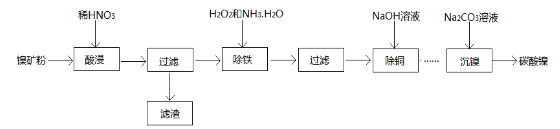
已知Ni和Fe为变价金属,常见化合价为+2价、+3价。
(1)在酸浸过程中,CuS与稀HNO3反应生成淡黄色固体,其离子方程式为___________________,滤渣的主要成分为________________________;
(2)在除FeS时,需加入过量的H2O2氧化,若用过强的氧化剂,其可能的后果是_______________;反应完全后,除去多余H2O2的简便方法是______________________;
(3)在“沉镍”工艺中,若将含Ni2+溶液缓慢加入至盛有Na2CO3溶液的反应容器中,可能会形成杂质,其原因是_______________________(用离子方程式表示)。检验碳酸镍沉淀完全的方法是__________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com