
【题目】锂离子电池己被广泛用作便携式电源。正极材料为LiCoO2、LiFePO4等,负极材料一般为石墨碳,以溶有LiPF6、LiBF4等的碳酸二乙酯(DEC)作电解液。
(1)Fe2+基态核外电子排布式为 ________。
(2)PO43-的空间构型为 ________ (用文字描述)。
(3)![]() 中
中![]() 的配位数为6,该配合物中的配位原子为 _____。
的配位数为6,该配合物中的配位原子为 _____。
(4)碳酸二乙酯(DEC)的分子结构如图所示,分子中碳原子的轨道杂化类型为_____,1mol碳酸二乙酯(DEC)中含有σ键的数目为_____。
![]()
(5)氮化锂是一种新型无机贮氢材料,其晶胞结构如图所示,该晶体的化学式为_______。
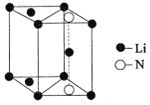
【答案】![]() 正四面体 N、Cl sp3、sp2 17NA Li3N
正四面体 N、Cl sp3、sp2 17NA Li3N
【解析】
(1)Fe2+原子核外有24个电子,依据核外电子排布规律, Fe2+基态核外电子排布式为![]() ,
,
故答案为:![]() ;
;
(2)P原子孤电子对数![]() ,价层电子对数
,价层电子对数![]() ,故PO43-的空间构型为正四面体,
,故PO43-的空间构型为正四面体,
故答案为:正四面体;
(3)![]() 中
中![]() 的配位数为6,则配体为Cl和NH3,配位原子为Cl、N,
的配位数为6,则配体为Cl和NH3,配位原子为Cl、N,
故答案为:N、Cl;
(4)根据碳酸二乙酯(DEC)的分子结构示意图可知,碳酸二乙酯中含有酯键,和甲基团,故碳原子的轨道杂化类型为sp3、sp2;碳酸二乙酯中含有17个σ键和一个π键,故1mol碳酸二乙酯(DEC)中含有σ键的数目为17NA,
故答案为:sp3、sp2;17NA;
(5)通过晶胞结构图可知Li原子数![]() ,N原子数
,N原子数![]() ,故化学式为Li3N,
,故化学式为Li3N,
故答案为:Li3N。


科目:高中化学 来源: 题型:
【题目】铅氧化还原液流电池是一种新型储能电池。该电池以酸性甲基磺酸铅溶液为电解液,简化的工作原理如图所示,下列说法正确的是
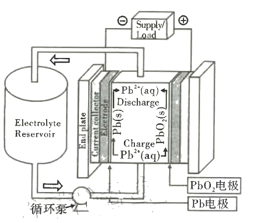
A.放电时,H+经过循环泵向Pb电极移动
B.放电时,负极反应式为Pb-2e- +SO42- = PbSO4
C.充电时,电解液中H+、Pb2+的物质的量浓度均减小
D.充电时,阳极反应式为Pb2+ +2H2O-2e- = PbO2 +4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如图装置,下列说法错误的是
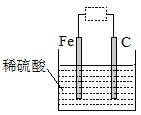
A.虚线框中接灵敏电流计,该装置可将化学能转化为电能
B.虚线框中无论是否接灵敏电流计,铁都要被腐蚀
C.虚线框中接直流电源,铁可能不易被腐蚀
D.虚线框中接灵敏电流计或接直流电源,铁都是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁基橡胶可用于制造汽车内胎,合成丁基橡胶的一种单体A的分子为C4H8,A氢化后得到2-甲基丙烷。完成下列填空:
(1)A分子中的官能团的名称为___。
(2)写出将A通入下列两种溶液后出现的现象。
A通入溴水:___,
A通入溴的四氯化碳溶液:___。
(3)写出A氢化后产物2-甲基丙烷的同分异构体的结构简式:___。
(4)A可以聚合,写出A的聚合反应___(以反应方程式表示)。
(5)A发生烷基化反应生成一种烃B,将B完全燃烧后得到CO2和H2O的物质的量之比为8:9,由此可以确定B的化学式为___。通过对B的结构深入研究,发现其一卤代物只有4种,且碳链不对称。写出B的结构简式,并用系统命名法命名:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBH4是一种常见的还原剂。一种以H2、Na、硼酸三甲酯[B(OCH3)3]为原料,生产NaBH4的工艺流程如下:
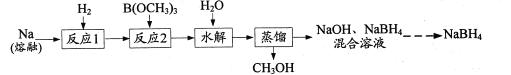
(1)下列措施能提高“反应1”的化学反应速率的有______(填字母)。
A.充分搅拌熔融钠
B.将熔融钠充分分散在石蜡油中
C.反应前排尽装置中的空气
(2)在浓硫酸作用下,B(OCH3)3可由B(OH)3和CH3OH发生酯化反应制得。浓H2SO4的作用是_____。
(3)“反应2”在240℃条件下进行,生成的产物是NaBH4和CH3ONa,写出该反应的化学方程式:____ 。“反应2”所用B(OCH3)3需充分干燥,原因是______。
(4)反应NaBH4+2H2O=NaBO2+4H2 可用于制取H2。一定浓度的NaBH4催化制氢的半衰期(溶液中NaBH4消耗一半时所需的时间)与溶液pH的关系如图所示:
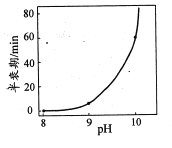
①NaBH4与水反应所得溶液呈碱性,原因是____。
②随着反应的进行,生成H2的速率逐渐减慢,原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8,下列说法不正确的是 ( )
A. 与W相邻的同主族元素可制成重要的半导体材料
B. X单质不可能置换出W单质
C. 元素原子半径从大到小的顺序是X、Y、Z
D. W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是制备乙酸乙酯的两种装置,下列说法错误的是
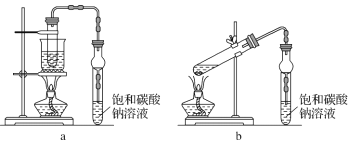
A.相比于 b,a装置具有副反应少、原料利用率高等优点
B.加入的浓硫酸要稍多于催化剂用量的原因是浓硫酸还起到吸水剂的作用,推动平衡正向进行
C.反应结束后,将收集到的产品倒入分液漏斗中,振荡、放气、静置、分液,然后从下口放出制备的产物
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度较小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求表示下列有机物:
(1)按系统命名法命名有机物![]() 的名称是 _________。
的名称是 _________。
(2) 4,4,5-三甲基-2-己炔(写出结构简式)_________________
(3) 对硝基苯乙烯(写出机构简式)__________________
(4) 2,2-二甲基-3-乙基-4-异丙基壬烷(写出结构简式)___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是( )
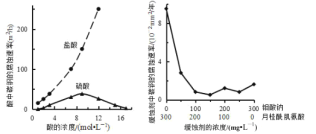
A.盐酸的浓度越大,腐蚀速率越快
B.钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小
C.碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比
D.对比盐酸和硫酸两条曲线,可知 Cl-也会影响碳素钢的腐蚀速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com