
【题目】碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症。制备反应2LaCl3+6NH4HCO3=La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化学兴趣小组利用下列装置模拟制备碳酸镧。
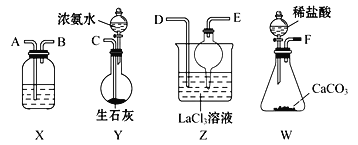
(1)盛放稀盐酸的仪器名称为________________。
(2)制备碳酸镧实验流程中导管从左向右的连接顺序为F→____→____→____→____→______。
(3)W中发生反应的离子方程式为_______Y中发生反应的化学反应方程式为__________
(4)X中盛放的试剂是_________,干燥管的作用为_________________。
(5)Z中通入气体的方式________
A.先通入足量NH3,后通入过量的CO2
B.先通入足量CO2,后通入过量的NH3
C.NH3和CO2同时通入
(6)该化学兴趣小组为探究La2(CO3)3和La(HCO3)3的稳定性强弱,设计了如下的实验装置,则甲试管中盛放的物质为________________,实验过程中,发现乙试管中固体质量与灼烧时间的关系曲线如图所示,则关于两种物质稳定性实验结论为_____。
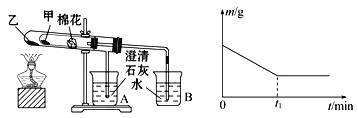
A.稳定性La2(CO3)3>La(HCO3)3
B.稳定性La2(CO3)3<La(HCO3)3
C.无法判断
【答案】分液漏斗 A B D E C CaCO3+2H+=Ca2++H2O+CO2 NH3·H2O+CaO=Ca(OH)2+NH3↑ 饱和NaHCO3溶液 防倒吸 A La(HCO3)3 C
【解析】
在W中用盐酸与CaCO3反应制取CO2气体,经过X装置除去CO2气体中的杂质HCl气体后通入Z装置在,与由Y装置制取得到的NH3在装置C中发生反应,制备La2(CO3)3沉淀;可根据NH3、CO2在水溶液中的溶解度大小确定气体通入的先后顺序。要确定La2(CO3)3、La(HCO3)3两种物质放入套管实验中的试管位置,先选择稳定强的直接加热,稳定性差的间接性加热;根据实验过程中乙试管中固体质量与灼烧时间的关系曲线图示,可证明乙试管中固体发生了分解反应,生成了CO2气体,据此分析两试管中的物质的稳定性。
(1)根据仪器结构可知盛装稀盐酸的仪器为分液漏斗;
(2)由装置可知,W中制备CO2气体,X除去CO2中的杂质HCl,Y中制备NH3,在Z中制备碳酸镧,则制备碳酸镧实验流程中导管从左向右的连接顺序为:F→A→B→D→E→C;
(3)W中稀HCl与CaCO3发生复分解反应制取CO2气体,反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑;Y中浓氨水与CaO发生反应制取NH3,反应的化学反应式为NH3·H2O+CaO=Ca(OH)2+NH3↑;
(4)X中盛放的试剂是NaHCO3溶液,其作用为吸收挥发的HCl、同时生成CO2;干燥管连接NH3的导气管C,由于氨气极容易溶于水,为防止倒吸现象的发生,连接干燥管,因此干燥管的作用是防止倒吸现象的发生;
(5)由于氨气在水中溶解度很大,Z中应先通入NH3,使溶液显碱性,然后通入过量的CO2,这样就可以溶解更多CO2气体,产生较大量的HCO3-,生成较大浓度的NH4HCO3,故合理选项是A;
(6)酸式碳酸盐稳定性较差,应直接加热,即甲试管中盛放的物质为La(HCO3)3,乙试管中盛放的物质为La2(CO3)3,乙试管中La2(CO3)3分解生成CO2,使最后得到的固体质量减轻,甲物质和乙物质受热都发生了分解反应,由于二者的温度不同,且都发生了反应,因此通过该套管实验不能确定二者稳定性大小,故合理选项是C。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨做电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A. 原混合溶液中c(K+)为2 mol·L-1
B. 上述电解过程中共转移6 mol电子
C. 电解得到的Cu的物质的量为0.5 mol
D. 电解后溶液中c(H+)为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述正确的是( )
A. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
B. 32 g S8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
C. 标准状况下,11.2 L Cl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA
D. 39g钾与氧气完全反应,生成K2O转移NA个电子,生成KO2转移2NA电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电导率用于衡量电解质溶液导电能力的大小,与离子浓度和离子迁移速率有关。图1 为相同电导率盐酸和醋酸溶液升温过程中电导率变化曲线,图2 为相同电导率氯化钠和醋酸钠溶液升温过程中电导率变化曲线,温度均由22℃上升到70℃。下列判断不正确的是
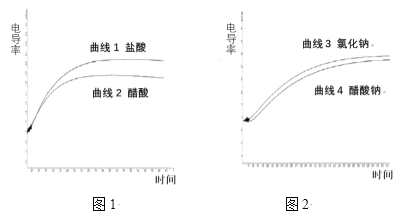
A. 由曲线1可以推测:温度升高可以提高离子的迁移速率
B. 由曲线4可以推测:温度升高,醋酸钠电导率变化与醋酸根的水解平衡移动有关
C. 由图1和图2可以判定:相同条件下,盐酸的电导率大于醋酸的电导率,可能的原因是Cl-的迁移速率大于CH3COO-的迁移速率
D. 由图1和图2可以判定:两图中电导率的差值不同,与溶液中H+、OH-的浓度和迁移速率无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①NaHCO3;②C2H5OH;③Cu;④H2O;⑤石灰乳;⑥CO;⑦Ba(OH)2;⑧盐酸;⑨H2CO3;⑩浓硝酸。
(1)属于电解质的是___(填写序号),属于非电解质的是___(填写序号)。
(2)⑨在水溶液中的电离方程式为___。
(3)⑤与⑧反应的离子方程式为___。
(4)向⑦的溶液中滴加①的溶液至Ba2+恰好完全沉淀,离子方程式为___。
(5)③与⑩反应的离子方程式如下,请配平方程式(在中填入系数,在横线上写上缺少的物质),并用“单线桥”标出电子转移的方向与数目。___
Cu+NO3-+ —Cu2++NO2↑+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列说法不正确的是
A.标况下,3.2g N2H4中含有的N-H键的数目为0.4NA
B.Cu与浓硝酸反应生成4.6 g NO2和N2O4混合气体时,转移的电子数为0.1NA
C.2 mol的CO2和H2O(g)的混合气体与过量Na2O2充分反应生成气体的分子数为NA
D.将1 mol Cl2通入足量水中,HClO、Cl-、ClO-的粒子数之和为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定相同体积、浓度均为0.l mol·L-1的三种弱酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是
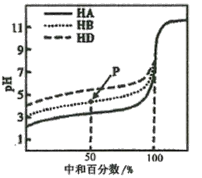
A.室温下,同浓度的NaA、NaB、NaD溶液的pH大小关系:pH(NaA)>pH(NaB)>PH(NaD)
B.滴定至P点时,溶液中:c(Na+)>c(B-)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)>c(B-)>c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、M、R为短周期元素,X、R在同一主族,![]() 与
与![]() 具有相同的电子层结构,X原子的L层电子数是K层电子数的2倍。判断下列说法正确的是
具有相同的电子层结构,X原子的L层电子数是K层电子数的2倍。判断下列说法正确的是
A.R的最高价氧化物对应水化物的酸性比Y的强
B.X、Y、M均可形成多种氧化物
C.X的简单气态氢化物的热稳定性比Y的强
D.离子半径的大小:r(![]() )>r(
)>r(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
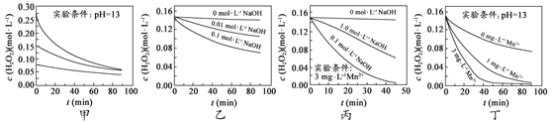
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com