
����Ŀ��ijһ��Ӧ��ϵ�е�������HCl��SnCl2��H2SnCl6��As��H3AsO3��H2O����֪��HCl�Ƿ�Ӧ��֮һ��As��������֮һ��
��1����д��δ��ƽ�ĸ÷�Ӧ�Ļ�ѧ����ʽ��_________________________
���ڸ÷�Ӧ�У��õ��ӵ�������__________����������Ԫ����____________��
���ڷ�Ӧ�У�ÿת��1 mol���ӣ�����HCl________mol��
����������������ȷ����_____________________(��д��ĸ���)��
a.����ͬ�����£��ڢ�A��Ԫ�ص������ӵĻ�ԭ�Դ��ϵ�������ǿ
b.�õ���Խ�������������������Խǿ
c.������ֻ����������
d.����ͬ�����£�������˳��Fe3+>Cu2+>H+>Fe2+
��2������ʢ��KI��Һ���Թ��м�������CCl4��μ���ˮ��CCl4������ɫ���÷�Ӧ�����ӷ���ʽΪ_________________________������������Թ��еμ���ˮ����CCl4�����dz���������ɫ���÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
�ڰ�KI����KBr����CCl4���Ϊ_______________ɫ�������μ���ˮ��CCl4�����ɫû�б仯��Cl2��HIO3��HBrO3��������ǿ������˳����___________________��
���𰸡�.HCl+SnCl2+H3AsO3![]() H2SnCl6+As+H2O H3AsO3 Sn 2 b.c Cl2+2I-=I2+2Cl- 5Cl2+I2+6H2O=2HIO3+10HCl �� HBrO3>Cl2>HIO3
H2SnCl6+As+H2O H3AsO3 Sn 2 b.c Cl2+2I-=I2+2Cl- 5Cl2+I2+6H2O=2HIO3+10HCl �� HBrO3>Cl2>HIO3
��������
��1����HCl�Ƿ�Ӧ��֮һ��������Ԫ�ء���Ԫ�صļ�̬����֪HCl�ڷ�Ӧ����������ã�HCl����Ԫ������ˮ����Ԫ���غ�֪H3AsO3�Ƿ�Ӧ�����As��SnԪ�ػ��ϼۼ�����ת���غ��֪��H3AsO3��������������ԭΪAs��SnCl2�ǻ�ԭ��������ΪH2SnCl������δ��ƽ�ķ�Ӧ����ʽΪHCl+SnCl2+H3AsO3![]() H2SnCl6+As+H2O��
H2SnCl6+As+H2O��
�ʴ�Ϊ��HCl+SnCl2+H3AsO3![]() H2SnCl6+As+H2O��
H2SnCl6+As+H2O��
����Ϸ���ʽ������As��SnԪ�ػ��ϼۿ�֪��H3AsO3��������������ԭΪAs��+2��Sn���ϼ�����Ϊ+4��������
�ʴ�Ϊ��H3AsO3��Sn��
���ɷ���ʽ��֪AsԪ����H3AsO3��+3�ۣ�����ΪAs��0�ۣ�ÿ1mol
H3AsO3��Ӧʱ����Ҫ����HCl6mol����ת��3mol��������6molHCl������ÿת��1mol���ӣ�����2mol HCl��
�ʴ�Ϊ��2��
�� a���ǽ�����Խǿ����Ӧ�����ӵĻ�ԭ��Խ��������ͬ�����£���VIIA��Ԫ�ش��ϵ��·ǽ��������������������ӵĻ�ԭ����ǿ����a��ȷ��
b��������Խǿ�õ�������Խǿ����õ��Ӷ����أ���b����
c���м��̬�ģ��Ⱦ����������־��л�ԭ�ԣ��磺Fe2+����c����
d��Cu��Fe3+��ӦCu+2Fe3+�TCu2++2Fe2+����������Fe3+������������Cu2+���������������Դ�����������������ԣ�����������Fe3+��Cu2+�������Խ�����ǿ���⣬��ǿ�ڽ���ͭ������������Cu2+��H+��Fe2+����������˳��Fe3+��Cu2+��H+��Fe2+����d��ȷ��
�ʴ�Ϊ��b c��
��2������������ǿ�����ԣ���ʢ��KI��Һ���Թ��м�������CCl4��μ���ˮ��CCl4������ɫ��˵������I2���������Թ��еμ���ˮ���� CCl4�����dz���������ɫ��˵��I2����һ������������HIO3��ͬʱ��������ԭΪHCl����Ӧ��Ϊ�����͵⡢ˮ���������ǵ�����Ȼ��⣬һ���������Ӳμӷ�Ӧ��2�����ӣ�һ������Ӳμӷ�Ӧʧȥ10�����ӣ��÷�Ӧ�е�ʧ���ӵ���С��������10�����Է���ʽΪ��5Cl2+I2+6H2O=2HIO3+10HCl
�ʴ�Ϊ��Cl2+2I-=I2+2Cl- ��5Cl2+I2+6H2O=2HIO3+10HCl
�������������Դ����壬�������������������������嵥�ʣ����������ӷ�Ӧ����ʽΪCl2+2Br=Br2+2Cl����ˮ�ʳ�ɫ����������ˮ�еμ���ˮ��CCl4�����ɫû�б仯��˵��������������С�����ᣬ�����ܺ͵ⷴӦ���ɵ��ᣬ���������������Դ��ڵ��ᣬ����Cl2��HIO3��HBrO3��������ǿ������˳�� HBrO3>Cl2>HIO3��
�ʴ�Ϊ���ȣ� HBrO3>Cl2>HIO3��


 ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������茶���[(NH4)2SO4��FeSO4��6H2O]�ֳ�Ħ���Σ��������Ҵ��������ڶ���������ijʵ��С�����ù�ҵ����м��ȡĦ���Σ����ⶨ�䴿�ȣ���������ͼ���¡�
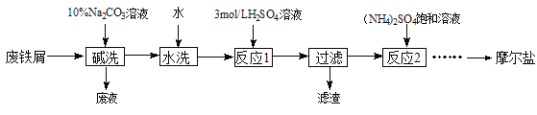
��֪������李�FeSO4��7H2O�������������ˮ�е��ܽ��
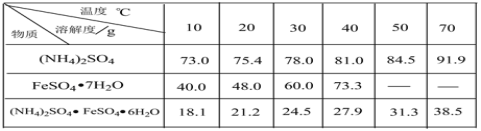
(1)��ϴ��Ŀ����_________��
(2)��Ӧ1�¶��������70~75�棬�ɲ�ȡ�Ĵ�ʩ��________��
(3)��Ӧ2�г���3 mol��L-1�����������Һ��pHΪ1��2����Ŀ����_______��
(4)�벹�������ɷ�Ӧ2������Һ�����������茶����ʵ�鷽����____�����ˡ����Ҵ�ϴ�ӡ����¸��
(5)Ϊ�ⶨ���������(NH4)2SO4��FeSO4��6H2O���崿�ȣ���������ʵ�飺
ȷ��ȡ0.4000g������������茶���������ƿ���ܽ⣬������ϡ�����ữ����0.0100 mol��L��1 ��KMnO4��Һ�ζ�����MnO![]() ǡ����ȫ����ԭΪMn2+ʱ������KMnO4��Һ�����Ϊ20.00 mL��
ǡ����ȫ����ԭΪMn2+ʱ������KMnO4��Һ�����Ϊ20.00 mL��
��ش��������⣺
�ٵζ��յ������Ϊ____________��
��������Ʒ��(NH4)2SO4��FeSO4��6H2O����(��Է�������Ϊ392)����������Ϊ______��
�������������Ļ����ϣ����д�ʩ�ܽ�һ����߲ⶨȷ�ȵ���_____������ĸ����
A���ʵ����ӳ�����Ʒ������ B�����������H2SO4��Һ
C���÷�̪��ָʾ�� D�����ʵ�飬ȡƽ��ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڱ�ǰ�����ڵ�Ԫ��a��b��c��d��e��ԭ��������������a�ĺ����������������������ͬ��b�ļ۵��Ӳ��е�δ�ɶԵ�����3����c������������Ϊ���ڲ��������3����d��cͬ�壻e�������ֻ��һ�����ӣ����������18�����ӣ��ش��������⣺
(1)b��c��d�е�һ�������ɴ�С��˳���ǣ�________________(��Ԫ�ط���)��e�ļ۲���ӹ��ʾ��ͼΪ__________________________________, e����ɫ��ӦΪ����ɫ������ԭ�ӽṹ��֪ʶ����ԭ��_____________________________
(2)a��b��c��d��e�γɵĶ�Ԫ���ۻ������кܶ��֣�������һ���ӳ������Σ��÷��ӵ�����ԭ�ӵ��ӻ���ʽΪ__________�����������ַ��ӣ��Ⱥ��м��Թ��ۼ����ֺ��зǼ��Թ��ۼ��Ļ�������_____________________(�ѧʽ)��
(3)��ЩԪ���γɵĺ������У����ӵ�����ԭ�ӵļ۲���Ӷ���Ϊ3����������_____��������ʽṹ�����ʵĹ�ϵ���ͣ�������������ǿ����ԭ����______________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ϵͳ������������������
��![]() __________________________
__________________________
�� _________________________
_________________________
��2���л��� ��ϵͳ������____�������ڴ������ڵ���������ȫ�⻯������������ϵͳ������ _______________________________________________��
��ϵͳ������____�������ڴ������ڵ���������ȫ�⻯������������ϵͳ������ _______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������I��C11H12O3�����Ʊ�Һ�����ϵ��м���֮һ��������к���ȩ����������I������E��H��һ�������ºϳɣ�
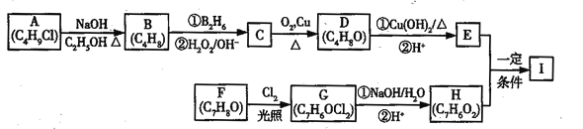
��֪������Ϣ��
��A�ĺ˴Ź������ױ�����ֻ��һ�ֻ�ѧ�������⣻
��R��CH=CH2![]() R��CH2CH2OH��
R��CH2CH2OH��
�ۻ�����F�����ϵ�һ�ȴ���ֻ�����֣�
��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ���
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ_______________________________��
��2��D�Ľṹ��ʽΪ_______________________________��
��3��E�еĹ���������Ϊ___________________________��
��4��F����G�Ļ�ѧ����ʽΪ__________________________���÷�Ӧ����Ϊ______________��
��5��I�Ľṹ��ʽΪ_________________________________��
��6��I��ͬϵ��J��I��Է�������С14��J��ͬ���칹������ͬʱ���������������ٱ�����ֻ������ȡ�������ڼ��ܷ���������Ӧ�������뱥��NaHCO3��Һ��Ӧ�ų�CO2������____�֣������������칹����J��һ��ͬ���칹�巢��������Ӧ���ữ��˴Ź�������Ϊ����壬�ҷ������Ϊ2:2:1��д��J������ͬ���칹��Ľṹ��ʽ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�������ɳ����ԭ�����͵���
A.ʵ�������ű���ʳ��ˮ�ķ����ռ�![]()
B.���Ṥҵ�У�ʹ�ù����Ŀ�������߶��������ת����
C.�ϳɰ���ҵ�У���ʱҺ������![]() ����ѭ������δ��Ӧ���
����ѭ������δ��Ӧ���![]() ��
��![]()
D.�ϳɰ���ҵ�У�500��ȳ��¸������ڰ��ĺϳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̶����ܱ������з�����Ӧ��![]() �����������в���˵��������Ӧ�Ѵﵽ��ѧƽ��״̬����
�����������в���˵��������Ӧ�Ѵﵽ��ѧƽ��״̬����
A.���������ܶȲ���
B.��ϵ��ѹǿ����
C.��������ƽ����Է�����������
D.��Ӧ��ϵ���Ҵ������ʵ���Ũ�Ȳ��ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ�����̼����ﴦ����Cu2+��ˮ��ý���ͭ����������м�ͻ���̿����������ʱ����÷�ˮ��Cu2+Ũ���ڲ�ͬ��̼������(x)��������ʱ��仯����������ͼ��ʾ��

������������������
A. ����̿��Cu2+����һ������������
B. ��м�ͻ���̿������Һ���γ���أ���Ϊ����
C. ������̼���������̼��(x)��һ������߷�ˮ��Cu2+��ȥ������
D. ������̼�������պ�Cu2+��ˮ��ͭ�ķ�Ӧԭ����Fe+Cu2+��Fe2++Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��һ������Ӫ��ǿ������һ������ˮ�ܿ���Ҫ�ɷ�Ϊ
��һ������Ӫ��ǿ������һ������ˮ�ܿ���Ҫ�ɷ�Ϊ![]() ��
��![]() ����������
����������![]() ��
��![]() ��MnO�ȣ�����ȡ
��MnO�ȣ�����ȡ![]() �Ĺ���������ͼ1��
�Ĺ���������ͼ1��
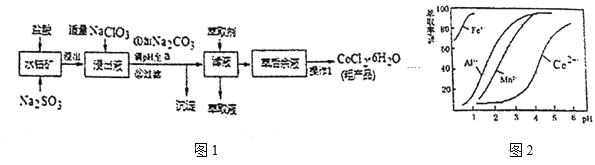
��֪��������Һ���е���������Ҫ��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() �ȣ�
�ȣ�
������������������������ʽ����ʱ��Һ��pH����������������Ũ��Ϊ��0.01mol/L��
��![]() �۵�Ϊ86����������110~120��ʱ��ʧȥ�ᾧˮ������ˮ�����ܡ�
�۵�Ϊ86����������110~120��ʱ��ʧȥ�ᾧˮ������ˮ�����ܡ�
������ |
|
|
|
|
|
��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��1��д������������![]() ������Ӧ�����ӷ���ʽ____��
������Ӧ�����ӷ���ʽ____��
��2��д��NaClO3������Ӧ����Ҫ���ӷ���ʽ____����������������Һ���мӹ���NaClO3ʱ�����ܻ������ж����壬д�����ɸ��ж���������ӷ���ʽ____��
��3������![]() ��pH��a�����������õ��ij����ɷ�Ϊ___��
��pH��a�����������õ��ij����ɷ�Ϊ___��
��4���Ƶõ�![]() �ں��ʱ���ѹ��ɵ�Դ����___��
�ں��ʱ���ѹ��ɵ�Դ����___��
��5����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ2��������Һ���м�����ȡ����Ŀ����___�r��ʹ�õ����pH��Χ��___��
A��2.0~2.5 B��3.0~3.5 C��4.0~4.5 D��5.0~5.5
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com