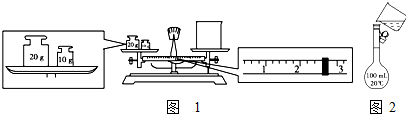
分析:(1)天平称量物体时遵循左物右码的原则,天平平衡原理:左盘物体质量=右盘砝码质量+游码质量;
(2)配制一定物质的量浓度的溶液实验,在移液时,要用玻璃棒引流,配制多大体积的溶液要采用多大体积的容量瓶;
(3)①根据c=
计算浓H
2SO
4的物质的量浓度,再根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
②根据配制一定物质的量浓度的溶液的配制步骤选择使用的仪器;
③根据C=
,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差.
解答:
解:(1)天平称量物体时遵循左物右码的原则,在该实验图中可以看出,该同学在操作时的一个错误是砝码与烧杯放反了位置,根据天平平衡原理:左盘物体质量=右盘砝码质量+游码质量,若果放反了,则左盘砝码质量=右盘物体质量+游码质量,所以右盘物体质量=左盘砝码质量-游码质量=30-2.6=27.4,
故答案为:砝码与烧杯放反了位置;27.4;
(2)配制一定物质的量浓度的溶液实验,在移液时,要用玻璃棒引流,右图该同学在转移溶液时没有用玻璃棒引流,配制150mL的溶液要采用150mL的容量瓶,
故答案为:未用玻璃棒引流;应用150 mL容量瓶;
(3)①浓H
2SO
4的物质的量浓度c=
mol/L=18.4mol/L;
根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则有:
xmL×18.4mol/L=1000mL×0.1mol/L,解得:x≈5.4,故答案为:5.4;②作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.由提供的仪器可知还需要仪器有玻璃棒、烧杯、1 000 mL容量瓶、胶头滴管,
故答案为:玻璃棒、烧杯、1 000 mL容量瓶、胶头滴管;
③A、生锈的砝码质量偏大,而m
物=m
砝+m
游,故称量出的药品的质量偏重,则配制出的溶液的浓度偏大;
B、将NaOH放在纸张上称量会潮解,导致真正的NaOH的质量偏小,则配制出的溶液的浓度偏小;
C、定容时俯视刻度线,溶液体积偏小,则浓度偏大;
D、往容量瓶转移时,有少量液体溅出,会导致溶质的损失,则溶液浓度偏小;
E、未洗涤溶解NaOH的烧杯,会导致溶质的损失,则溶液浓度偏小;
F、定容时仰视刻度线,会导致溶液体积偏大,则浓度偏小;
G、只要最后定容时凹液面与刻度线相切即可,至于水是事先就有的还是后来加入的,对浓度无影响;
H、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线是正常的,再加水至刻度线导致浓度偏小.
故答案为:AC.




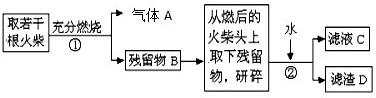
 .请回答下列问题:
.请回答下列问题: