
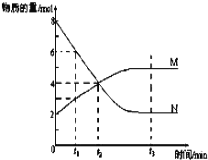
����Ŀ��I��һ���¶��£�ij�ݻ�Ϊ2 L���ܱ������ڣ�ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯����������ͼ����ͼ��ʾ��
��1���÷�Ӧ�Ļ�ѧ����ʽ��____________________________��
��2����ͼ����ʾ������ʱ���У�_______����t1��t2��t3��ʱ�̴ﵽ��ѧ��Ӧ����
II��һ���¶��½�6 mol A��6 mol B�����2 L���ܱ������У�
�������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(g)������5���Ӻ�Ӧ�ﵽƽ�⣬���A��ת����Ϊ60%��C��ƽ����Ӧ������0.36 mol/��L��min������
xC(g)+2D(g)������5���Ӻ�Ӧ�ﵽƽ�⣬���A��ת����Ϊ60%��C��ƽ����Ӧ������0.36 mol/��L��min������
��1��ƽ��ʱD��Ũ��=___________________��
��2��B��ƽ����Ӧ������(B)= ___________________________��
��3��x=_________��
��4����ʼʱ�����е�ѹǿ��ƽ��ʱ��ѹǿ֮��Ϊ______________����Ϊ��������ȣ���
���𰸡� 2N![]() M t3 1.2 mol��L�C1 0.12 mol��L�C1��min�C1 3 10:11
M t3 1.2 mol��L�C1 0.12 mol��L�C1��min�C1 3 10:11
��������(1)��ͼ��֪��N����8-2=6��M����5-2=3��NΪ��Ӧ�MΪ������ұ仯��֮��Ϊ2��1������ѧ������֮��Ϊ2��1����ӦΪ2N(g) ![]() M(g)���ʴ�Ϊ��2N(g)
M(g)���ʴ�Ϊ��2N(g) ![]() M(g)��
M(g)��
(2)�����ʵ�����ʱ��ı仯���������仯ʱΪƽ��״̬����ͼ��֪��t3Ϊƽ��״̬���ʴ�Ϊ��t3��
3A(g)+B(g) ![]() xC(g)+2D(g)������5���Ӻ�Ӧ�ﵽƽ�⣬���A��ת����Ϊ60%����
xC(g)+2D(g)������5���Ӻ�Ӧ�ﵽƽ�⣬���A��ת����Ϊ60%����
3A(g)+B(g) ![]() xC(g)+2D(g)��
xC(g)+2D(g)��
��ʼ(mol/L) 33 00
ת��3��60%0.60.6x1.2
ƽ��1.22.40.6x1.2
(1)������������֪ƽ��״̬D��Ũ��Ϊ1.2mol/L���ʴ�Ϊ��1.2mol/L��
(2)B��ƽ����Ӧ���ʦ�(B)= ![]() =0.12mol/(L��min)���ʴ�Ϊ��0.12mol/(L��min)��
=0.12mol/(L��min)���ʴ�Ϊ��0.12mol/(L��min)��
(3)������֮�ȵ��ڻ�ѧ������֮�ȿ�֪�� ![]() =
=![]() �����x=3���ʴ�Ϊ��3��
�����x=3���ʴ�Ϊ��3��
(4)��ʼʱ�����е�ѹǿ��ƽ��ʱ��ѹǿ֮�ȵ��ڷ�Ӧǰ������ʵ���֮�͵ıȣ�Ϊ(6+6)mol��(1.2+2.4+0.6��3+1.2)mol/L��2L=10��11���ʴ�Ϊ��10��11��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���þƾ��ƶ�����ʵ����������ʱ����������ʯ�������ǣ� ��
A.�Թ�
B.�ձ�
C.��ƿ
D.������ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ˮ��Һ�ֳ�Ϊ˫��ˮ��������������ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹��������Ũ�ȣ�����д���пհף�
��1����10.00 mL����������Һ��ȡ��250mL �����������ƣ��У���ˮϡ�����̶ȣ�ҡ�ȡ���ȡϡ�ͺ�Ĺ���������Һ25.00mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
��2���ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽ���£��뽫������ʵĻ�ѧ����������ѧʽ��д�ڷ����
MnO4���� H2O2�� H��= Mn2���� H2O��______�� ��
��3����ȡ10mL����������Һ������ �����ʽ����ʽ�����ζ��ܡ��ζ������յ�������� ��
��4���ظ��ζ����Σ�ƽ������cmol/L KMnO4����ҺVmL����ԭ����������Һ�й��������Ũ��Ϊ ��
��5����ʢװ������ر���Һ�ĵζ���������ˮϴ��û���ñ�Һ��ϴ����ⶨ��� ���ƫ�ߡ���ƫ�͡����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ��Ӧ���ʵ�˵����ȷ������ ��
A. ����Ƭ��ϡ���ᷴӦ��ȡ����ʱ������98%��Ũ������Լӿ��������������
B. 2mol/ L100ml�������пƬ��Ӧ�������������Ȼ�����Һ����Ӧ���ʲ���
C. SO2�Ĵ�������һ�����ȵķ�Ӧ�����������¶ȣ���Ӧ���ʼ���
D. ����β���е�NO��CO���Ի�����Ӧ����N2��CO2����Сѹǿ��Ӧ���ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ�����ȷ���� (����)
A. ʯ�͡�ú��С�մ��ǻ���� B. �ռ�����ʯ�Ҷ��Ǽ�
C. HNO3��NaOH��NaNO3���ǵ���� D. HCl��H2SO4��NaOH�������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и�������һ������ָ����Һ�д����������
A. pH=l ����Һ�У�Ba2+��Fe3+ ��Cl-��SCN-
B. ��ʹ��̪������Һ��Ca2+��K+��HCO3-��CO32-
C.  =10-12����Һ�У�NH4+��Cu2+��NO3-��SO42-
=10-12����Һ�У�NH4+��Cu2+��NO3-��SO42-
D. ��ˮ�����c(H+)=10-12mol��L-1����Һ�У�Na+��Al3+��Cl-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���㲻ͬ����Ҫ������Ӧ��ԭ���ԭ�������˶��ֵ�ء�
��1�������Ի�ѧ��Ӧ2Zn+O2+4H+=2Zn2++2H2OΪ�������һ��ԭ��أ�������������Ϊ������������Դ�����ǿ�������ѪҺ������һ��Ũ�ȵ�O2��H+��Zn2+���й��������ԭ��ظ����ĵ缫��ӦΪ___________��
��2��FeCl3��Һ�����ڸ�ʴӡˢ��·ͭ�壬�䷴Ӧ�����ӷ���ʽΪ________________�������˷�Ӧ��ƻ�ԭ��أ������õ缫����Ϊ___________��������ӦΪ_________________��
��3����������������ɴ���ʹ����һ�����ͷ���װ�á�����ȼ�ϵ�أ��乹����ͼ��ʾ������A��B�����缫���ɶ��̼Ȳ��ɣ��õ�ص�������ӦʽΪ_________________�����õ�ع���ʱ��Һ������1molH2O���������ϵ�·��ͨ�����ӵ����ʵ���Ϊ_______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ᡢ�������������Һ�д�������ƽ�⼰���Ӧ��ƽ�ⳣ��
CH3COOH![]() CH3COO����H�� ��H1��0 (K1��1.75��10��5)
CH3COO����H�� ��H1��0 (K1��1.75��10��5)
CH3COO����H2O![]() CH3COOH��OH�� ��H2��0 ( K2��5.71��10��10 )
CH3COOH��OH�� ��H2��0 ( K2��5.71��10��10 )
�����£���������������ʵ���Ũ�ȵĴ���ʹ�������Һ��ϣ�����������ȷ����( )
A�������ҺpH��7
B���Ի����Һ�����ȣ�K1����K2��С
C�����ڻ����Һ��pH�����ԣ����ʱ��Һ��c(Na��)��c(CH3COO��)
D���¶Ȳ��䣬���ڻ����Һ�м�������NaOH���壬c(CH3COO��)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƿ�������������ʵ���Ũ�ȵ���Һ�Ķ������������ϱ��У����¶ȡ���Ũ�ȡ�����������ѹǿ�����̶����������еģ� ��
A. �ڢ� B. �ۢ� C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com