
【题目】节能减排、开发新能源目前受到国际社会的高度关注。
(1)近年我国努力开发新能源,调整能源结构。下列属于可再生能源的是_______(填字母)。
A.氢能 B.天然气 C.石油 D.生物质能
(2)工业生产中会产生SO2、H2S等有害气体,可采取多种方法进行处理。
I.生物法脱H2S的原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(S04)3+2H2O
2Fe2(S04)3+2H2O
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_______。
②由图1和图2判断使用硫杆菌的最佳条件为_____。若反应温度过高,反应速率下降,其原因是_____。

I.双碱法去除SO2的原理是先用NaOH溶液吸收SO2,再用CaO使NaOH再生。
NaOH溶液![]() Na2SO3溶液
Na2SO3溶液
写出过程①的离子方程式:______________。
(3)人们也利用多种方法回收利用烟气用的有害气体,变废为宝。如果利用NaOH溶液、石灰和O2处理硫酸工厂尾气中的SO2使之最终转化为石膏(CaSO4·2H2O),假设硫元素不损失,每天处理1000m3(标准状况)含0.2%(体积分数)SO2的尾气,理论上可以得到多少千克石膏 (计算结果保留小数点后一位)?_______
【答案】 AD 催化作用 30℃、pH=2.0 蛋白貭变性(或硫杆菌失去活性),使催化剂失去催化作用 2OH-+SO2=SO32-+H2O 15.4kg
【解析】再生能源是指在自然界能反复生成的。SO2是酸性氧化物,能和碱反应生成盐和水。二氧化硫与石灰乳反应生成亚硫酸钙与水,亚硫酸钙在水存在的条件下被氧气氧化生成CaSO4·2HO,根据关系式SO2--CaSO4.2H2O来计算生成石膏。
(1)煤、石油、天然气以及核能短期内从自然界得不到补充,属于不可再生能源,而太阳能、氢能可以从自然界源源不断的得到补充,属于可再生能源,所以AD选项正确的。
(2)①根据生物脱的H2S原理可知:硫杆菌在反应中充当催化剂,可以降低反应所需活化能,加快反应速率,因此硫杆菌存在时,FeSO4被氧化的速率远大于无菌时FeSO4被氧化的速率。答案:催化作用。
②由两图可知,在30![]() 、PH=2.0时,硫杆菌对Fe2+的氧化速率最大;温度过高,反应速率下降的原因是高温使得硫杆菌蛋白质变性,失去活性,催化作用。答案:30
、PH=2.0时,硫杆菌对Fe2+的氧化速率最大;温度过高,反应速率下降的原因是高温使得硫杆菌蛋白质变性,失去活性,催化作用。答案:30![]() 、PH=2.0
、PH=2.0
(2)过程①中NaOH溶液与SO2反应生成Na2SO3, 离子方程式为2OH-+SO2=SO32-+H2O。
(3) 二氧化硫与石灰乳反应生成亚硫酸钙与水,亚硫酸钙在水存在的条件下被氧气氧化生成二水合硫酸钙即石膏,根据关系式计算:设理论上可得到mg的石膏,则有SO2--CaSO4.2H2O,1molSO2生成172g石膏,根据硫原子守恒,m(CaSO4·2HO)=[(1000×1000)L/22.4(L· mol-1)]×0.2%×172 g· mol-1=15357 g≈15.4 kg。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列关于该装置的说法正确的是

A. 外电路的电流方向为X![]() 外电路
外电路![]() Y
Y
B. 若两电极分别为Fe和碳棒,则X 为碳棒,Y 为Fe
C. X 极上发生的是还原反应,Y 极上发生的是氧化反应
D. 若两电极都是金属,则它们的活泼性顺序为X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置进行实验,能达到相应实验目的的是

A. 图甲可用于蒸馏石油并收集60~150℃馏分
B. 图乙可用于除去乙烯气体中混有的少量SO2
C. 图丙装置可用于比较S、C、Si三种元素的非金属性
D. 图丁装置可用于测定CO2的生成速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] 有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
Ⅰ.配制含0.10mol FeSO4的绿矾溶液。
Ⅱ.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL 1.1mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
Ⅲ.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
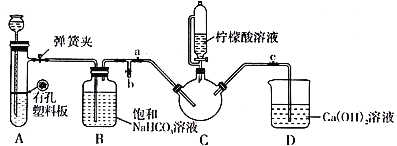
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为_______(写化学式)。再滴加少量稀硫酸的作用是__________________________。
(2)实验II中:生成沉淀的离子方程式为__________________________。
(3)实验Ⅲ中:①C中盛柠檬酸溶液的仪器名称为___________________。
②装置A中所盛放的药品是___________________。(填序号)
A.Na2CO3和稀H2SO4 B.CaCO3和稀H2SO4 C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是____________________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是________________。
⑤洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是___________________。(填序号)
A.热水 B.乙醇溶液 C.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国天然气化工的一项革命性技术是甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳烃等化工产品。以甲烷为原料合成部分化工产品流程如下(部分反应条件已略去):

(1)A、C分子中所含官能团的名称分别为____、_______。
(2)写出A的同分异构体的结构简式:_______。
(3)写出下列反应的化学方程式和反应类型。
反应①:__________,反应类型:_____________;
反应②:___________;反应类型: _____________;
反应③:_____________,反应类型:_____________。
(4)下图为实验室制取D的装置图。

①图中试剂a名称为_______,其作用是______________。用化学方程式表示试剂a参与的化学反应:______________。
②实验结束后从混合物中分离出D的方法为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5molL﹣1的盐酸10mL稀释到200mL,从中取出5mL,这5mL溶液的物质的量浓度为( )
A.0.5 molL﹣1
B.0.25 molL﹣1
C.0.1 molL﹣1
D.1 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。

下列说法不正确的是
A. 电流从右侧电极经过负载后流向左侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为:2NH3-6e-=N2+6H+
D. 当有4.48LNO2(标准状况) 被处理时,转移电子为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中有如下反应:mA(g)+nB(g)pC(g)达到平衡后,保持温度不变,将容器体积缩小到原来的 ![]() ,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是( )
,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是( )
A.m+n>p
B.A的转化率降低
C.平衡向正反应方向移动
D.C的质量分数增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com